
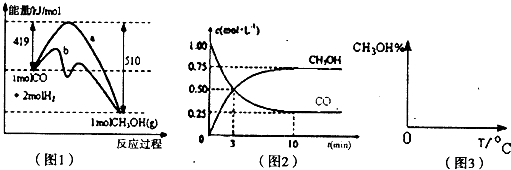
| n(CH3OH) |
| n(CO) |
| 1mol/L-0.25mol/L |
| 10min |
| 4mol-3mol |
| 2L |
| 0.75 |
| 0.25×0.52 |
 ,
, .
.

 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.B的生成速率与A的消耗速率相等 |
| B.体系的质量不再发生变化 |
| C.A、B、C的浓度之比为1:1:2 |
| D.每消耗1mol A同时生成2mol C |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.混合气体的密度保持不变 |
| B.容器内B、C的浓度之比为2:1 |
| C.B的生成速率等于C的消耗速率 |
| D.气体的体积分数保持不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 一定条件 |
| 时间/min | 0 | 30 | 70 | 80 | 100 |
| n(CO2)/mol | 0.10 | 0.060 | 0.040 | 0.040 | 0.040 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
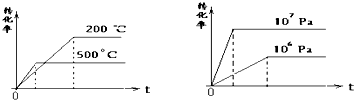
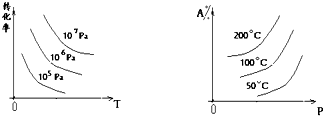
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.P1>P2,n<3 | B.P1<P2,n>3 | C.P1>P2,n>3 | D.P1<P2,n<3 |
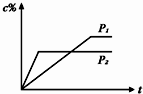
查看答案和解析>>
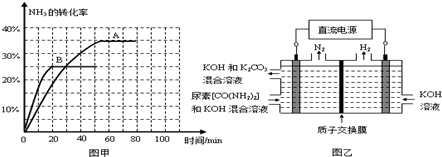
科目:高中化学 来源:不详 题型:单选题
| 一定条件 |
| n(NH3) |
| n(CO2) |
| A.该反应在60min时达到平衡状态 |
| B.NH3的平衡转化率为30% |
| C.增加氨碳比可进一步提高CO2的平衡转化率 |
| D.A点的逆反应速率υ逆(CO2)大于B点的正反应速率υ正(CO2) |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.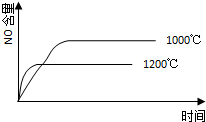 | B.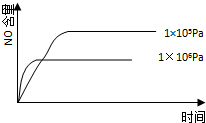 |
C.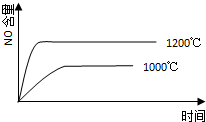 | D.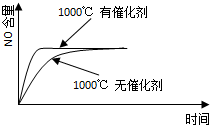 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com