
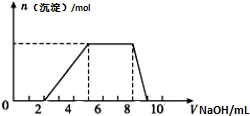
 某溶液中可能含有如下离子:H+、Mg2+、Al3+、NH4+、Cl-、AlO2-.当向该溶液中逐滴加入NaOH溶液时,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
某溶液中可能含有如下离子:H+、Mg2+、Al3+、NH4+、Cl-、AlO2-.当向该溶液中逐滴加入NaOH溶液时,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )| A、原溶液中一定含有的阳离子是H+、Mg2+、Al3+、NH4+ |
| B、反应最后形成的溶液中的溶质含AlCl3 |
| C、原溶液中Al3+与NH4+的物质的量之比1:3 |
| D、原溶液中含有的阴离子是AlO2-、Cl- |


科目:高中化学 来源: 题型:
| A、加入Ba(NO3)2溶液生成白色沉淀,加入稀盐酸后沉淀不消失,则原溶液中一定含有SO42- |
| B、通入氯气后,溶液变黄色,加入淀粉溶液后变蓝,则原溶液中一定有I- |
| C、加入碳酸钠溶液有白色沉淀生成,再加入盐酸,沉淀消失,则原溶液中一定含有Ba2+ |
| D、加入氢氧化钠溶液并加热,产生能使湿润的蓝色石蕊试纸变红的气体,则原溶液中一定有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
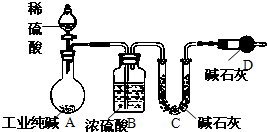 工业纯碱中常常含有NaCl、Na2SO4等杂质.为测定某工业纯碱的纯度,设计了如图实验装置.依据实验设计,请回答:
工业纯碱中常常含有NaCl、Na2SO4等杂质.为测定某工业纯碱的纯度,设计了如图实验装置.依据实验设计,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、-128.1 kJ?mol-1 |
| B、-411.1 kJ?mol-1 |
| C、-157.7 kJ?mol-1 |
| D、+157.7 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
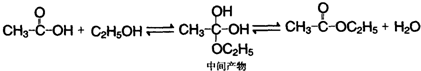
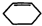 )为原料,通过以下各步转化,最终可制得有机物
)为原料,通过以下各步转化,最终可制得有机物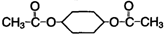 (部分反应过程及反应条件略去)
(部分反应过程及反应条件略去)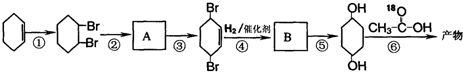
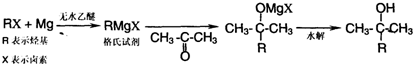
查看答案和解析>>
科目:高中化学 来源: 题型:
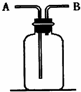 根据正放在桌面上的如图装置,回答下列问题:
根据正放在桌面上的如图装置,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
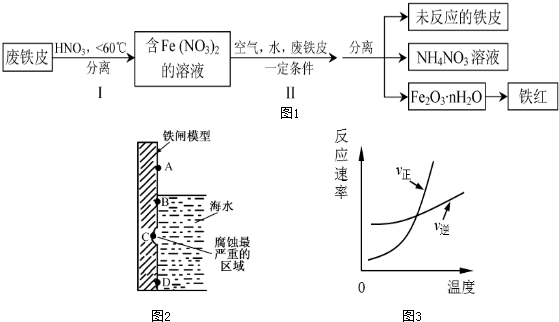
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com