
 .
.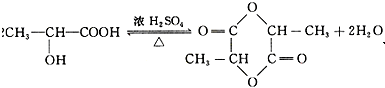 .
. .
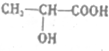
.分析 (1)乳酸的物质的量为$\frac{90g}{90g/mol}$=1mol,-OH、-COOH均与Na反应生成氢气;-OH、-COOH可发生酯化反应生成环状的酯;
(2)1mol葡萄糖中含5mol-OH;
(3)C6H12的某烃,其所有的碳原子都一定在同一平面上,乙烯为平面结构,则每个双键C上各连2个C;
(4)某苯的同系物分子式为C11H16,苯环上只有一个取代基,取代基为:-C5H11,戊烷的同分异构体有:①正戊烷CH3CH2CH2CH2CH3、②异戊烷CH3CH2CH(CH3)CH3 和③新戊烷 C(CH3)4,取代基的数目决定同分异构体的数目.
解答 解:(1)醋酸含有羧基和羟基,乳酸的物质的量为$\frac{90g}{90g/mol}$=1mol,-OH、-COOH均与Na反应生成氢气,则生成1mol氢气,其体积为22.4 L,反应为CH2OHCH2COOH+2Na→CH2(ONa)CH2COONa+H2↑,两分子乳酸可在一定条件下反应生成环状的酯的方程式为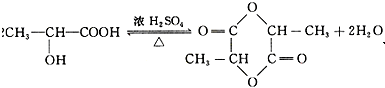 ,
,
故答案为:羧基;羟基;22.4;CH2OHCH2COOH+2Na→CH2(ONa)CH2COONa+H2↑;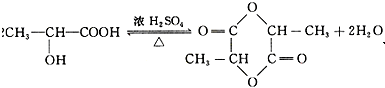 ;
;
(2)1mol葡萄糖中含5mol-OH,-OH与醋酸以1:1发生酯化反应,则消耗醋酸为5mol,故答案为:5;
(3)C6H12的某烃,其所有的碳原子都一定在同一平面上,乙烯为平面结构,则每个双键C上各连2个C,C6H12可看做乙烯中的四个氢原子被甲基取代,故结构简式为: ,故答案为:
,故答案为: ;
;
(4)某苯的同系物分子式为C11H16,苯环上只有一个取代基,取代基为:-C5H11,戊烷的同分异构体有:①正戊烷CH3CH2CH2CH2CH3、②异戊烷CH3CH2CH(CH3)CH3 和③新戊烷 C(CH3)4,取代基的数目决定同分异构体的数目,则其中①正戊烷分子中氢原子被苯环取代所得的同分异构体有三种,分别为: 、
、 、
、 ;
;
②异戊烷中氢原子被苯环取代的同分异构体有四种:
③新戊烷中氢原子被苯环确定的同分异构体有1种,其结构简式为: ,
,
所以苯的同系物分子式为C11H16,苯环上只有一个取代基,其同分异构体共有8种,
故答案为:8.
点评 本题考查了钠与乳酸的反应、同分异构体的求算,题目难度中等,该题综合性较高,(4)中考查了苯的同系物的同分异构体的书写,难度较大,注意同分异构体的求算方法.


 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.22 mol/L | B. | 0.11 mol/L | C. | 0.022 mol/L | D. | 0.011 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 1 | 6 | 4 | x |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mn>Cu | B. | Al>Mn | C. | Mg>Al | D. | Mn>Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H3PO2溶于水的电离方程式为:H3PO2?3H++PO23- | |
| B. | H3PO2与过量NaOH溶液反应的离子方程式为:H3PO2+3OH-=PO23-+3H2O | |
| C. | 将H3PO2溶液加入到酸性高锰酸钾溶液中,H3PO2的还原产物为H3PO4 | |
| D. | 用惰性电极电解NaH2PO2溶液,其阳极反应式为:H2PO2-4e-+2H2O=O2↑+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 温州某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
温州某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:| 滴定次数 | 待测液体积/mL | 标准溶液的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | |||
| 1 | 20 | 1.02 | 21.03 | |
| 2 | 20 | 2.00 | 25.00 | |
| 3 | 20 | 0.60 | 20.60 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com