
在温度和容积不变的密闭容器中,A气体与B气体反应生成C气体。反应过程中,反应物与生成物的浓度随时间变化的曲线如下图,则下列叙述正确的是

A.该反应的化学方程式为A+3B  2C
2C
B.在tl s时,v(A)正=0
C.(t1+l0)s时再充入0.4 molA和0.25 mol B,反应物A的转化率增大
D.若该反应在绝热容器中进行,也在tl时刻达到平衡
C
【解析】
试题分析:A.根据反应方程式可知在相同的时间内,A减少0.6mol/L;B减少0.2mol/L;C增加0.4mol/L,最终各种物质都存在处于平衡状态,因此该反应的化学方程式为3A+B  2C,错误;B.在tl s时,反应处于平衡状态,各种物质的正反应速率与逆反应速率相等但是都大于0,错误;C.(t1+l0)s时再充入0.4 molA和0.25 mol B,即增大了压强,平衡正向移动,所以反应物A的转化率增大,正确;D.任何反应都伴随着能量变化,因此若该反应在绝热容器中进行,该反应在达到平衡的时间可能比tl时刻早,也可能晚,错误。
2C,错误;B.在tl s时,反应处于平衡状态,各种物质的正反应速率与逆反应速率相等但是都大于0,错误;C.(t1+l0)s时再充入0.4 molA和0.25 mol B,即增大了压强,平衡正向移动,所以反应物A的转化率增大,正确;D.任何反应都伴随着能量变化,因此若该反应在绝热容器中进行,该反应在达到平衡的时间可能比tl时刻早,也可能晚,错误。
考点:考查化学反应方程式的书写及外界条件对化学反应速率、物质的转化率及平衡的影响的知识。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2015届河南省顶级名校高三入学定位考试化学试卷(解析版) 题型:选择题
将0.4gNaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是 ( )
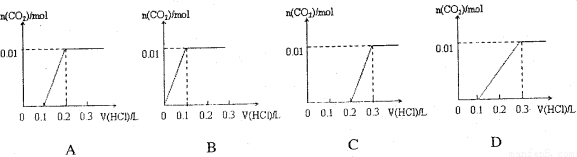
查看答案和解析>>
科目:高中化学 来源:2015届河北省邯郸市高三第一次调研考试化学试卷(解析版) 题型:填空题
下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
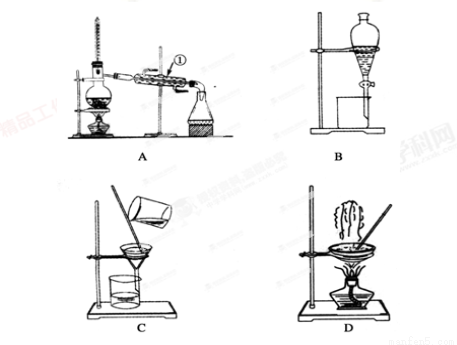
(1)从氯化钾溶液中得到氯化钾固体,选择装置________(填代表装置图的字母,下同);除去自来水中 的Cl-等杂质,选择装置________________。
(2)从碘水中分离出I2,选择装置________,该分离方法的名称为________________。
(3)装置A中①的名称是________,进水的方向是从________口进水。装置B在分液时为使液体顺利下滴,应进行的具体操作是_________________________________________。
查看答案和解析>>
科目:高中化学 来源:2015届河北省邯郸市高三第一次调研考试化学试卷(解析版) 题型:选择题
在某体系内有反应物和生成物5种物质:H2S、S、FeCl3、FeCl2、HCl.已知H2S为反应物,则另一反应物是( )
A.FeCl3 B.FeCl2 C.S D.HCl
查看答案和解析>>
科目:高中化学 来源:2015届河北省唐山市高三年级摸底考试理综化学试卷(解析版) 题型:填空题
(15分)工业上研究燃料脱硫的过程中,涉及如下反应:
CaSO4(s)+CO(g)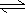 CaO(s)+SO2(g)+CO2(g),K1,△H1= 218.4 kJ·mol-l(反应I)
CaO(s)+SO2(g)+CO2(g),K1,△H1= 218.4 kJ·mol-l(反应I)
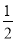 CaSO4(s)+2CO(g)
CaSO4(s)+2CO(g)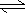
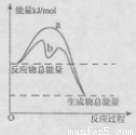
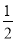 CaS(s)+2CO2(g),K2,△H2= -87.8 kJ·mol-l(反应II)
CaS(s)+2CO2(g),K2,△H2= -87.8 kJ·mol-l(反应II)
(1)反应CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g)的△H= ;平衡常数K=____ (用K1,K2表示)。
CaS(s)+3CO2(g)的△H= ;平衡常数K=____ (用K1,K2表示)。
(2)某温度下在一密闭容器中若只发生反应I,测得数据如下:

前100 s 内v(SO2)= mo1·L-1·s-l,平衡时CO的转化率为 。
(3)若只研究反应II,在不同条件下其反应能量变化如下图所示:图中曲线a到曲线b的措施是________,恒温恒容时,下列说法能说明反应Ⅱ到达平衡状态的是____ 。
A.体系中气体的平均摩尔质量不再改变
B.v(CO)=v(CO2)
C.CO的转化率达到了最大限度
D.体系内气体压强不再发生变化
(4)某科研小组研究在其它条件不变的情况下,改变起始一氧化碳物质的量[用n(CO)表示]对CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g)反应的影响,实验结果如右图所示(图中T表示温度):
CaS(s)+3CO2(g)反应的影响,实验结果如右图所示(图中T表示温度):

①比较在a、b、c三点所处的平衡状态中,反应物SO2的转化率最高的是
____ 。
②图像中T2 T1(填“高于”、“低于”、“等于”或“无法确定”):判断的
理由是____ 。
查看答案和解析>>
科目:高中化学 来源:2015届河北省“五个一名校联盟”高三教学质量监测(一)化学试卷(解析版) 题型:填空题
【化学—选修5:有机化学基础】(15分)
有机化合物J是治疗心脏病药物的一种中间体,分子结构中含有3个六元环。其中一种合成路线如下:
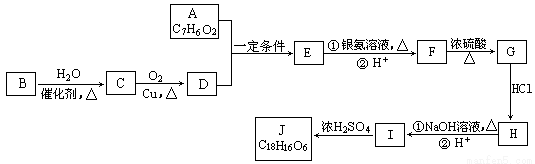
已知:
①A既能发生银镜反应,又能与FeCl3溶液发生显色反应,其核磁共振氢谱显示有4种氢,且峰面积之比为1︰2︰2︰1。
②有机物B是一种重要的石油化工产品,其产量可用来衡量国家的石油化工发展水平。
③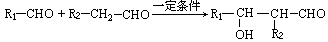
回答以下问题:
(1)A中含有的官能团名称是。
(2)写出有机反应类型B→C,F→G,I→J。
(3)写出F生成G的化学方程式 。
(4)写出J的结构简式。
(5)E的同分异构体有多种,写出所有符合以下要求的E的同分异构体的结构简式
。
FeCl3溶液发生显色反应 ②能发生银镜反应 ③苯环上只有两个对位取代基 ④能发生水解反应。
查看答案和解析>>
科目:高中化学 来源:2015届河北省“五个一名校联盟”高三教学质量监测(一)化学试卷(解析版) 题型:选择题
美国圣路易斯大学研制新型的乙醇燃料电池,用质子(H+)溶剂,在200oC左右供电。电池总反应为:C2H5OH+3O2→2CO2+3H2O,下图是该电池的示意图,下列说法正确的是

A.a极为电池的正极
B.电池工作时电流由a极沿导线经灯泡再到b极
C.电池正极的电极反应为:4H+ + O2 + 4e-=2H2O
D.电池工作时,1mol乙醇被氧化时就有6mol电子转移
查看答案和解析>>
科目:高中化学 来源:2015届河北省“五个一名校联盟”高三教学质量监测(一)化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.沼气和水煤气都是可再生能源
B.石油裂解和油脂皂化都有高分子生成小分子的过程
C.不能用植物油萃取溴水中的溴
D.可以用加热使蛋白质变性的方法分离提纯蛋白质
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三暑期化学试卷(解析版) 题型:选择题
在t ℃时,将a g NH3完全溶于水,得到V mL溶液,设该溶液的密度为ρ g·cm3,质量分数为w,其中含NH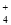 的物质的量为b mol。下列叙述中不正确的( )。
的物质的量为b mol。下列叙述中不正确的( )。
A.溶质的质量分数w= ×100%
×100%
B.溶质的物质的量浓度c=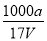 mol·L-1
mol·L-1
C.溶液中c(OH-)=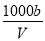 mol·L-1+c(H+)
mol·L-1+c(H+)
D.上述溶液中再加入V mL水后,所得溶液中溶质的质量分数小于0.5 w
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com