
(15分)工业上研究燃料脱硫的过程中,涉及如下反应:
CaSO4(s)+CO(g)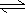 CaO(s)+SO2(g)+CO2(g),K1,△H1= 218.4 kJ·mol-l(反应I)
CaO(s)+SO2(g)+CO2(g),K1,△H1= 218.4 kJ·mol-l(反应I)
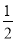 CaSO4(s)+2CO(g)
CaSO4(s)+2CO(g)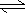
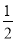 CaS(s)+2CO2(g),K2,△H2= -87.8 kJ·mol-l(反应II)
CaS(s)+2CO2(g),K2,△H2= -87.8 kJ·mol-l(反应II)
(1)反应CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g)的△H= ;平衡常数K=____ (用K1,K2表示)。
CaS(s)+3CO2(g)的△H= ;平衡常数K=____ (用K1,K2表示)。
(2)某温度下在一密闭容器中若只发生反应I,测得数据如下:

前100 s 内v(SO2)= mo1·L-1·s-l,平衡时CO的转化率为 。
(3)若只研究反应II,在不同条件下其反应能量变化如下图所示:图中曲线a到曲线b的措施是________,恒温恒容时,下列说法能说明反应Ⅱ到达平衡状态的是____ 。
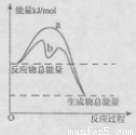
A.体系中气体的平均摩尔质量不再改变
B.v(CO)=v(CO2)
C.CO的转化率达到了最大限度
D.体系内气体压强不再发生变化
(4)某科研小组研究在其它条件不变的情况下,改变起始一氧化碳物质的量[用n(CO)表示]对CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g)反应的影响,实验结果如右图所示(图中T表示温度):
CaS(s)+3CO2(g)反应的影响,实验结果如右图所示(图中T表示温度):

①比较在a、b、c三点所处的平衡状态中,反应物SO2的转化率最高的是
____ 。
②图像中T2 T1(填“高于”、“低于”、“等于”或“无法确定”):判断的
理由是____ 。
(1)-394kJ/mol (2分) 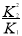 (2分);(2)0.009(1分) 60%(2分);
(2分);(2)0.009(1分) 60%(2分);
(3)使用催化剂(1分),A、C(2分)
(4)① c (2分)②低于(1分) 该反应为放热反应,升高温度平衡向逆反应方向移动,CO2体积分数降低,故T2低于T1(2分)
【解析】
试题分析:(1)II×2-I整理可得:CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g)的△H=-394kJ/mol; K1=
CaS(s)+3CO2(g)的△H=-394kJ/mol; K1=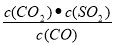 ; K2=
; K2=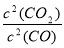 ;K=
;K=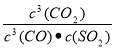 ;所以K=
;所以K=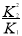 。(2)在反应I中,前100 s 内v(CO)=(2-1.1)mol/L÷100s=0.009mol/(L·s),v(SO2)== v(CO)=0.009mol/(L·s);平衡时CO的转化率为[(2-0.8)÷2]×100%=60%;(3)若只研究反应II,在不同条件下其反应能量变化如图所示,由于降低了反应的活化能,反应热没有变化,所以图中曲线a到曲线b的措施是加入了催化剂;A.由于反应前后气体的质量发生了变化,而气体的物质的量不变,所以若体系中气体的平均摩尔质量不再改变,则气体的质量不再发生变化,反应达到平衡状态,正确;B.因为在方程式是两种气体的方程式的系数相同,所以在任何时刻都存在v(CO)=v(CO2),因此不能作为判断反应达到平衡的标志,错误;C.反应物CO达到平衡时其的转化率达到了最大限度,正确;D.由于容器的容积不变,反应前后气体的体积相等,所以在任何时刻都存在体系内气体压强不再发生变化,故不能作为判断反应达到平衡状态的标志,错误;(4)①根据图像可知a、b、c三点同一温度下不同的n(CO)开始投入量的所处的平衡状态中,由于CO越大,c(CO)就越大,增大反应物的浓度,可以提高其它反应物的转化率,所以这三点中反应物SO2的转化率最高的是c点;②由于反应CaO(s)+3CO(g)+SO2(g)
。(2)在反应I中,前100 s 内v(CO)=(2-1.1)mol/L÷100s=0.009mol/(L·s),v(SO2)== v(CO)=0.009mol/(L·s);平衡时CO的转化率为[(2-0.8)÷2]×100%=60%;(3)若只研究反应II,在不同条件下其反应能量变化如图所示,由于降低了反应的活化能,反应热没有变化,所以图中曲线a到曲线b的措施是加入了催化剂;A.由于反应前后气体的质量发生了变化,而气体的物质的量不变,所以若体系中气体的平均摩尔质量不再改变,则气体的质量不再发生变化,反应达到平衡状态,正确;B.因为在方程式是两种气体的方程式的系数相同,所以在任何时刻都存在v(CO)=v(CO2),因此不能作为判断反应达到平衡的标志,错误;C.反应物CO达到平衡时其的转化率达到了最大限度,正确;D.由于容器的容积不变,反应前后气体的体积相等,所以在任何时刻都存在体系内气体压强不再发生变化,故不能作为判断反应达到平衡状态的标志,错误;(4)①根据图像可知a、b、c三点同一温度下不同的n(CO)开始投入量的所处的平衡状态中,由于CO越大,c(CO)就越大,增大反应物的浓度,可以提高其它反应物的转化率,所以这三点中反应物SO2的转化率最高的是c点;②由于反应CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g)的△H=-394kJ/mol,即该反应是放热反应,升高温度,平衡向逆反应方向移动,CO2体积分数降低,故T2低于T1。
CaS(s)+3CO2(g)的△H=-394kJ/mol,即该反应是放热反应,升高温度,平衡向逆反应方向移动,CO2体积分数降低,故T2低于T1。
考点:考查盖斯定律的应用、化学平衡常数的表达与比较、化学平衡状态的判断、不同反温度的比较化学反应速率和物质平衡转化率的计算的知识。


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源:2015届河南省顶级名校高三入学定位考试化学试卷(解析版) 题型:选择题
几种短周期元素的原子半径及主要化合价如下表:下列叙述正确的是
元素代号 | X | Y | Z | W |
原子半径/pm | 160 | 143 | 70 | 66 |
主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
A.X、Y元素的金属性 X<Y
B.一定条件下, Z单质与W的常见单质直接生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,W单质可以将Z单质从其氢化物中置换出来
查看答案和解析>>
科目:高中化学 来源:2015届河南省偃师市高三上学期第一次月考化学试卷(解析版) 题型:选择题
化学在生产和日常生活中有着重要的应用,下列说法不正确的是
A.氧化镁用作耐火材料
B.Na2O常用于潜水艇或呼吸面具的供氧剂
C.明矾溶于水形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
D.FeCl3溶液可用于刻制印刷铜电路板
查看答案和解析>>
科目:高中化学 来源:2015届河北省邯郸市高三第一次调研考试化学试卷(解析版) 题型:选择题
在无色透明的强酸性溶液中,能大量共存的是( )
A.Na+、NO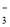 、Al3+、Cl-
、Al3+、Cl-
B.Na+、CO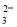 、Ca2+、NO
、Ca2+、NO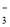
C.K+、SO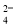 、Cl-、Cu2+
、Cl-、Cu2+
D.Ba2+、Cl-、K+、SO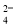
查看答案和解析>>
科目:高中化学 来源:2015届河北省邯郸市高三第一次调研考试化学试卷(解析版) 题型:选择题
下列关于钠的化合物的说法中,正确的是( )
A.Na2CO3和NaHCO3均能与盐酸和NaOH溶液反应
B.Na2CO3固体中含有的NaHCO3可用加热的方法除去
C.Na2O2和Na2O均为白色固体,与CO2反应均放出O2
D.分别向Na2O2和Na2O与水反应后的溶液中立即滴入酚酞溶液,现象相同
查看答案和解析>>
科目:高中化学 来源:2015届河北省唐山市高三年级摸底考试理综化学试卷(解析版) 题型:选择题
在温度和容积不变的密闭容器中,A气体与B气体反应生成C气体。反应过程中,反应物与生成物的浓度随时间变化的曲线如下图,则下列叙述正确的是

A.该反应的化学方程式为A+3B  2C
2C
B.在tl s时,v(A)正=0
C.(t1+l0)s时再充入0.4 molA和0.25 mol B,反应物A的转化率增大
D.若该反应在绝热容器中进行,也在tl时刻达到平衡
查看答案和解析>>
科目:高中化学 来源:2015届河北省“五个一名校联盟”高三教学质量监测(一)化学试卷(解析版) 题型:实验题
(15分)固体硝酸盐加热易分解且产物较复杂。以Mg(NO3)2为研究对象,四个学习小组拟通过实验探究其热分解的产物,分别提出如下4种猜想:
甲组:Mg(NO2)2、NO2、O2 乙组:MgO、NO2、O2
丙组:MgO、NO2、N2 丁组:Mg3N2、O2
(1)实验前,小组成员经讨论认定 组的猜想一定不成立,理由是_____________。
查阅资料得知:2NO2+2NaOH=NaNO3+NaNO2+H2O
针对其他小组猜想,设计如下图所示的实验装置(图中加热、夹持仪器等均省略)进行探究:

A B C D
(2)实验过程
①简述检验该装置气密性的方法 。
②称取硬质试管A的质量为18.0g,试管A与Mg(NO3)2固体共21.8 g置于A中,加热前通入N2以驱尽装置内的空气,其目的是 ;关闭K,用酒精灯加热时,正确操作是先 然后固定在管中固体部位下加热。
③观察到A中有红棕色气体生成,C中有气泡。
④待样品完全分解,A装置冷却至室温、称量,测得硬质试管A和剩余固体的总质量为19.0g。
⑤取少量剩余固体于试管中,加入适量水,未见明显现象。
(3)实验结果分析讨论
①证明一定有O2生成的依据是 ,与此相关的化学原理为(用化学方程式表示) 。
根据实验现象和剩余固体的质量经分析可初步确认猜想_______组结论是正确的。
②一位同学认为上述装置不能确认分解产物中有O2,他的理由你认为可能是 , 如果需改进装置,应该 。
(4)据以上分析,Mg(NO3)2分解的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2015届河北省“五个一名校联盟”高三教学质量监测(一)化学试卷(解析版) 题型:选择题
向溶液X中持续通入过量气体Y,会产生“先浑浊,后澄清”现象的是
A.X:氯化钙溶液 Y:二氧化碳
B.X:硝酸钡溶液 Y:二氧化硫
C.X:氯化铝溶液 Y:氨气
D.X:偏铝酸钠溶液 Y:二氧化氮
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三暑期化学试卷(解析版) 题型:选择题
下列实验方案中,不能达到实验目的的是( )
选项 | 实验目的 | 实验方案 |
A | 检验CH3CH2Br在NaOH溶液中是否发生水解 | 将CH3CH2Br与NaOH溶液共热。冷却后,取出上层水溶液,用稀HNO3酸化,加入AgNO3溶液,观察是否产生淡黄色沉淀 |
B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色 |
D | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com