
【题目】在某无色透明的酸性溶液中,能共存的离子组是( )
A.Na+、K+、SO42﹣、HCO3﹣
B.Cu2+、K+、SO42﹣、NO3﹣
C.Na+、K+、Cl﹣、NO3﹣
D.Fe3+、K+、SO42﹣、Cl ﹣
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.活化分子碰撞即发生化学反应
B.升高温度会加快反应速率,其主要原因是增加了活化分了碰撞的次数
C.有气体参加的化学反应,增大压强可增大活化分子百分数,从而使反应速率增大
D.活化分子间的碰撞不一定是有效碰撞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na、Al、Fe、Cu是中学化学中重要的金属元素。它们的单质及其化合物之间有很多转化关系。下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是( )
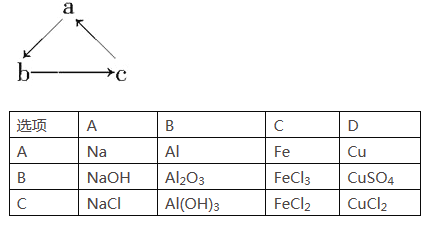
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知强酸与强碱的稀溶液发生中和反应的热化学方程式为 H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,又知电解质的电离是吸热过程。向1 L 0.5 mol·L-1的NaOH溶液中加入下列物质:①稀醋酸;②浓硫酸;③稀硝酸,恰好完全反应。则其焓变ΔH1、ΔH2、ΔH3的关系是( )
A. ΔH1>ΔH2>ΔH3 B. ΔH1<ΔH3<ΔH2
C. ΔH1=ΔH3>ΔH2 D. ΔH1>ΔH3>ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个体积都为2L的恒容密闭容器中发生反应:2CH3OH(g)![]() CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
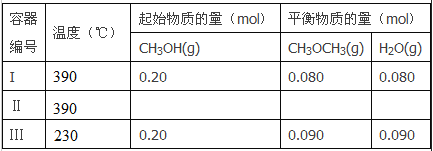
回答下列问题:
(1)反应的△H_________O(填“>”或“<”);判断的理由是_____________。
(2)容器I到达平衡所需的时间为20s,反应速率v(CH3OH)为________mol/(L·s)。390℃时该反应的平衡常数K1=_________(填数值)。
(3)容器II达平衡时,压强是容器I的两倍,CH3OH的体积分数和容器I中的相同,CH3OH起始的物质的量为____________;平衡时CH3OH(g)的体积分数为__________。
(4)390℃,若向3L容器中充入0.9mol CH3OH(g), 0.6mol CH3OCH3(g)和0.3molH2O(g),则起始时该反应速率V正_____________V逆。(填“>”“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组研究铝土矿中Al2O3的含量。已知铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:
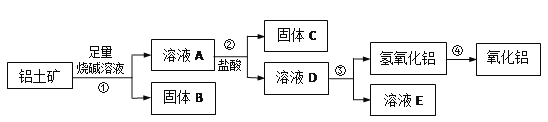
(1)固体B的主要用途有(写出1条即可)_______。
(2)第①步,向铝土矿中加入足量烧碱溶液后,发生反应的离子方程式是_____;_____;第③步中,生成氢氧化铝的离子方程式是______。
(3)将实验过程中所得固体精确称量,课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,则该铝土矿中Al2O3的质量分数是______(保留一位小数)
(4)工业上制取AlCl3用Al2O3与C、Cl2在高温条件下反应,每消耗0.5 mol 碳单质,转移1mol电子,反应的化学方程式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选用如图所示仪器中的两个或几个(内含物质)组装成实验装置,以验证木炭可被浓H2SO4氧化成CO2,下列说法正确的是( )

A. 按气流从左向右流向,连接装置的正确顺序是A→F→E→C→D→B
B. 丁中溶液褪色,乙中溶液变浑浊说明甲中生成CO2
C. 丙中品红溶液褪色,乙中溶液变浑浊说明甲中生成CO2
D. 丁和丙中溶液都褪色,乙中溶液变浑浊,说明甲中有CO2生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com