
在常温下,相同pH的硫酸溶液和硫酸铝溶液中,水电离出的[H+]分别是1.0×10-amol/L和1.0×10-b mol/L,水的电离度分别是a1和a2.下列关系式错误的是
[ ]
科目:高中化学 来源: 题型:
| 弱酸 | CH3COOH | H2SO3 | HCN |
| 物质的量浓度mol/L | 0.01 | 0.01 | 0.01 |
| pH | 3.4 | 2.3 | 5.6 |
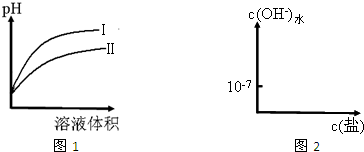
 HSO3-+OH-
HSO3-+OH- HSO3-+OH-
HSO3-+OH-| c(H+) |
| c(CH3COOH) |
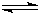 H+(aq)+CN-(aq)△H=+43.5kJ?mol-1
H+(aq)+CN-(aq)△H=+43.5kJ?mol-1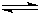 HCN(aq)+OH-(aq)的△H=
HCN(aq)+OH-(aq)的△H=查看答案和解析>>
科目:高中化学 来源:2015届重庆市高二上学期期中考试化学试卷(解析版) 题型:填空题
结合下表回答下列问题(均为常温下的数据):
|
酸 |
电离常数(Ka) |
酸 |
电离常数(Ka) |
|
CH3COOH |
1.8×10-5 |
H2CO3 |
K1=4.4×10-7 K2=4.7×10-11 |
|
HClO |
3×10-8 |
(1)上述三种酸中,酸性最强的是 。
(2)在常温下,相同物质的量浓度的①CH3COONa、 ②Na2CO3、③NaClO三种溶液的pH由小到大的顺序为 。(用序号回答)
(3)设计一个现象明显、操作简便的实验方案证明CH3COOH酸性强于碳酸(不用叙述仪器和具体操作) 。
(4)向Na2CO3溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的钠盐,同时还有另两种钠盐生成,该反应的化学方程式为 。
(5)实验证明:向0.01 mol/L NaAlO2溶液中加入等体积0.01 mol/L NaHCO3溶液,会产生白色胶状沉淀。据此推断CO32-和AlO2-两种离子中,结合质子(H+)能力较强的是 。
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 弱酸 | CH3COOH | H2SO3 | HCN |
| 物质的量浓度mol/L | 0.01 | 0.01 | 0.01 |
| pH | 3.4 | 2.3 | 5.6 |
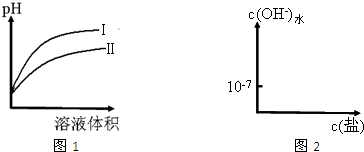
| c(H+) |
| c(CH3COOH) |
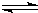
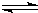
查看答案和解析>>
科目:高中化学 来源:2010-2011学年浙江省镇海中学高三学年模拟卷一化学试卷(理综)(5月份)(解析版) 题型:解答题
| 弱酸 | CH3COOH | H2SO3 | HCN |
| 物质的量浓度mol/L | 0.01 | 0.01 | 0.01 |
| pH | 3.4 | 2.3 | 5.6 |
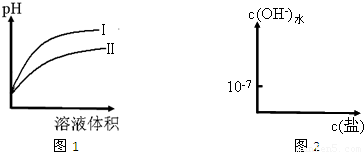
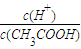 同时增大的是______.
同时增大的是______.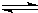 H+(aq)+CN-(aq)△H=+43.5kJ?mol-1
H+(aq)+CN-(aq)△H=+43.5kJ?mol-1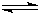 HCN(aq)+OH-(aq)的△H=______.该反应25℃时的平衡常数K=______.
HCN(aq)+OH-(aq)的△H=______.该反应25℃时的平衡常数K=______.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com