
| 阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 | OH-、C1-、CO32-、NO3-、SO42- |
分析 ①A、B两溶液呈碱性,结合离子的共存可知,应为Ba(OH)2、Na2CO3中的一种,C、D、E溶液呈酸性,应为AgNO3、硫酸铝、HCl中的一种;
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生,则A为Na2CO3,B为Ba(OH)2,E为Al2(SO4)3,C为HCl;
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀,则D为AgNO3,然后结合物质的性质及化学用语来解答.
解答 解:①A、B两溶液呈碱性,结合离子的共存可知,应为Ba(OH)2、Na2CO3中的一种,C、D、E溶液呈酸性,应为AgNO3、硫酸铝、HCl中的一种;
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生,则A为Na2CO3,B为Ba(OH)2,E为Al2(SO4)3,C为HCl;
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀,则D为AgNO3,
(1)上述分析可知B为Ba(OH)2,C为HCl,
故答案为:Ba(OH)2; HCl;
(2)A溶液与E溶液反应的化学方程式为3Na2CO3+Al2(SO4)3+3H2O=2Al(OH)3↓+3CO2↑+3Na2SO4,
故答案为:3Na2CO3+Al2(SO4)3+3H2O=2Al(OH)3↓+3CO2↑+3Na2SO4;
(3)E溶液与过量的B溶液反应的离子方程式为2A13++3SO42-+3Ba2++8OH-=2A1O2-+3BaSO4↓+4H2O,
故答案为:2A13++3SO42-+3Ba2++8OH-=2A1O2-+3BaSO4↓+4H2O;
(4)B与C的稀溶液反应的热化学方程式为OH-(aq)+H+(aq)=H2O(1)△H=-a kJ/mol或1/2Ba(OH)2(aq)+HC1(aq)=1/2BaC12(aq)+H2O(1)△H=-a kJ/mol
或Ba(OH)2(aq)+2HC1(aq)=BaC12(aq)+2H2O(1)△H=-2a kJ/mol,
故答案为:OH-(aq)+H+(aq)=H2O(1)△H=-a kJ/mol或1/2Ba(OH)2(aq)+HC1(aq)=1/2BaC12(aq)+H2O(1)△H=-a kJ/mol
或Ba(OH)2(aq)+2HC1(aq)=BaC12(aq)+2H2O(1)△H=-2a kJ/mol.
点评 本题考查离子的共存及物质的推断,明确信息中物质之间的反应为解答的关键,熟悉离子之间的反应即可解答,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
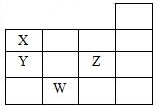 如图表示元素周期表的一部分,关于元素X、Y、Z、W的叙述正确的是( )
如图表示元素周期表的一部分,关于元素X、Y、Z、W的叙述正确的是( )| A. | 只有③ | B. | 只有①③ | C. | 只有①②③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH、KOH、CsOH碱性依次增强 | |
| B. | Li、Na、K、Rb、Cs的失电子能力逐渐增强 | |
| C. | Al3+、Mg2+、Na+的离子半径依次减小 | |
| D. | O22-和S2-具有相同的质子数和电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7 | B. | 10 | C. | 4.3 | D. | 11.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
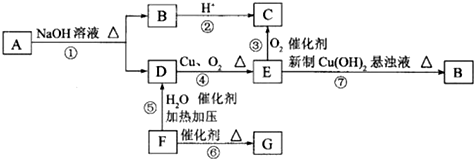
 ,
, .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| B. | 氧的原子结构示意图: | |
| C. | NaCl的电子式: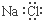 | |
| D. | 质量数为37的氯原子:${\;}_{34}^{17}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30% | B. | 20% | C. | 40% | D. | 35% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com