
【题目】已知反应X+Y=M+N为放热反应,对该反应的下列说法中正确的( )
A.X的能量一定高于M
B.Y的能量一定高于N
C.因该反应为放热反应,故不必加热就可发生
D.X和Y的总能量一定高于M和N的总能量
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(题文)F是重要的有机化合物,可以由基础化合物A通过以下过程制得:

已知:① ;②核磁共振氢谱显示C的分子中含有4种不同化学环境的氢原子;③F的分子式为C16H22O4,分子中苯环上的一溴代物只有两种。
;②核磁共振氢谱显示C的分子中含有4种不同化学环境的氢原子;③F的分子式为C16H22O4,分子中苯环上的一溴代物只有两种。
(1)A发生加聚反应的化学方程式是____________________________________________。
(2)B物质的名称为________________________;检验B中官能团的实验操作方法_________________。
(3)F中的官能团的名称为__________;C+E→F的化学方程式是_____________________。
(4)X与E互为同分异构体,且X具有下列性质,符合条件的X有___种(不考虑立体异构)。
①分子中含有苯环,且能与NaHCO3溶液反应生成二氧化碳气体②与银氨溶液共热有银镜生成。
(5)设计由乙烯和必要的无机原料合成丙酸乙酯的合成路线___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己烯雌酚是一种激素类药物,结构如下.下列有关叙述中不正确的是( )

A. 它易溶于有机溶剂
B. 可与NaOH和NaHCO3发生反应
C. 1mol该有机物可以与5molBr2发生反应
D. 该有机物分子中,可能有16个碳原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知还原性I->Fe2+>I2,在水溶液中I2可被Cl2氧化为IO![]() 。向含溶质a mol的FeI2溶液中通入b mol Cl2,充分反应(不考虑单质与水的反应)。下列说法不正确的是( )
。向含溶质a mol的FeI2溶液中通入b mol Cl2,充分反应(不考虑单质与水的反应)。下列说法不正确的是( )
A. 当a=2b时,反应后的离子浓度之比c(Fe2+)∶c(I-)∶c(Cl-)=1∶1∶1
B. 当3a=2b时,发生的离子反应:2Fe2++4I-+3Cl2===2Fe3++2I2+6Cl-
C. 当13a=2b时,发生的离子反应为2Fe2++4I-+13Cl2+12H2O===4IO![]() +26Cl-+2Fe3++24H+
+26Cl-+2Fe3++24H+
D. 若反应后溶液中I2与IO![]() 的物质的量之比为1∶1,则反应中转移电子3.5b mol
的物质的量之比为1∶1,则反应中转移电子3.5b mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最早使用的化学电源是锌锰电池,即大家所熟悉的干电池(dry cell),其结构如下图所示:尽管这种电池的历史悠久,但对它的电化学过程尚未完全了解。一般认为,放电时,电池中的反应如下:

E极:2MnO2+2H2O+2e-="==" 2MnO(OH)+2OH-
F极:Zn+2NH4Cl -2e-=== Zn(NH3)2Cl2+2H+
总反应式:2MnO2+Zn+2NH4Cl ="==" 2MnO(OH)+Zn(NH3)2Cl2
下列说法正确的是
A. E极是电池的正极,发生的是氧化反应
B. F极是电池的负极,发生的是氧化反应
C. 从结构上分析,锌锰电池应属于可充电电池
D. 锌锰电池内部发生的氧化还原反应是可逆的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有6种短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
W | 周期表中原子半径最小的元素 |
U | 地壳中含量最多的金属元素 |
R | 单质为空气的主要成分 |
T | M层上有6个电子 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
完成下列空白(涉及W、U、R、T、X、Y、Z时,用元素符号表示):
(1)元素T的原子共有__个电子;元素X的一种核素可测定文物年代,这种核素的符号是___。
(2)用电子式表示:
①气态化合物XR2_______;
②元素W、R形成的10电子分子的形成过程_____________。
(3)用离子方程式表示:
①元素Y与元素W形成的离子YW4+与NaOH溶液共热的反应_____;
②元素U的单质与NaOH溶液反应_______。
(4)元素Z与元素T相比,非金属性较强的是___,下列表述中能证明这一事实的是___(填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(5)探寻物质的性质差异性是学习的重要方法之一。在T、X、Y、Z四种元素的最高价氧化物的水化物中,化学性质明显不同于其他三种的是____(用分子式表示),理由是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究实验室制氯气过程中反应物与生成氯气之间量的关系,设计了如下图所示的装置。

(1)装置A的名称是_____________________。
(2)该实验装置检查气密性的方法是________________________________。
(3)如果将过量二氧化锰与20mL 12mol/L的盐酸混合加热,充分反应后收集到的氯气少于0.06mol,其可能原因有__________
a.加热使浓盐酸挥发出大量HCl b.盐酸变稀后不发生该反应
c.烧瓶中残留有氯气 d.装置B中液面高于A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,工业大规模生产前,实验室先按如下流程进行模拟制备少量Mg(ClO3)2·6H2O:
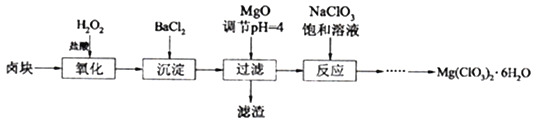
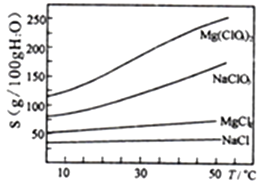
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。②几种化合物的溶解度(S)随温度(T)变化曲线如右图。
(1)卤块中加H2O2的目的是________________,写出该反应的离子方程式__________________。
(2)加入BaCl2的目的是除去SO42-,如何检验SO42-已沉淀完全?_________________。
(3)常温下,加MgO调节pH=4后溶液中c(Fe3+)=___________(已知Ksp[Fe(OH)3=4×10-38],过滤所得滤渣的主要成分有______________。
(4)加入NaClO3饱和溶液公有NaCl晶体析出,写出该反应的化学方程式:___________,请利用该反应,结合上图,制取Mg(ClO3)2·6H2O的实验步骤依次为:
①取样,加入NaClO3饱和溶液充分反应;②蒸发结晶;③___________;④冷却结晶;⑤过滤、洗涤,获得Mg(ClO3)2·6H2O晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯水中存在多种分子和离子,它们在不同的反应中表现出不同的性质。下列结论正确的是( )
A. 加入有色布条,片刻后有色布条褪色,说明有Cl2存在
B. 溶液呈浅黄绿色,且有刺激性气味,说明有Cl2存在
C. 先加入盐酸酸化,再加入AgNO3溶液,生成白色沉淀,说明有Cl-存在
D. 加入NaOH溶液,氯水的浅黄绿色消失,说明有HClO存在
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com