
【题目】下列有关1mol H2的说法中,不正确的是(NA表示阿伏加德罗常数)( )
A.质量为2g
B.含氢原子数为NA
C.含氢分子数为NA
D.在标准状况下,体积约为22.4L
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】
(1)在仪器a 分液漏斗 b 试剂瓶 c 集气瓶 d 滴定管 e 容量瓶f 量筒 g 托盘天平中,标有“0”刻度的是________(填序号,有2个选项)。
(2)“磨砂”是增加玻璃仪器密封性的一种处理工艺,在下列仪器中,没有用到“磨砂”工艺处理的有________(填序号,有2个选项)。
a.试管
b.分液漏斗
c.带滴管的试剂瓶(滴瓶)
d.碱式滴定管
e.酸式滴定管
(3)用装置甲、乙、丙和乳胶管组成一套装置(气密性已检查),可用于制取并收集NH3或HCl气体,可供选择的液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液。试回答下列问题:
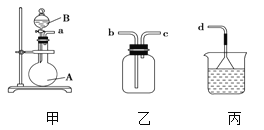
① 若制取某气体的过程中,丙中的石蕊溶液变红,且烧瓶中的试剂A与分液漏斗中的试剂B均为无色液体,则试剂A为________,制取该气体利用了B的性质有________、_____ 。
通过丙中紫色石蕊溶液变红或变蓝,说明乙中气体已集满。若石蕊溶液变蓝,则烧瓶甲中应加入的固体试剂A为________。
②若在乙中收集氨气,气体流经装置的顺序是:a→____→_____→d(填接口代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用某矿渣(含有Cu2O、Al2O3,Fe2O3、SiO2)制取铜的操作流程如下:
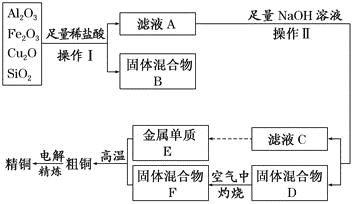
已知:Cu2O+2H+= Cu+Cu2++H2O
(1)实验操作Ⅰ的名称为 ;在空气中灼烧固体混合物D时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有 (填仪器名称)。
(2)滤液A中铁元素的存在形式为 (填离子符号),生成该离子的离子方程式为 ,检验滤液A中存在该离子的试剂为 (填试剂名称)。
(3)金属E与固体F发生的某一反应可用于焊接钢轨,该反应的化学方程式为 。
(4)常温下,等pH的NaAlO2和NaOH两份溶液中,由水电离出的c(OH-)前者为后者的108倍,则两种溶液的pH= 。
(5)利用电解法进行粗铜精炼时,下列叙述正确的是 (填代号)。
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.精铜作阴极,电解后电解液中Cu2+浓度减小
d.粗铜精炼时通过的电量与阴极析出铜的量无确定关系
(6)从浓硫酸、浓硝酸、蒸馏水中选用合适的试剂,测定粗铜样品中金属铜的质量分数,涉及的主要步骤为:称取一定质量的样品→ →过滤、洗涤、干燥→称量剩余固体铜的质量。(填缺少的操作步骤,说出主要操作方法,不必描述操作过程的细节)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】径A>B>C;②D、E是非金属元素且为相邻周期元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;④G是除氢外原子半径最小的元素。
(1)B位于周期表中第______周期_____族,C的原子结构示意图是 。
(2)E的单质颜色是____________________。
(3)A元素与D元素形成化合物的电子式是__________________。
(4)G的单质与水反应的化学方程式是 。
(5)F的元素符号是_____________________。
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的化学式是_________,酸性最强的化学式是_______________,气态氢化物最稳定的化学式是______________。
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是:__________________________________________ _。
查看答案和解析>>
科目:高中化学 来源: 题型:
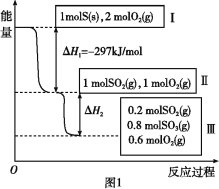
【题目】恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示。
已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ/mol。
2SO3(g) ΔH=-196.6 kJ/mol。
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式: 。
(2)状态II到状态III放出的热量为 。
(3)恒温恒容时,1 mol SO2和2 mol O2充分反应,放出热量的数值比∣ΔH2∣ (填“大”、“小”或“相等”)。
(4)将Ⅲ中的混合气体通入足量的NaOH溶液中消耗NaOH的物质的量为 ,若溶液中发生了氧化还原反应,则该过程的离子方程式为: 。
(5)恒容条件下,下列措施中能使n(SO3)/ n(SO2)增大的有 。
A.升高温度
B.充入He气
C.再充入1 mol SO2(g)和1 mol O2(g)
D.使用催化剂
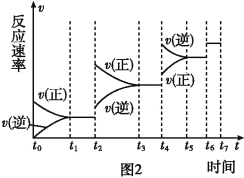
(6)某SO2(g)和O2 (g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是 ;图中表示平衡混合物中SO3的含量最高的一段时间是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【物质结构与性质】A、B、C、D、E、F为原子序数依次增大的前四周期六种元素,A2-和B+具有相同的电子层结构;C、E为同周期元素,C核外电子总数是最外层电子数的3倍;E元素最外层有一个未成对电子;F的最外层只有1个电子,但次外层有18个电子。
请回答下列问题:
(1)基态F原子的核外电子排布式为 ,F2+能与足量氨水反应得到深蓝色透明溶液,该深蓝色离子的结构式为 。
(2)六种元素中电负性最小的是 ,其中C、D、E的第一电离能由大到小顺序为 (填元素符号)。
(3)A、B 的氢化物所属的晶体类型分别为 。
(4)指出A、D的简单氢化物中沸点较高的物质并说明原因 。
(5)C和E的单质反应可生成组成比为1︰3的化合物,该化合物的立体构型名称为 ,中心原子的杂化轨道类型为 。
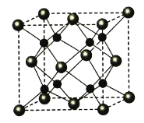
(6)A和B能够形成化合物Y,其晶胞结构如图所示,晶胞参数为a nm,Y的化学式为 ,列式计算晶体Y的密度(可不化简) g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】充分燃烧2.8g某有机物A,生成8.8g CO2和3.6g H2O,这种有机物蒸气的相对密度是 相同条件下N2的2倍.
(1)求该有机物的分子式 .
(2)该有机物链状同分异构体的结构简式为: 、 、 .
(3)若有机物A在核磁共振氢谱中只有一个信号峰(即只有一种氢原子),则用键线式表示的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,能在溶液中大量共存的是( )
A.Ca2+、Mg2+、Cl-、NO3- B.Al3+、K+、SO42-、OH-
C.Fe2+、H+、SO42-、NO3- D.Na+、OH-、HCO3-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com