
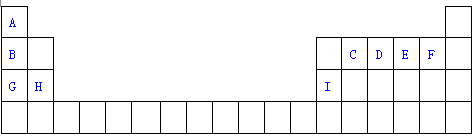
分析 由元素在周期表中的位置可知,A为H,R为He,B为Li,C为C,D为N,E为O,F为F,G为Na,H为Mg,I为Al,
(1)Mg与二氧化碳反应生成MgO和C;
(2)D的气态氢化物为氨气;
(3)金属活泼性越强,第一电离能越小,但Mg的最外层s电子全满,为稳定结构,则第一电离能最大;
(4)由A、C、D形成的ACD分子为H-C≡N,单键为σ键,三键中有1个σ键、2个π键.
解答 解:由元素在周期表中的位置可知,A为H,R为He,B为Li,C为C,D为N,E为O,F为F,G为Na,H为Mg,I为Al,
(1)Mg与二氧化碳反应生成MgO和C,该反应为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
(2)D的气态氢化物为氨气,有1对孤对电子和3个σ键,VSEPR模型为四面体,空间构型为三角锥型,N原子采取sp3杂化,故答案为:四面体;sp3杂化;
(3)金属活泼性越强,第一电离能越小,但Mg的最外层s电子全满,为稳定结构,则第一电离能最大,所以第一电离能为Mg>Al>Na,故答案为:Mg>Al>Na;
(4)由A、C、D形成的ACD分子为H-C≡N,单键为σ键,三键中有1个σ键、2个π键,则分子中共有2个σ键、2个π键,故答案为:2;2.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、性质、分子构型及杂化、第一电离能为解答的关键,侧重分析与应用能力的考查,注意原子结构与性质的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
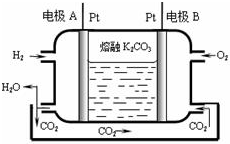
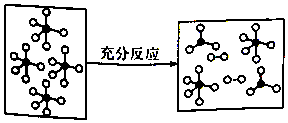 一定条件下,某容器中各微粒在反应前后变化示意图如图,其中“o”和“•”代表不同元素的原子.下列关于此反应的说法不正确的是( )
一定条件下,某容器中各微粒在反应前后变化示意图如图,其中“o”和“•”代表不同元素的原子.下列关于此反应的说法不正确的是( )| A. | 该反应可表示为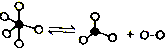 | |
| B. | 可能是PCl5的分解反应 | |
| C. | 反应过程中,一定伴随共价键的断裂与形成 | |
| D. | 该反应的△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
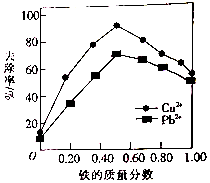 铁炭混合物(铁屑和活性炭的混合物)、纳米铁粉均可用于处理水中污染物.在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如图所示.已知活性炭对重金属离子具有一定的吸附作用.
铁炭混合物(铁屑和活性炭的混合物)、纳米铁粉均可用于处理水中污染物.在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如图所示.已知活性炭对重金属离子具有一定的吸附作用.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 碳及其化合物应用广泛.
碳及其化合物应用广泛.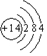 (2)向1L恒容密闭容器中注人CO和H2O(g),830℃时测得部分数据如表.
(2)向1L恒容密闭容器中注人CO和H2O(g),830℃时测得部分数据如表.| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n(CO)/mol | 0.200 | 0.160 | 0.125 | 0.099 | 0.080 | 0.080 |
| n(H2O)/mol | 0.300 | 0.260 | 0.225 | 0.199 | 0.180 | 0.180 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图是研究二氧化硫性质的微型实验装置.现用60%硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不易污染空气.下列说法中错误的是( )
如图是研究二氧化硫性质的微型实验装置.现用60%硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不易污染空气.下列说法中错误的是( )| A. | 紫色石蕊溶液变红色,说明SO2呈酸性 | |
| B. | 品红溶液褪色,说明SO2具有漂白性 | |
| C. | 溴水橙色褪去,体现了SO2的还原性 | |
| D. | 含酚酞的NaOH溶液红色变浅,表明SO2能够和NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | Fe3+具有氧化性 | 用KSCN溶液可以鉴别Fe3+ |
| B | 浓硫酸具有脱水性和强氧化性 | 浓硫酸滴到湿润的蔗糖中,蔗糖变成黑色海绵状 |
| C | SiO2有导电性 | SiO2可用于制备光导纤维 |
| D | 铝制品在空气中耐腐蚀 | 铝是不活泼金属 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
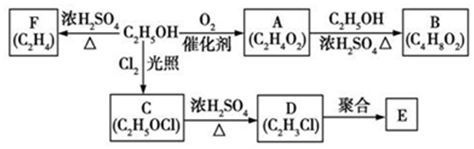
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能通过加氢反应得到③的烯烃有四种 | |
| B. | ①和②互为同分异构体,①和④互为同系物 | |
| C. | ②可以由烯烃与氢气加成而获得 | |
| D. | ④的一氯代物有四种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com