
����Ŀ����֪A��B��C��D��E����Ԫ�ص�ԭ���������ε�����A��B��C��Dλ��ǰ�����ڣ�Aλ�����ڱ���s������ԭ���е��Ӳ�����δ�ɶԵ�������ͬ��B�Ļ�̬ԭ���е���ռ������������ͬ��ԭ�ӹ������ÿ�ֹ���еĵ���������ͬ��Dԭ�ӵĺ���ɶԵ�������δ�ɶԵ�������3����A��B��D����Ԫ����ɵ�һ�ֻ�����M����װ�����г����е�һ���к����壬A��B����Ԫ����ɵ�ԭ�Ӹ�����Ϊ1��1�Ļ�����N�dz������л��ܼ���E�С����������֮�ƣ�E4+���ԭ�ӵĺ�������Ų���ͬ��
��ش��������⣺������ʱ��A��B��C��D��E������Ӧ��Ԫ�ط��ű�ʾ��
��1��E�Ļ�̬ԭ�ӵ���Χ�����Ų�ʽΪ ��
��2����A��B��C�γɵ�ABC�����У��������Ҽ������м���
��3������������ȷ���� �� ������ĸ��
a��M������ˮ������ΪM��ˮ���Ӽ����γ��������M�Ǽ��Է��ӣ�N������ˮ������ΪN�ǷǼ��Է���
b��M�Ͷ�����̼�����е�����ԭ�Ӿ�����sp2�ӻ�
c��N�����к���6���Ҽ���1���м�
d��BD2������۵㡢�е㶼�ȶ������辧��ĵ�
��4��E��һ��������Q���侧���ṹ����ͼ��ʾ����Q�Ļ�ѧʽΪ �� �þ�������ԭ�ӵ���λ��Ϊ �� 
��5��B��C��D����Ԫ�صĵ�һ��������С�����˳��Ϊ ��
��6����Ũ��ECl3��������Һ�м������ѣ���ͨ��HCl�����ͣ��ɵõ���λ��Ϊ6�����ΪECl36H2O����ɫ���壬�þ�����������������ʵ���֮��Ϊ1��5����������ӵĻ�ѧʽΪ ��
���𰸡�
��1��3d24s2
��2��2��2
��3��d
��4��TiO2��3
��5��N��O��C
��6��[TiCl��H2O��5]2+
���������⣺A��B��C��D��E����Ԫ�ص�ԭ���������ε�����A��B��C��Dλ��ǰ�����ڣ�Aλ�����ڱ���s������ԭ���е��Ӳ�����δ�ɶԵ�������ͬ����A��HԪ�أ�
B�Ļ�̬ԭ���е���ռ������������ͬ��ԭ�ӹ������ÿ�ֹ���еĵ���������ͬ����B��CԪ�أ�
Dԭ�ӵĺ���ɶԵ�������δ�ɶԵ�������3����A��B��D����Ԫ����ɵ�һ�ֻ�����M����װ�����г����е�һ���к����壬M�Ǽ�ȩ����D��OԪ�أ�
CԪ��ԭ������С��D������B��ΪNԪ�أ�
A��B����Ԫ����ɵ�ԭ�Ӹ�����Ϊ1��1�Ļ�����N�dz������л��ܼ���Ϊ����
E�С����������֮�ƣ�E4+���ԭ�ӵĺ�������Ų���ͬ��Eԭ�Ӻ��������=18+4=22��ΪTiԪ�أ���1��E��TiԪ�أ���ԭ�Ӻ�����22�����ӣ�����Χ����Ϊ3d��4s���ӣ�3d��4s�ܼ��Ϸֱ���2�����ӣ����̬ԭ����Χ�����Ų�ʽΪ3d24s2 �� ���Դ��ǣ�3d24s2����2����A��B��C�γɵ�HCN�����У���ṹʽΪH��C��N�����۵���Ϊ�Ҽ������������к���һ���Ҽ��������м����÷����к���2���Ҽ���2���м������Դ��ǣ�2��2����3��a��M�Ǽ�ȩ����ȩ������ˮ��N�DZ�������������ˮ����ȩ�ͱ����ǷǼ��Է��ӣ�����ȩ�ܺ�ˮ�γ����������ˮ�����γ���������Լ�ȩ������ˮ������������ˮ���ʴ���
b��M������Cԭ�Ӽ۲���ӶԸ�����3�Ҳ����µ��Ӷԣ�������̼������Cԭ�Ӽ۲���ӶԸ�����2�Ҳ����µ��Ӷԣ����Լ�ȩ��Cԭ�Ӳ���sp2�ӻ���������̼������Cԭ�Ӳ���sp�ӻ����ʴ���
c���������к���12���Ҽ����ʴ���
d�����Ӿ����۷е�С��ԭ�Ӿ��壬������̼�Ƿ��Ӿ��塢����������ԭ�Ӿ��壬�������̼�۷е�С�ڶ������裬����ȷ��
��ѡd����4���þ�����Tiԭ�Ӹ���=1+8�� ![]() =2��Oԭ�Ӹ���=2+4��
=2��Oԭ�Ӹ���=2+4�� ![]() =4�������仯ѧʽΪTiO2��ÿ��Oԭ������3��Tiԭ�ӣ���ԭ����λ����3��
=4�������仯ѧʽΪTiO2��ÿ��Oԭ������3��Tiԭ�ӣ���ԭ����λ����3��
���Դ��ǣ�TiO2��3����5��B��C��D�ֱ���C��N��OԪ�أ�ͬһ����Ԫ��Ԫ�ص�һ����������ԭ��������������������Ƶ���IIA�塢��VA��Ԫ�ص�һ�����ܴ���������Ԫ�أ����Ե�һ�����ܴ�С˳����N��O��C��
���Դ��ǣ�N��O��C����6����λ��Ϊ6�����ΪTiCl36H2O����ɫ���壬�þ�����������������ʵ���֮��Ϊ1��5����������ֻ����3��Cl�� �� ����������Ŀ�����H2O��H2O��Cl����ֵΪ5��1�����Ը������ӵĻ�ѧʽΪ[TiCl��H2O��5]2+ ��
���Դ��ǣ�[TiCl��H2O��5]2+ ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ��������C5H12�ѽ⣬�����Եõ�ϩ���������ǣ�������
A.3��B.4��C.5��D.6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����5.04gNa2CO3��NaOH�Ĺ��������ˮ�ܽ⣬�����Һ����μ���2molL��1�����ᣬ�����������������CO2���������״������ϵ��ͼ��ʾ������˵���в���ȷ���ǣ� �� 
A.OA�η�����Ӧ�����ӷ���ʽΪ��H++OH���TH2O? CO ![]() +H+�THCO3��
+H+�THCO3��
B.B����Һ�е�����ΪNaCl��������Ϊ5.85g
C.������35mL����ʱ������CO2�����Ϊ224mL����״����
D.�������NaOH������2.40g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪X��M������ѧ�̲��еij���Ԫ�أ����ף� XO3n��+Xn��+H+��X�����ʣ�+H2O��δ��ƽ���� ���ң�Mm++mOH��=M��OH��m�������ж��������ӷ�Ӧͨʽ���ƶ��У���ȷ���ǣ� �� ����n=1����XO3n����XԪ��Ϊ+5�ۣ�Xλ�����ڱ��ڢ�A��
����n=2����X����������ˮ��������������⻯�ﷴӦ
����m=1����M��NO3��m��Һ�Ͱ�ˮ����ʱ��������ܲ�ͬ
����m=2�����ڿ��������ɡ�����MSO4��Һһ���ܵõ�MSO4
����m=3����MCl3����������������Һ��Ӧһ������M��OH��m ��
A.�٢ۢ�
B.�ڢ�
C.�٢ڢ�
D.�ܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ҵ���������ײ�����ҵ�����ϡ���'���Ϊ����̽�������ǻ�ѧ����Ҫ��ɵģ�ij�����Ĺ��˷����к���ͭ�������������������Ʊ�CuSO45H2O��Fe SO47H2O��AlCl3������ͼ�� 
��1����AlCl3��Һ���ɲ����գ��õ��IJ����� ��
��2��д��A��C�Ļ�ѧ����ʽ�� ��
��3��������ҺD�еĽ��������ӵķ�����
��4��д��E��CuSO4�Ļ�ѧ����ʽ�� ��
��5��д���������ռӦ�����ӷ���ʽ�� ��
��6��ȡ������ҺD�������м���˫��ˮ������Ϊ�� ��
��7����CuSO4��Һ����ͭ�ľ���Һ�������Ϸ����ĵ缫��ӦʽΪ�� ��
��8���ƺ������ǻ��ý�����д�����������ƵĻ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Ȼ�л���A���ˮ��������ø������ˮ������B��1molBˮ�������2molC��D����Һ�dz��õ�����֮һ��E�ĺ˴Ź�������Ϊ3��1��1��1����F�е���Ԫ��ȥ���ɵõ�һ��̼��ά���ϣ�����֮���ת����ϵ��ͼ��ʾ����ش�����������⣺ 
��1��B�����ƣ� ��
��2��E�еĹ����ţ� ��
��3��H��I�Ļ�ѧ����ʽ�� �� ��Ӧ���ͣ� ��
��4��I��K���ɸ߷��ӻ�����Ļ�ѧ����ʽ�� ��
��5��J������Cu��OH��2����Һ��Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������һ����ȷ����
A���κ�Ũ����Һ������Զ�����pH��ֽ�ⶨ
B��ij�¶��£�pH=6.2�Ĵ�ˮ������
C��25��ʱ��pH=1�Ĵ�����Һ��c(H+)��pH=2��������Һ��c(H+)��10��
D��25��ʱ��pH=12��NaOH��Һ�е�n(OH��)=10-2mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��300����ǰ��������ѧ�Ҳ����������������ûʳ�������ɫ��Ӧ�����ɴ˷���������īˮ��ûʳ����Ľṹʽ��ͼ��ʾ��
��1����ûʳ��������īˮ��Ҫ���������������ʣ�����ţ���
A.��
B.��
C.��֬
D.����
��2��ûʳ�������������п��������ã���Ŀǰ�㷺Ӧ�õ�ʳƷ���Ӽ�����ṹ��ʽΪ
��3���Ჴ�����Ƕ��ǻ��������봼�γɵ��������ǹ�������ʹ�õ�ʳƷ���Ӽ����Ჴ�����ķ���ʽΪ �� �䱽��ֻ�멁OH�ͩ�COOR����ȡ����ֱ������������ȡ����λ�ڱ�����λ��ͬ���칹�����֣�
��4��д���Ჴ������������������Һ���ȷ�Ӧ�Ļ�ѧ����ʽ�� �� 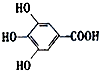
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����NaCl��Һ��װ����ͼ��ʾ������˵������ȷ���ǣ� �� 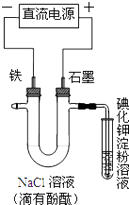
A.���缫�ϵĵ缫��ӦʽΪFe��2e��=Fe2+
B.��Һ��Na+�����缫�����ƶ�
C.ͨ��һ��ʱ��ɿ������缫������Һ���
D.ͨ��һ��ʱ��ɿ����Թ�����Һ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com