
【题目】铅蓄电池反应为:Pb(s)+PbO2(s)+2H2SO4(aq)![]() 2PbSO4(s)+2H2O(l)。下列说法正确的是( )
2PbSO4(s)+2H2O(l)。下列说法正确的是( )
A.放电时Pb为正极,发生还原反应
B.放电时电解质溶液中的H+向负极移动
C.充电时阳极的电极反应为:PbSO4(s)-2e-=Pb(s)+SO![]() (aq)
(aq)
D.充电时阳极附近电解质溶液的pH逐渐减小
【答案】D
【解析】
由总方程式可知,为原电池时,Pb为负极,发生氧化反应,电极方程式为Pb+SO42--2e-=PbSO4,PbO2为正极,发生还原反应,电极方程式为PbO2+4H++SO42-+2e-=2H2O+PbSO4,在充电时,阴极发生的反应是PbSO4+2e-=Pb+SO42-,阳极反应为PbSO4-2e-+2H2O=PbO2+SO42-+4H+,放电时,阴离子向负极移动,阳离子向正极移动,以此解答该题。
A.放电时,该原电池的负极材料是铅,铅失电子发生氧化反应,故A错误;
B.放电时,蓄电池内电路中H+向正极移动,故B错误;
C.充电时阳极发生氧化反应,阳极反应为PbSO4-2e-+2H2O=PbO2+SO42-+4H+,故C错误;
D.阳极反应为PbSO4-2e-+2H2O=PbO2+SO42-+4H+,由电极方程式可知阳极附近电解质溶液的pH逐渐减小,故D正确;
故答案为D。


科目:高中化学 来源: 题型:
【题目】常温下,用0.10molL-1NaOH溶液分别滴定20.00mL0.10molL-1的HX和HY溶液,滴定曲线如图所示。下列说法正确的是( )

A.pH=7时,滴定HX消耗NaOH溶液体积等于20.00mL
B.将上述HX、HY溶液各加水稀释10倍,稀释后溶液的pH:pH(HY)>pH(HX)
C.当NaOH溶液体积为20.00mL时,HX溶液中离子浓度:c(Na+)>c(X-)>c(H+)>c(OH-)
D.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时,c(H+)+c(HX)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 氢氧化钡溶液与稀H2SO4反应:Ba2++SO42-= BaSO4↓
B. 碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑
C. SiO2和氢氧化钠溶液的反应:SiO2+2OH-=SiO32-+H2O
D. 用FeCl3溶液腐蚀铜箔制造印刷电路板:Fe3++Cu=Fe2++Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2 是一种高效安全的杀菌消毒剂。用氯化钠电解法生成ClO2的工艺原理示意图如下图, 发生器内电解生成ClO2。下列说法正确的是

A. a气体是氯气,b气体是氢气
B. 氯化钠电解槽内每生成2 mol a气体,转移2mol e-
C. ClO2发生器中阴极的电极反应式为:ClO3- + 2H+ + e-![]() ClO2↑ + H2O
ClO2↑ + H2O
D. 为使a、b气体恰好完全反应,理论上每生产1molClO2需要补充44.8Lb气体(标况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨在化肥生产、贮氢及燃煤烟气脱硫脱硝等领域用途非常广泛.
![]() 尿素
尿素![]() 与氰酸铵
与氰酸铵![]() 互为 ______ ;氰酸铵属于 ______ 化合物
互为 ______ ;氰酸铵属于 ______ 化合物![]() 选填:“离子”或“共价”
选填:“离子”或“共价”![]() 。
。
![]() 液氨是一种贮氢材料,气态氨转变为液氨将 ______ 能量
液氨是一种贮氢材料,气态氨转变为液氨将 ______ 能量![]() 选填:“吸收”或“释放”
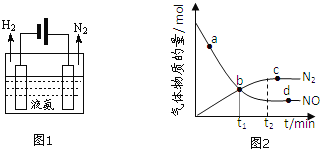
选填:“吸收”或“释放”![]() 液氨可通过图1装置释放氢气,该过程中能量转化方式为 ______ 。
液氨可通过图1装置释放氢气,该过程中能量转化方式为 ______ 。
![]() 氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和
氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和![]() ,在一定条件下发生反应:
,在一定条件下发生反应:![]() 。
。
①能说明该反应已达到平衡状态的标志是 ______ ![]() 不定项选择
不定项选择![]() 。
。
![]() 反应速率
反应速率![]()
![]()
![]()
![]() 容器内压强不再随时间而发生变化
容器内压强不再随时间而发生变化
![]() 容器内
容器内![]() 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化
![]() 容器内
容器内![]() :
:![]() :
:![]() :
:![]() :4:5:6
:4:5:6
②某次实验中测得容器内NO及![]() 的物质的量随时间变化如图2所示,图中
的物质的量随时间变化如图2所示,图中![]() 正
正![]() 与
与![]() 逆
逆![]() 相等的点为 ______
相等的点为 ______ ![]() 选填字母
选填字母![]() 。
。
![]() 已知:断开1mol共价键吸收的能量或形成1mol共价键释放的能量数据如表
已知:断开1mol共价键吸收的能量或形成1mol共价键释放的能量数据如表
共价键 |
|
|
|
能量变化 | 436 |
| 946 |
则合成氨反应:![]()
![]() ______
______ ![]()
![]() 工业上用氨水吸收硫酸工业尾气中的
工业上用氨水吸收硫酸工业尾气中的![]() ,既可消除污染又可获得
,既可消除污染又可获得![]() 等产品.若用1000kg 含
等产品.若用1000kg 含![]() 质量分数为
质量分数为![]() 的氨水吸收
的氨水吸收![]() 且全部转化为
且全部转化为![]() ,不考虑其它成本,则可获得的利润为 ______ 元
,不考虑其它成本,则可获得的利润为 ______ 元![]() 参照下面的价格表
参照下面的价格表![]() 。
。
| 无水 | |
价格 |
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,可逆反应![]() 达到平衡的标志是
达到平衡的标志是
A. ![]() 生成的速率和
生成的速率和![]() 分解的速率相等
分解的速率相等
B. ![]() 、
、![]() 、
、![]() 的浓度相等
的浓度相等
C. 单位时间内生成![]() ,同时生成
,同时生成![]()
D. ![]() 、
、![]() 、
、![]() 的分子数之比为1:3:2
的分子数之比为1:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数逐渐增大,四种元素形成的化合物结构如图所示。且W与X、Y、Z均可形成电子数相等的分子,W2Z常温常压下为液体。下列说法正确的是( )

A.YW3的水溶液呈酸性
B.W2Z的稳定性大于YW3
C.YCl3分子中Y原子不是稳定的8电子结构
D.Y元素的氧化物对应的水化物为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酸的酸式盐NaHY在水溶液中,HY-的电离程度小于HY-的水解程度。有关的叙述中,正确的是
A. H2Y电离方程式为:H2Y+H2O![]() HY-+H3O+
HY-+H3O+
B. 常温下,该酸式盐的水溶液中溶液中,各离子浓度大小关系为:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
C. 常温下,酸式盐NaHY 的水溶液呈酸性
D. HY-的水解方程式为:HY-+ H2O![]() H3O++Y2-
H3O++Y2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置完成相关实验,不合理的是( )
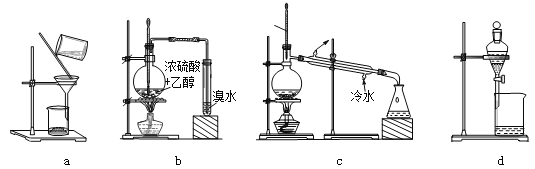
A. 用a趁热过滤提纯苯甲酸B. 用b制备并检验乙烯
C. 用c除去溴苯中的苯D. 用d分离硝基苯与水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com