
【题目】A~J是中学化学中常见的物质,它们之间的转化关系如图所示(部分产物已略去)。已知A是一种高熔点物质,D是一种红棕固体,H的焰色呈黄色。

请回答下列问题:
(1)A物质的化学式为______________,H物质的名称为______________。
(2)G→J的实验现象是______________________________________________,化学方程式为____________________________。
(3)D与C高温下反应的化学方程式为____________________________。
(4)D物质与盐酸恰好反应的离子方程式为____________________________。
【答案】Al2O3偏铝酸钠白色沉淀迅速变为灰绿色,最终变成红褐色沉淀4Fe(OH)2+O2+2H2O=4Fe(OH)3Fe2O3+2Al![]() 2Fe+Al2O3Fe2O3+6H+=2Fe3++3H2O
2Fe+Al2O3Fe2O3+6H+=2Fe3++3H2O
【解析】
A熔融电解生成两种单质,且A的熔点较高,能和氢氧化钠溶液反应,则A是Al2O3,D是红棕色固体,为Fe2O3,氧化铁和铝发生铝热反应生成氧化铝,则C是Al,B是O2,H是NaAlO2,I是AlCl3,E是Fe,F是FeCl2,氯化亚铁和氨水反应生成氢氧化亚铁和氯化铵,G能和氧气反应,则G是Fe(OH)2,J是Fe(OH)3,氢氧化铁在加热条件下分解生成氧化铁,再结合物质之间的反应分析解答。
根据以上分析可知A是Al2O3,B是O2,C是Al,D是Fe2O3,E是Fe,F是FeCl2,G是Fe(OH)2,H是NaAlO2,I是AlCl3,J是Fe(OH)3,则
(1)通过以上分析知,A的化学式为Al2O3,H的名称是偏铝酸钠;
(2)G是白色的氢氧化亚铁沉淀,氢氧化亚铁不稳定,易被氧化为氢氧化铁,反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,其实验现象为白色沉淀迅速变为灰绿色,最终变成红褐色沉淀;
(3)D与C高温下发生铝热反应,反应的化学方程式为Fe2O3+2Al![]() 2Fe+Al2O3。
2Fe+Al2O3。
(4)氧化铁与盐酸恰好反应生成氯化铁和水,反应的离子方程式为Fe2O3+6H+=2Fe3++3H2O。


科目:高中化学 来源: 题型:
【题目】在一个密闭容器中,中间有一个可自由滑动的隔板,将容器分成两部分,当左边充入1molN2,右边充入8gCO和CO2的混合气体,隔板处于如图所示位置(两侧温度相同),则混合气体中CO和CO2的总物质的量为_____mol,其中CO和CO2的分子数之比为_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子在指定溶液中可能大量共存的是( )
A.Na+、Fe2+、ClO-、SO42-B.Fe3+、NH4+、NO3-、SCN-
C.Na+、Cl-、SiO32-、NO3-D.HCO3-、K+、Na+、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的叙述,错误的是( )
A. 镁是第IIA族元素
B. 第IA族元素全部是金属元素
C. O族中无金属元素
D. 第3周期中既有金属元素又有非金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是
A. 标准状况下,2.24LCH3OH分子中共价键的数目为0.5NA
B. 25℃1LpH=12的Na2CO3溶液中,由水电离出H+的数目为0.01NA
C. 1molNa2O2与足量CO2充分反应,转移的电子数为2 NA
D. 0.1molH2和0.1molI2于密闭容器中充分反应后,HI分子总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某可逆反应从0~2分钟进行过程中,在不同反应时间各物质的量的变化情况如下图所示。
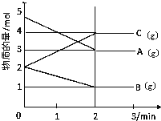
(1)则该反应的化学方程式为__________________;
(2)反应开始至2分钟时,能否用C表示反应速率?_____(填能或不能)。若能,其反应速率为 ;若不能,则其原因为__________;
(3)2分钟后A、B、C各物质的量不再随时间的变化而变化,则此时v正(B)与v逆(C)的等量关系是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,其中X原子最外层电子数是内层电子数的两倍,元素Y的核电荷数等于W原子的最外层电子数,Z在空气中燃烧发出耀眼的白光。下列说法正确的是
A. X和Y的氧化物都是可导致酸雨的污染物
B. Z和W形成的化合物中既有离子键又有共价键
C. 最高价氧化物对应水化物的酸性由强到弱的顺序:W、Y、X
D. 原子半径由大到小的顺序:r(X)>r(Y)>r(Z)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)写出NaHSO4在水中的电离方程式 _________________________。
(2)粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,除去这些杂质的试剂可选用,①Na2CO3、②NaOH、③BaCl2、④HCl,用序号表示加入的先后顺序是______________________。
(3)实验证明铜不能在低温下与O2反应,也不能与稀H2SO4共热发生反应,但工业上却是将废铜屑倒入热的稀H2SO4中并通入空气来制备CuSO4溶液的。铜屑在此状态下被溶解的化学方程式为_______。
(4)利用铜制备CuSO4的另一种方法可用化学方程式表示为________________________。
(5)以上两种方法________(填“前”或“后”)者好,原因是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容积固定的密闭容器中,达平衡的可逆反应2A(g)![]() 2B(?) + C (?)(△H>0),若随着温度升高,气体平均相对分子质量减小,则下列判断正确的是:( )
2B(?) + C (?)(△H>0),若随着温度升高,气体平均相对分子质量减小,则下列判断正确的是:( )
A. B和C可能都是液体 B. B和C肯定都是气体
C. B和C可能都是固体 D. 若C为固体,则B一定是气体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com