
【题目】根据题意解答。
(1)KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其变化可表示为: KClO3+HCl(浓)→ KCl+ClO2↑+Cl2↑+H2O
请完成该化学方程式并配平,并标出电子转移的方向和数目 .
(2)浓盐酸在反应中显示出来的性质是(填写序号).
①只有还原性 ②还原性和酸性③只有氧化性 ④氧化性和酸性
(3)产生0.1mol Cl2 , 则转移的电子的物质的量为 mol.
【答案】
(1)2;4;2;2;1;2;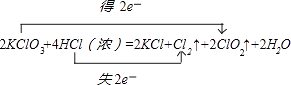
(2)②
(3)0.2
【解析】解:(1)KClO3中氯元素化合价由+5价降低为ClO2中+4价,化合价降低1价;HCl中氯元素化合价由﹣1价升高为Cl2中0价,化合价升高2价,化合价升降最小公倍数为2,故ClO2系数为2,Cl2系数为1;所以KClO3系数为2,KCl系数为2,HCl系数为4,水的系数是2.电子转移的方向和数目为: 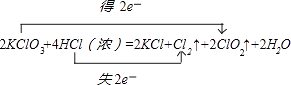
所以答案是:2;4;2;2;1;2; 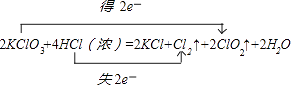 ;(2)反应2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2↑+2H2O中,HCl中氯元素化合价由﹣1价升高为Cl2中0价可知,HCl中氯元素被氧化,HCl在反应中还原剂与酸的作用,各占一半.
;(2)反应2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2↑+2H2O中,HCl中氯元素化合价由﹣1价升高为Cl2中0价可知,HCl中氯元素被氧化,HCl在反应中还原剂与酸的作用,各占一半.
故选:②;(3)反应中只有Cl2是氧化产物,HCl中氯元素化合价由﹣1价升高为Cl2中0价,所以产生0.1molCl2 , 转移的电子的物质的量为0.1mol×2=0.2mol.
所以答案是:0.2.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
【题目】以下为中学化学中常见的物质:①Cu; ②1molL﹣1的FeCl3溶液; ③CuCl2溶液;④CO2;⑤H2SO4;⑥酒精;⑦CaCO3;⑧FeSO4
(1)以上物质中属于电解质的是;属于混合物的是 .
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入②的溶液,至液体呈透明的红褐色氢氧化铁胶体.则反应的化学方程式为;氢氧化铁胶体中分散质微粒的直径范围为nm;判断该胶体制备是否成功的方法是 .
(3)将②③⑧混合配制成浓度均为1molL﹣1的混合溶液100mL,加入一定量的铁粉,充分反应后,若铁粉无剩余,且有铜生成.则反应后的溶液中一定含有阳离子,可能含有阳离子,该阳离子在溶液中物质的量可能的存在范围是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D和Cu五种金属片,将其分别用导线连接后浸入稀硫酸中(如图),每次实验时,通过灵敏电流计测出电子流动方向如下。

根据上述情况,回答下列问题:
(1)上述五种金属的活动性顺序是______________。
(2)在①中,Cu片上观察到的现象是_____________________。
(3)在②中,溶液中H+向金属片______________移动。
(4)在④中,两金属片上均无气泡放出。此时两金属片上的电极反应式分别为Cu:_____________________;B:____________________________。
(5)如果实验⑤用B、D,则导线中电流方向为_______(填“B→D”或“D→B”)。
(6)已知反应:Cu+2Fe3+Cu2++2Fe2+。请用下列试剂和材料,用如图所示装置,将此反应设计成原电池。
试剂:CuCl2溶液、FeCl3溶液、FeCl2溶液、双氧水、NaOH溶液
材料:Cu片、Fe片、石墨棒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由A、B、C、D四种金属按下表中装置图进行实验。
装置 |
|
|
|
现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是_______________。
(2)装置乙中正极的电极反应式是_______________。
(3)装置丙中溶液的pH________(填“变大”“变小”或“不变”)。
(4)四种金属活动性由强到弱的顺序是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关范德华力的说法正确的是( )
A.范德华力尽管很弱,但这种作用力仍属于化学键
B.范德华力具有方向性和饱和性
C.结构和组成相似的物质,其相对分子质量越大,范德华力越大
D.范德华力越大,物质的熔沸点越低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应中的能量变化,表述正确的是:
A. 氧化反应均为吸热反应
B. 断开化学键的过程会放出能量
C. 加热才能发生的反应一定是吸热反应
D. 放热反应中,反应物的总能量大于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关生物体内有机化合物及其功能的叙述,不正确的是( )
A. 葡萄糖是细胞内主要的能源物质 B. 胰岛素能促进肝糖原分解
C. 脱氧核苷酸是DNA的基本组成单位 D. 纤维素是组成植物细胞壁的成分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.
请回答该实验中的问题.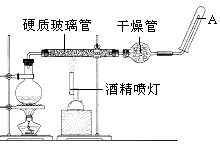
(1)写出该反应的反应方程式:
(2)如何检验该装置的气密性
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是 .
(4)酒精灯和酒精喷灯点燃的顺序是 , 为什么
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为常见的金属单质,根据如图所示的转化关系回答下列问题。

(1)确定A、B、C、D、E、F的化学式:A________,B________,C________,D________,E________,F________。
(2)写出⑧的化学方程式及④、⑤的离子方程式:
⑧的化学方程式________________________________________。
④的离子方程式:__________________________。
⑤的离子方程式:__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com