
【题目】下列能使品红溶液褪色的是( )
A. SO2 B. BaSO4 C. KCl D. CO2
科目:高中化学 来源: 题型:
【题目】现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A. 分液、蒸馏、萃取 B. 萃取、蒸发、分液
C. 分液、萃取、蒸馏 D. 蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和热的测定是重要的定量实验。取0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于下图所示的装置中进行中和热的测定实验,回答下列问题:
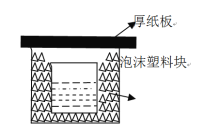
(1)从图中实验装置看,其中尚缺少的两种玻璃用品是_,为保证该实验成功,该同学采取了许多措施,如图的泡沫塑料块的作用在于。
(2)倒入NaOH溶液的正确操作是:(从下列选出)。
A.沿玻璃棒缓慢倒入
B.分三次少量倒入
C.一次迅速倒入
D.简述测量温度的方法
(3)实验记录数据如表
项目 | 反应起始温度T1(℃) | 终止温度T2(℃) | T2-T1 | ||
HCl | NaOH | 平均温度 | |||
第1次 | 26.2 | 26.0 | 29.4 | ||
第2次 | 27.0 | 27.4 | 32.2 | ||
第3次 | 25.9 | 25.9 | 29.1 | ||
第4次 | 26.4 | 26.2 | 29.7 | ||
设0.55mol/LNaOH溶液和0.50mol/L盐酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·℃)。则中和热ΔH=(取到小数点后一位)。
(4)不能用醋酸代替盐酸做此实验,原因是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量Mg、Zn、Al的混合物与足量稀H2SO4反应,生成H2 2.8L(标准状况),则原混合物的质量不可能是( )
A.2g B.4g C.6g D.8g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同温度下,水溶液中c(H+)与c(OH-)关系如图所示。下列说法不正确的是
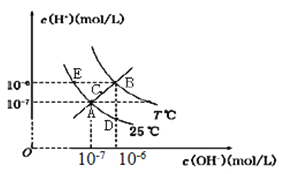
A.图中五点Kw间的关系:B>C>A=D=E
B.E点对应的水溶液中,可能有NH4+、Ba2+、Cl-、I-大量同时存在
C.若0.1 mol/L 的NaHA 溶液水溶液中c(H+)与c(OH-)关系如图D 点所示,则溶液中有: c(HA-)>c(OH-)>c(A2-)>c(H2A)
D.向NaHSO4溶液中滴入Ba(OH)2溶液,当c(H+)与c(OH-)关系如图A点所示,则溶液中反应:2H+ + SO42- + Ba2+ + 2OH- = BaSO4↓+ 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国家规定,酿造食醋的总酸含量标准为3.5~5.0g/100mL(总酸含量即100mL食醋中CH3COOH的质量)。某化学兴趣小组为测定某市售食醋的总酸含量,进行了实验.实验后,得知10.0mL该食醋样品与7.5g溶质的质量分数为4%的氢氧化钠溶液恰好完全反应.计算该市售食醋样品中的总酸含量,并说明是否符合国家标准(假设该市售食醋样品中其他物质不与氢氧化钠发生反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将镁铝的固体混合物0.1mol溶于100mL 2mol·L-1稀硫酸中充分反应后,固体全部溶解,然后再向反应后的混合溶液中滴加2mol·L-1NaOH溶液。
(1)若在滴加NaOH溶液过程中,使Mg2+、Al3+全部生成沉淀,则滴入的NaOH溶液体积是 mL。
(2)设0.1mol镁铝固体混合物中Mg的物质的量分数为a,若在滴加NaOH溶液230mL后,所得沉淀只有Mg(OH)2,则a的取值范围 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如下图所示的装置来测定镁与硫酸反应的速率,在锥形瓶中加入0.7克镁带,按右图连接好装置,从A中加入20.0ml0.5mol/LH2SO4。记录注射器活塞的位置和相应的时间。记录数据如下
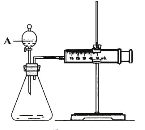
时间/s | 0 | t | 2t | ...... |
活塞的位置/ml | 17.3 | 25.6 | 36.6 | ...... |
(1)检查该装置气密性的方法是。
(2)仪器A的名称是。
(3)0-t时间段与t-2t时间段,化学反应速率最快的是,原因是。
(4)用上述装置探究Fe3+、Cu2+对双氧水分解速率的影响,所用试剂:5%H2O2、0.1mol/LFeCl3、0.2mol/LCuCl2,完成下表的实验设计:
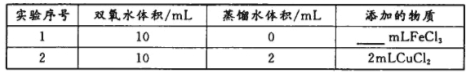
①写出本实验H2O2分解反应方程式并标明电子转移的方向和数目:___________。
②上表中需要添加的物质是mlFeCl3溶液。
③本实验需要测定的数据是。
(5)为确定MnO2催化双氧水分解的最佳条件,用该实验装置进行实验,反应物用量和反应停止的时间数据如下表。
MnO2 时间 H2O2 | 0.1g | 0.3g | 0.8g |
10mL1.5% | 223s | 67s | 36s |
10mL3.0% | 308s | 109s | 98s |
10mL4.5% | 395s | 149s | 116s |
分析表中数据回答下列问题:
①相同浓度的过氧化氢的分解速率随着MnO2用量的增加而_______(填“加快”、“减慢”或“不变”)。
②从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入__________g的MnO2为较佳选择。
③该小组的某同学分析上述数据后认为:“当用相同质量的MnO2时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确?______(填“正确”或“不正确”),理由是_________________________。(提示:H2O2溶液的密度可认为近似相等。)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com