
分析 (1)生石灰是氧化钙;
(2)生石灰只含钙和氧两种元素;
(3)生石灰与水反应生成氢氧化钙,所以可以吸收水分,做干燥剂;
(4)浓硫酸具有吸水性,可用作干燥剂.
解答 解:(1)生石灰是氧化钙,所以化学式为CaO,故答案为:CaO;
(2)生石灰只含钙和氧两种元素,能与酸反应生成盐和水,属于碱性氧化物,故答案为:碱性氧化物;
(3)生石灰与水反应生成氢氧化钙,方程式为:CaO+H2O=Ca(OH)2,所以可以做吸水剂,故答案为:CaO+H2O=Ca(OH)2;
(4)浓硫酸、固体NaOH具有吸水性,P2O5能与水反应,可用作干燥剂,故答案为:浓硫酸、P2O5、固体NaOH等均可做干燥剂.
点评 本题考查了氧化钙的类别和性质,属于对基础知识的考查,题目难度不大.


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:选择题
| A. | 向硫酸铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ | |
| B. | 向Ba(OH)2溶液中滴加NaHSO4溶液至混合溶液恰好为中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| C. | FeSO4溶液与稀硫酸、双氧水混合:2Fe2++H2O2+2H+=2Fe3++2H2O | |
| D. | 向NaHCO3溶液中加入足量Ba(OH)2的溶液:Ba2++2HCO3-+2OH-=2H2O+BaCO3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素基态原子核外共有7种运动状态不同的电子 | |
| B. | 该元素位于周期表的S 区,属于金属元素 | |
| C. | 该元素在周期表中的位置第四周期第VA族 | |
| D. | 该元素M层含有11个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
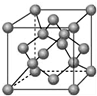 已知A、B、C、D都是元素周期表中前36号的元素.A元素的一种核素没有中子;B的基态原子核外电子有7种不同的运动状态;C元素是无机非金属材料的主角,它的单质可以用作电脑芯片;D元素是地壳中含量第二的金属元素.请回答:
已知A、B、C、D都是元素周期表中前36号的元素.A元素的一种核素没有中子;B的基态原子核外电子有7种不同的运动状态;C元素是无机非金属材料的主角,它的单质可以用作电脑芯片;D元素是地壳中含量第二的金属元素.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com