
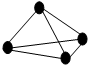
 ,则1molP4中含有6mol非极性键;金刚石晶体碳原子形成4个共价键,则1mol金刚石晶体中含有4mol非极性键,
,则1molP4中含有6mol非极性键;金刚石晶体碳原子形成4个共价键,则1mol金刚石晶体中含有4mol非极性键,

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下28g乙烯中所含极性键的数目为4NA |
| B、将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NAFe3+ |
| C、标准状况下,22.4L甲醇的分子数中所含羟基数为NA |
| D、10L pH=1的硫酸溶液中含有的H+离子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol丙烯酸中含有双键的数目为Na |
| B、等质量14NO和13CO气体中含有的中子数相等 |
| C、一定量的钠与8g氧气作用,若两者均无剩余,转移Na个电子 |
| D、100mlpH=1的醋酸溶液中含有的氢离子数为0.01Na |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(OH-)/c(NH3?H2O) |
| B、c(NH3?H2O)/c(OH-) |
| C、c(H+)和c(OH-)的乘积 |
| D、n(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com