
【题目】福莫特罗是一种治疗哮喘病的药物,它的关键中间体(G)的合成路线如下: 
回答下列问题:
(1)F中的含氧官能团有(填名称);反应④的反应类型为 .
(2)反应①的化学方程式为 .
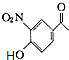
(3)C能与FeCl3溶液发生显色反应,C的结构简式为;D的结构简式为 .
(4)B的同分异构体(不含立体异构)中能同时满足下列条件的共有种.
a.能发生银镜反应 b.能与NaOH溶液发生反应 c.含有苯环结构
其中核磁共振氢谱显示为4组峰,且峰面积比为3:2:2:1的是(填结构简式)
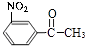
(5)参照G的合成路线,设计一种以 ![]() 为起始原料制备
为起始原料制备 ![]() 的合成路线: .
的合成路线: .
【答案】
(1)醚键、羰基、硝基;取代反应
(2)![]() +(CH3CO)2O→
+(CH3CO)2O→ ![]() +CH3COOH
+CH3COOH
(3)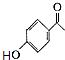 ;
;
(4)17;![]()
(5)![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】解:由D的分子式与E的结构可知,D与 ![]() 发生取代反应生成E,则D为
发生取代反应生成E,则D为 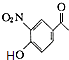 ,C能与FeCl3溶液发生显色反应,含有酚羟基,结合C的分子式逆推可知C为
,C能与FeCl3溶液发生显色反应,含有酚羟基,结合C的分子式逆推可知C为 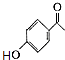 ,A的分子式为C6H6O,A与乙酸酐反应得到酯B,B在氯化铝作用下得到C,则A为
,A的分子式为C6H6O,A与乙酸酐反应得到酯B,B在氯化铝作用下得到C,则A为 ![]() ,B为
,B为 ![]() .E与溴发生取代反应生成F,相当于E中羰基还原为羟基,再发生取代反应得到F.(1)F中的含氧官能团有:醚键、羰基、硝基,反应④的反应类型为取代反应,故答案为:醚键、羰基、硝基;取代反应;(2)反应①的化学方程式为:
.E与溴发生取代反应生成F,相当于E中羰基还原为羟基,再发生取代反应得到F.(1)F中的含氧官能团有:醚键、羰基、硝基,反应④的反应类型为取代反应,故答案为:醚键、羰基、硝基;取代反应;(2)反应①的化学方程式为: ![]() +(CH3CO)2O→
+(CH3CO)2O→ ![]() +CH3COOH,
+CH3COOH,
故答案为: ![]() +(CH3CO)2O→
+(CH3CO)2O→ ![]() +CH3COOH;(3)C的结构简式为
+CH3COOH;(3)C的结构简式为 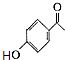 ,D的结构简式为
,D的结构简式为 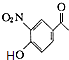 ,
,
故答案为:  ;
;  ;(4)B(
;(4)B( ![]() )的同分异构体(不含立体异构)中能同时满足下列条件:a.能发生银镜反应,说明含有醛基,b.能与NaOH溶液发生反应,说明含有酯基或酚羟基,c.含有苯环结构,
)的同分异构体(不含立体异构)中能同时满足下列条件:a.能发生银镜反应,说明含有醛基,b.能与NaOH溶液发生反应,说明含有酯基或酚羟基,c.含有苯环结构,
若为甲酸形成的酯基,含有1个取代基,可以为甲酸苯甲酯,含有2个取代基为﹣CH3、﹣OOCH,有邻、间、对3种,
若含有醛基、酚羟基,含有2个取代基,其中一个为﹣OH,另外的取代基为﹣CH2CHO,有邻、间、对3种,含有3个取代基,为﹣OH、﹣CH3、﹣CHO,当﹣OH、﹣CH3处于邻位时,﹣CHO有4种位置,当﹣OH、﹣CH3处于间位时,﹣CHO有4种位置,当﹣OH、﹣CH3处于对位时,﹣CHO有2种位置,
符合条件的同分异构体共有17种,其中核磁共振氢谱显示为4组峰,且峰面积比为3:2:2:1的是 ![]() ,
,
故答案为:17; ![]() ;(5)
;(5) ![]() 在氢氧化钠水溶液、加热条件下发生水解反应生成
在氢氧化钠水溶液、加热条件下发生水解反应生成 ![]() ,发生催化氧化生成
,发生催化氧化生成 ![]() ,在硝酸/磷酸条件下发生取代反应生成
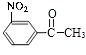
,在硝酸/磷酸条件下发生取代反应生成 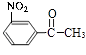 ,最后在NaBH4条件下反应生成
,最后在NaBH4条件下反应生成 ![]() ,合成路线流程图为:
,合成路线流程图为: ![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ,
,
故答案为: ![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() .
.
由D的分子式与E的结构可知,D与 ![]() 发生取代反应生成E,则D为
发生取代反应生成E,则D为 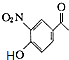 ,C能与FeCl3溶液发生显色反应,含有酚羟基,结合C的分子式逆推可知C为
,C能与FeCl3溶液发生显色反应,含有酚羟基,结合C的分子式逆推可知C为 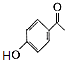 ,A的分子式为C6H6O,A与乙酸酐反应得到酯B,B在氯化铝作用下得到C,则A为
,A的分子式为C6H6O,A与乙酸酐反应得到酯B,B在氯化铝作用下得到C,则A为 ![]() ,B为
,B为 ![]() .E与溴发生取代反应生成F,相当于E中羰基还原为羟基,再发生取代反应得到F.(5)
.E与溴发生取代反应生成F,相当于E中羰基还原为羟基,再发生取代反应得到F.(5) ![]() 在氢氧化钠水溶液、加热条件下发生水解反应生成
在氢氧化钠水溶液、加热条件下发生水解反应生成 ![]() ,发生催化氧化生成
,发生催化氧化生成 ![]() ,在硝酸/磷酸条件下发生取代反应生成
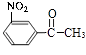
,在硝酸/磷酸条件下发生取代反应生成 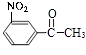 ,最后在NaBH4条件下反应生成
,最后在NaBH4条件下反应生成 ![]() .
.


科目:高中化学 来源: 题型:
【题目】下列A~H八种物质存在如下图所示的转化关系(反应条件、部分产物未标出).已知A是酸式盐,B能使品红溶液褪色,G是红棕色气体,D和H是同一类物质. 
试回答下列问题:
(1)写出下列各物质的化学式:A、H .
(2)按要求写出下列反应的有关方程式 ①A→E反应的离子方程式;
②E→F 反应的化学方程式;
(3)常温下可以用铝制容器盛装浓D,是因为 , 将铁粉逐渐加入100ml浓H中直至过量,按先后顺序写出所发生反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是( )
A.2 mol H2O的摩尔质量和1mol H2O的摩尔质量
B.200 mL 1 molL﹣1氯化钙溶液中c(Cl﹣)和100 mL 2 molL﹣1氯化钾溶液中c(Cl﹣)
C.64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数
D.20% NaOH溶液中NaOH的物质的量浓度和10% NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化镁(MgH2)既可用于劣质燃料的助燃又可同时脱硫脱硝.有关原理如下:
MgH2(s)Mg(s)+H2(g)△H1
2Mg(s)+O2(g)2MgO(s)△H2
2MgO(s)+2SO2(g)2MgSO4(s)△H3
(1)①MgH2的电子式为 .
②反应:SO2(g)+MgH2(s)+O2MgSO4(s)+H2(g)的△H=(用含△H1、△H2、△H3
的代数式表示).
(2)1300℃时,不同微粒的MgH2分解时放氢容量与时间的关系如图1所示. 
则粒径A,B,C从小到大的顺序是 .
(3)在2L的恒容密闭容器中加入1molMgO、1molSO2和0.5molO2 , 发生反应:2MgO(s)+2SO2(g)+O2(g)2MgSO4(s)△H3 , 测得SO2的平衡转化率与温度的关系如图2所示.
①该反应的△H3(填“>”或“<“,下同)0;Q点的反应速率:v(正)v(逆).
②P点对应温度下该反应的平衡常数为 .
③为提高SO2的转化率,除改变温度外,还可采取的措施有(任写2点).
(4)镁铝合金(Mg17Ar12)是一种贮氢合金,完全吸氢时生成氢化镁和金属铝,该吸氢反应的化学方程式为 . 7.32gMg17Ar12完全吸氢后所得的产物与足量稀H2SO4反应,释放出的氢气在标准状况下的体积为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】世界卫生组织(WHO)确认人体中的14种必需微量元素中有铜、铬、硅、碘、氟等. 
(1)铜位于元素周期表区,基态铬原子的价电子排布式为 .
(2)碘酸及高碘酸的结构式如图1所示,酸性较强的是 , 理由是 .
(3)工业上制取单质可通过电解KHF2和HF混合溶液获得,HF2﹣中所包含的作用力有;与HF2﹣互为等电子体的分子为(任填一种).
(4)IO3﹣中碘原子的杂化轨道类型为 , IO3﹣的空间结构为 .
(5)用金属镁还原二氧化硅可得到一种硅镁化合物,其晶胞结构如图2所示.
已知Si4﹣位于晶胞的顶点和面心,Mg2+位于八个小立方体的中心,其晶体参数a=0.635nm.
①SiO2与SiF4相比,熔点更低的是(填化学式).
②硅镁化合物的化学式为;列式表示该硅镁化合物的密度:gcm﹣3(不必计算出结果,NA为阿伏伽德罗常数的数值).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人类较早使用的金属之一,铁及其化合物之间的相互转化作用可用下式表示: Fe2+ ![]() Fe3+
Fe3+ ![]() FeO42﹣(高铁酸根离子)
FeO42﹣(高铁酸根离子)
I.回答下列有关问题:
(1)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒大小范围是nm.
(2)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,生成FeCl2和CuCl2 , 制造印刷电路板.写出FeCl3溶液腐蚀铜的化学反应方程式: . 检验反应后溶液中还存在Fe3+ 的试剂是 .
(3)在下列化学方程式中:2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O还原剂是 , 生成1molNa2FeO4转移电子数目为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近期微博热传的“苯宝宝表情包”是一系列苯的衍生物配以相应的文字形成的(如图所示).则关于有机物的说法正确的是( ) 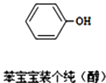
A.碳原子采用sp3杂化
B.氧原子采用sp2杂化
C.该有机物属于醇类
D.该分子中的13个原子有可能处于同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁分别是NaOH、AlCl3、BaCl2、MgCl2四种物质中的一种,若将乙溶液滴入丁溶液中,发现有白色沉淀生成,继续滴加则沉淀消失;乙溶液滴入丙溶液中,无明显现象发生。据此可推断甲物质是
A.BaCl2B.NaOHC.AlCl3D.MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关原子结构和元素周期律的表述正确的是 ( )
A. 第二周期元素的最高正价和负价的绝对值之和等于8
B. ⅦA族元素一定是同周期中非金属性最强的元素
C. 氮的非金属性比磷强,所以氮气的性质比白磷活泼
D. Na+半径大于Cl-半径
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com