
ЁОЬтФПЁПКЃбѓзЪдДЕФРћгУОпгаЙуРЋЧАОАЁЃ
ЃЈ1ЃЉЮоашОЙ§ЛЏбЇБфЛЏОЭФмДгКЃЫЎжаЛёЕУЕФЮяжЪЪЧ________ЃЈЬюађКХЃЉ
AЃЎCl2 BЃЎЕЫЎ CЃЎЩеМю DЃЎЪГбЮ
ЃЈ2ЃЉДгКЃЫЎжаЬсШЁфхЕФжївЊВНжшЪЧЯђХЈЫѕЕФКЃЫЎжаЭЈШыТШЦјЃЌНЋфхРызгбѕЛЏЃЌИУЗДгІЕФРызгЗНГЬЪНЪЧ________________________ЁЃ
ЃЈ3ЃЉЯТЭМЪЧДгКЃЫЎжаЬсШЁУОЕФМђЕЅСїГЬЁЃ
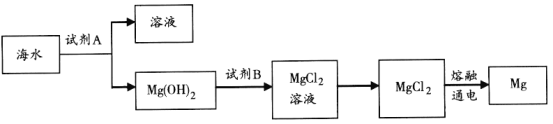
ЂйЙЄвЕЩЯГЃгУгкГСЕэMg2ЃЋЕФЪдМСAЪЧ________ЃЌзЊMgЃЈOHЃЉ2ЛЏЮЊMgCl2ЕФРызгЗНГЬЪНЪЧ________________________________ЁЃ
ЂкгЩЮоЫЎMgCl2жЦШЁMgЕФЛЏбЇЗНГЬЪНЪЧ________________________ЁЃ
ЃЈ4ЃЉКЃДјЛвжаИЛКЌвдIЃаЮЪНДцдкЕФЕтдЊЫиЁЃЪЕбщЪвЬсШЁI2ЕФЭООЖШчЯТЫљЪОЃК
![]()
ЂйзЦЩеКЃДјжСЛвН§ЪБЫљгУЕФжївЊвЧЦїУћГЦЪЧ________________ЁЃ
ЂкЯђЫсЛЏЕФТЫвКжаМгЙ§бѕЛЏЧтШмвКЃЌаДГіИУЗДгІЕФРызгЗНГЬЪН_______________________ЁЃ
ЗДгІНсЪјКѓЃЌдйМгШыCCl4зїнЭШЁМСЃЌеёЕДЁЂОВжУЃЌПЩвдЙлВьЕНCCl4ВуГЪ________ЩЋЁЃ
ЁОД№АИЁПЃЈ1ЃЉBD
ЃЈ2ЃЉCl2+2Br-=Br2+2Cl-
ЃЈ3ЃЉЂйЪЏЛвШщЛђбѕЛЏИЦЃЛMgЃЈOHЃЉ2+2H+=Mg2++2H2O
ЂкMgCl2ЃЈШлШкЃЉ![]() Cl2Ёќ+Mg
Cl2Ёќ+Mg
ЃЈ4ЃЉЂйлслі
Ђк2H++2I-+H2O2ЈTI2+2H2O
ЂлзЯ
ЁОНтЮіЁП
ЪдЬтЗжЮіЃКЃЈ1ЃЉAЃЎЕчНтБЅКЭТШЛЏФЦШмвКЕУЕНЩеМюЁЂЧтЦјЁЂТШЦјЃЌгааТЮяжЪЩњГЩЪєгкЛЏбЇБфЛЏЃЌЙЪAДэЮѓЃЛBЃЎАбКЃЫЎгУеєСѓЕШЗНЗЈПЩвдЕУЕНЕЫЎЃЌЙЪBе§ШЗЃЛCЃЎЕчНтБЅКЭТШЛЏФЦШмвКЕУЕНЩеМюЁЂЧтЦјЁЂТШЦјЃЌгааТЮяжЪЩњГЩЪєгкЛЏбЇБфЛЏЃЌЙЪCДэЮѓЃЛDЃЎАбКЃЫЎгУЬЋбєБЉЩЙЃЌеєЗЂЫЎЗжКѓМДЕУЪГбЮЃЌВЛашвЊЛЏбЇБфЛЏОЭФмЙЛДгКЃЫЎжаЛёЕУЃЌЙЪDе§ШЗЁЃ
ЙЪД№АИЮЊЃКBDЃЛ
ЃЈ2ЃЉТШЦјОпгаЧПбѕЛЏадЃЌФмКЭфхРызгЗЂЩњжУЛЛЗДгІЩњГЩфхЃЌРызгЗНГЬЪНЮЊЃКCl2+2Br-=Br2+2Cl-ЁЃ
ЙЪД№АИЮЊЃКCl2+2Br-=Br2+2Cl-ЃЛ
ЃЈ3ЃЉЂйЙЄвЕЩЯГЃгУЪЏЛвШщЛђбѕЛЏИЦГСЕэMg2+ЃЌCaOКЭH2OЗДгІЩњГЩCaЃЈOHЃЉ2ЃЌCaЃЈOHЃЉ2КЭУОРызгЗДгІЩњ
ГЩMgЃЈOHЃЉ2ЃЛЧтбѕЛЏУОКЭбЮЫсЗДгІЕУЕНТШЛЏУОКЭЫЎЃЌЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃКMgЃЈOHЃЉ2+2HCl=MgCl2+2H2OЃЌЫљвдРызгЗНГЬЪНЮЊMgЃЈOHЃЉ2+2H+=Mg2++2H2OЁЃ
ЙЪД№АИЮЊЃКЪЏЛвШщЛђбѕЛЏИЦЃЛMgЃЈOHЃЉ2+2H+=Mg2++2H2OЃЛ
ЂкШлШкзДЬЌЯТЕчНтТШЛЏУОвБСЖУОЃЌЕчНтЗДгІЗНГЬЪНЮЊMgCl2ЃЈШлШкЃЉ![]() Cl2Ёќ+MgЁЃ
Cl2Ёќ+MgЁЃ
ЙЪД№АИЮЊЃКMgCl2ЃЈШлШкЃЉ![]() Cl2Ёќ+MgЃЛ
Cl2Ёќ+MgЃЛ
ЃЈ4ЃЉЂйзЦЩеЙЬЬхЪБЫљгУЕФжївЊвЧЦїУћГЦЪЧлсліЁЃ
ЙЪД№АИЮЊЃКлсліЃЛ
ЂкМгШыЧтРызгКЭЙ§бѕЛЏЧтЦ№ЕФзїгУЮЊбѕЛЏМСЃЌНЋЕтРызгзЊЛЏЮЊЕЅжЪЕтЃЌРызгЗНГЬЪНЮЊ2H++2I-+H2O2ЈTI2+2H2OЁЃ
ЙЪД№АИЮЊЃК2H++2I-+H2O2ЈTI2+2H2OЃЛ
ЂлЕтЕФCCl4ШмвКГЪзЯЩЋЁЃ
ЙЪД№АИЮЊЃКзЯЁЃ


 КЎМйРждАББОЉНЬг§ГіАцЩчЯЕСаД№АИ
КЎМйРждАББОЉНЬг§ГіАцЩчЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПНЋ7.28g FeШмгкЙ§СПЕФЯЁH2SO4жаЃЌдкМгШШЕФЬѕМўЯТЃЌгУ2.02gKNO3ШЅбѕЛЏШмвКжаFe2+ЃЌД§ЗДгІЭъШЋКѓЃЌЪЃгрFe2+ЛЙаш0.4mol/L KMnO4ШмвК25mLВХФмЭъШЋбѕЛЏЃЌдђKNO3ЕФЛЙдВњЮя
AЃЎNO BЃЎNO2 CЃЎN2O DЃЎN2O3
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
AЃЎЬМдзгМфвдЕЅМќЯрСЌЕФЬўЪЧЭщЬў
BЃЎЫљгаЬЧРрЮяжЪЕФзщГЩЗћКЯCnЃЈH2OЃЉmЭЈЪН
CЃЎгЭжЌгаЙЬЖЈЕФШлЗаЕу
DЃЎЦЯЬбЬЧгыЙћЬЧЛЅЮЊЭЌЗжвьЙЙЬх
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП6дТ26ШеЪЧЙњМЪНћЖОШеЃЌОнЙЋАВВПЭЈБЈЃЌФПЧАБљЖОЁЂвЁЭЗЭшЁЂТШАЗЭЊЕШаТаЭЖОЦЗдкЮвЙњгаНЯДѓДЋВЅЗЖЮЇЃЌЮќЁЂЗЗаТаЭЖОЦЗЮЪЬтЪЎЗжЭЛГіЁЃвбжЊЯТСаЫФжжЖОЦЗЕФНсЙЙМђЪНЃК

ЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЃЈ ЃЉ
AЃЎБљЖОФмгыбЮЫсЗДгІ
BЃЎвЁЭЗЭшОпгаСНад
CЃЎ1molKЗлзюЖрПЩвдгы4molH2ЗЂЩњМгГЩЗДгІ
DЃЎЪЪЕБЬѕМўЯТЃЌ1molДѓТщзюЖрПЩгы3mol Br2ЗЂЩњЗДгІ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСагУЯЕЭГУќУћЗЈУќУћЕФЭщЬўУћГЦе§ШЗЕФЪЧ
AЃЎ2-МзЛљ-3-ввЛљЮьЭщ BЃЎ3,4,4-Ш§МзЛљМКЭщ
CЃЎ2-МзЛљ-4-ввЛљЮьЭщ DЃЎ1,2-ЖўМзЛљЖЁЭщ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТЭМЮЊдЊЫижмЦкБэЕФвЛВПЗжЃЌИљОндЊЫиЂйЁЋЂрдкжмЦкБэжаЕФЮЛжУЃЌАДвЊЧѓЛиД№ЯТСаЮЪЬтЁЃ
зх | IA | 0зх | ||||||
1 | Ђй | IIA | IIIA | ЂєA | VA | ЂіA | VIIA | |
2 | Ђк | Ђл | ||||||
3 | Ђм | Ђн | Ђо | Ђп | Ђр | |||
ЃЈ1ЃЉдкдЊЫиЂйЁЋЂржаЃЌН№ЪєадзюЧПЕФдЊЫиЪЧ_____________ЃЈЬюдЊЫиЗћКХЃЉЃЌзюВЛШнвзаЮГЩЛЏКЯЮяЕФдЊЫиЪЧ______________ЃЈЬюдЊЫиЗћКХЃЉЁЃ
ЃЈ2ЃЉгУЕчзгЪНБэЪОЂпЕФЦјЬЌЧтЛЏЮяЕФаЮГЩЙ§ГЬ__________________________________ЁЃ
ЃЈ3ЃЉЂлЁЂЂмЁЂЂожадзгАыОЖгЩДѓЕНаЁЕФЫГађЪЧ____________________ЃЈЬюдЊЫиЗћКХЃЉЁЃ
ЃЈ4ЃЉБэжаСНжждЊЫиЕФдзгАД1ЃК1зщГЩЕФГЃМћвКЬЌЛЏКЯЮяXвзБЛДпЛЏЗжНтЁЃФГЭЌбЇШЁ5жЇДѓаЁЯрЭЌЕФЪдЙмЃЌИїМгШыЕШЮяжЪЕФСПХЈЖШЕШЬхЛ§ЕФXШмвКЃЌЗжБ№НјааЯТСаЪЕбщЃЌбаОПЭтНчЬѕМўЖдXЗжНтЗДгІЫйТЪЕФгАЯьЃЌЪЕбщМЧТМШчЯТБэЫљЪОЁЃ
ађКХ | ЬѕМў | ЯжЯѓ | НсТл | ||
ЮТЖШЃЏЁц | ДпЛЏМС | ||||
ЕквЛзщ | 1 | 40 | FeCl3ШмвК | ПьЫйВњЩњДѓСПЦјХн | ЯрЭЌЬѕМўЯТЃЌЮТЖШЩ§ИпЃЌЛЏбЇЗДгІЫйТЪМгПь |
2 | 20 | A | ЛКТ§ВњЩњЪЪСПЦјХн | ||
3 | 5 | FeCl3ШмвК | ЛКТ§ВњЩњМЋЩйСПЦјХн | ||
ЕкЖўзщ | 4 | t | MnO2 | ПьЫйВњЩњДѓСПЦјХн | |
5 | 20 | Юо | ЛКТ§ВњЩњМЋЩйСПЦјХн | ||
ЂйЕквЛзщЪЕбщФПЕФЪЧЃКЯрЭЌЬѕМўЯТЃЌЬНОП________________ЖдИУЗДгІЫйТЪЕФгАЯьЁЃ
ЪЕбщ2ЕФДпЛЏМСAЪЧ___________________ЁЃ
ЂкЕкЖўзщЪЕбщжаЃЌЪЕбщ4ЕФЮТЖШtЪЧ_________________ЃЌЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ__________________ЁЃ
ЕкЖўзщЪЕбщНсТлЪЧЃК__________________________________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈе§ШЗЕФЮЊЃЈЁЁЁЁЃЉ
A. 12CЁЂ13CЁЂ14CЁЂН№ИеЪЏЁЂЪЏФЋЖМЪЧЬМдЊЫиЕФЭЌЮЛЫи
B. ЭЌжждЊЫиЕФдзгЃЌжЪСПЪ§вЛЖЈЯрЭЌ
C. ЛЅЮЊЭЌЮЛЫиЕФдзгЃЌжЪзгЪ§вЛЖЈЯрЭЌ
D. гЩвЛжждЊЫизщГЩЕФЮяжЪЃЌвЛЖЈЪЧДПОЛЮя
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЗћКЯЗжзгЪНC4H9ClЕФЭЌЗжвьЙЙЬхЕФЪ§ФПЮЊ
AЃЎ2жж BЃЎ3жж CЃЎ4жж DЃЎ5жж
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдкЯТСаБфЛЏЙ§ГЬжаЃЌМШгаРызгМќБЛЦЦЛЕгжгаЙВМлМќБЛЦЦЛЕЕФЪЧ(ЁЁЁЁ)
AЃЎ НЋSO2ЭЈШыЫЎжаЁЁЁЁЁЁЁЁЁЁ BЃЎ ЩеМюШмгкЫЎ
CЃЎ НЋHClЭЈШыЫЎжа DЃЎ СђЫсЧтФЦШмгкЫЎ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com