
����Ŀ����ͼΪԪ�����ڱ���һ���֣�����Ԫ�������������ڱ��е�λ�ã���Ҫ��ش��������⡣
�� | IA | 0�� | ||||||
1 | �� | IIA | IIIA | ��A | VA | ��A | VIIA | |
2 | �� | �� | ||||||
3 | �� | �� | �� | �� | �� | |||
��1����Ԫ���������У���������ǿ��Ԫ����_____________����Ԫ�ط��ţ���������γɻ������Ԫ����______________����Ԫ�ط��ţ���
��2���õ���ʽ��ʾ������̬�⻯����γɹ���__________________________________��
��3��������������ԭ�Ӱ뾶�ɴ�С��˳����____________________����Ԫ�ط��ţ���
��4����������Ԫ�ص�ԭ�Ӱ�1��1��ɵij���Һ̬������X�ױ����ֽ⡣ijͬѧȡ5֧��С��ͬ���Թܣ�����������ʵ���Ũ�ȵ������X��Һ���ֱ��������ʵ�飬�о����������X�ֽⷴӦ���ʵ�Ӱ�죬ʵ���¼���±���ʾ��
��� | ���� | ���� | ���� | ||
�¶ȣ��� | ���� | ||||
��һ�� | 1 | 40 | FeCl3��Һ | ���ٲ����������� | ��ͬ�����£��¶����ߣ���ѧ��Ӧ���ʼӿ� |
2 | 20 | A | ���������������� | ||
3 | 5 | FeCl3��Һ | ������������������ | ||
�ڶ��� | 4 | t | MnO2 | ���ٲ����������� | |
5 | 20 | �� | ������������������ | ||
����һ��ʵ��Ŀ���ǣ���ͬ�����£�̽��________________�Ը÷�Ӧ���ʵ�Ӱ�졣
ʵ��2�Ĵ���A��___________________��
���ڶ���ʵ���У�ʵ��4���¶�t��_________________��������Ӧ�Ļ�ѧ����ʽ��__________________��
�ڶ���ʵ������ǣ�__________________________________________________��
���𰸡���1��Na��Ar
��2��![]()
��3��Na��S��F
��4�����¶ȣ�FeCl3��Һ
��20��2H2O2![]() 2H2O+O2������20��������ͬ�����£���MnO2���Լӿ�H2O2�ֽ�ķ�Ӧ����
2H2O+O2������20��������ͬ�����£���MnO2���Լӿ�H2O2�ֽ�ķ�Ӧ����
�����������������ͬ����Ԫ�أ������ң�����ԭ������������ԭ�Ӱ뾶��С�������Լ������ǽ�������ǿ��ͬ����Ԫ�أ����ϵ��£�����ԭ������������ԭ�Ӱ뾶���ǽ����Լ�������������ǿ������Ԫ�������������ڱ��е�λ�ÿ�֪����Ϊ��Ԫ�ء���Ϊ��Ԫ�ء���Ϊ��Ԫ�ء���Ϊ��Ԫ�ء���ΪþԪ�ء���Ϊ��Ԫ�ء���Ϊ��Ԫ�ء���Ϊ�Ԫ�ء��ݴ˿ɵ����н��ۣ�
��1������Ԫ��������֪����������ǿ��Ԫ����Ԫ�����ڱ������½ǣ�����ΪNaԪ�أ�ϡ������ԭ�ӵ��������Ӵﵽ�ȶ��ṹ�������仯ѧ���ʽ��ȶ�������������γɻ������Ԫ����ArԪ�ء�
�ʴ�Ϊ��Na��Ar��
��2��HClΪ���ۻ������ԭ�������ȶ��ṹ�����ۼ��γɹ���Ϊ![]() ��
��
�ʴ�Ϊ��![]() ��
��
��3��ԭ�ӵĵ��Ӳ���Խ����ԭ�Ӱ뾶Խ��ͬһ����Ԫ���У�Ԫ��ԭ�Ӱ뾶����ԭ���������������С��
����������Ԫ�ص�ԭ�Ӱ뾶��С˳����Na��S��F��
�ʴ�Ϊ��Na��S��F��
��4����������Ԫ�ص�ԭ�Ӱ�1��1��ɵij���Һ̬������X�ױ����ֽ⣬������ΪH2O2��
�����ݱ�������֪��ֻ���¶Ȳ�ͬ�����ʵ���Ŀ����̽���¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬Ҫ̽���¶ȶԷ�Ӧ��Ӱ�죬����������������ͬ������AΪ�Ȼ�����Һ��
�ʴ�Ϊ���¶ȣ�FeCl3��Һ��
���ڶ���ʵ���У���������Ĵ�����ͬ��Ҫ�о������Է�Ӧ��Ӱ�죬��������Ҫ��ͬ�������¶�Ҫ��ͬ��Ϊ20����˫��ˮ�ڴ����������������·ֽ�����ˮ����������Ӧ����ʽΪ��2H2O2![]() 2H2O+O2�������ݵڶ���ʵ��֪����20��������ͬ�����£���MnO2���Լӿ�H2O2�ֽ�ķ�Ӧ���ʣ�
2H2O+O2�������ݵڶ���ʵ��֪����20��������ͬ�����£���MnO2���Լӿ�H2O2�ֽ�ķ�Ӧ���ʣ�
�ʴ�Ϊ��20��2H2O2![]() 2H2O+O2������20��������ͬ�����£���MnO2���Լӿ�H2O2�ֽ�ķ�Ӧ���ʡ�
2H2O+O2������20��������ͬ�����£���MnO2���Լӿ�H2O2�ֽ�ķ�Ӧ���ʡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��4������2���һ���1����ϩ�����������ò�������Ϊ�� ��
A��4������2���һ����� B��2��5����������
C��2���һ���4�������� D��2��4����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ú��ʯ�͡���Ȼ������Դ��˵���У���ȷ���ǣ� ��
A��ú��̼���� B��ʯ���Ǵ�����
C����Ȼ������Ҫ�ɷ��Ǽ��� D��ú��ʯ�͡���Ȼ���ǿ�������Դ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ������������ԭ��Ӧ���������ȷ�Ӧ����
A������ϡ����ķ�Ӧ
B�����ȵ�ľ̿��CO2��Ӧ
C�������������е�ȼ�շ�Ӧ
D��Ba(OH)2��8H2O������NH4Cl����ķ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Դ�����þ��й���ǰ����
��1�����辭����ѧ�仯���ܴӺ�ˮ�л�õ�������________������ţ�
A��Cl2 B����ˮ C���ռ� D��ʳ��
��2���Ӻ�ˮ����ȡ�����Ҫ��������Ũ���ĺ�ˮ��ͨ�����������������������÷�Ӧ�����ӷ���ʽ��________________________��
��3����ͼ�ǴӺ�ˮ����ȡþ�ļ����̡�
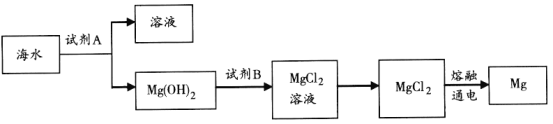
�ٹ�ҵ�ϳ����ڳ���Mg2�����Լ�A��________��תMg��OH��2��ΪMgCl2�����ӷ���ʽ��________________________________��
������ˮMgCl2��ȡMg�Ļ�ѧ����ʽ��________________________��
��4���������и�����I����ʽ���ڵĵ�Ԫ�ء�ʵ������ȡI2��;��������ʾ��
![]()
�����պ������ҽ�ʱ���õ���Ҫ����������________________��
�����ữ����Һ�мӹ���������Һ��д���÷�Ӧ�����ӷ���ʽ_______________________��
��Ӧ�������ټ���CCl4����ȡ���������ã����Թ۲쵽CCl4���________ɫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��ʵ������пƬ��ϡ���ᷴӦ��ȡ����������֤�����Ļ�ԭ�Լ���������п���塣
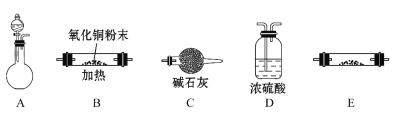
��������������˳��Ϊ________________��װ��C��������_________________��
��п�����ᷴӦ��ȡ�������ʣ���Һ�У�����������ʣ������ᣬ����ȥ��������Ტ��������п���壬���BaCl2��Һ��п�ۡ�NaOH��Һ�����Լ���ѡ��һ���Լ����Ӳ�������������п�����ʵ�����______________________��
��2����ҵ����п��(��Ҫ�ɷ���ZnO��������Fe2O3��CuO��SiO2������)�Ʊ�ZnSO4��7H2O���������¡�
��֪�������£���Һ�е�Fe3+��Zn2+��Fe2+������������ʽ��ȫ������pH�ֱ�Ϊ3.7��6.5��9.7��
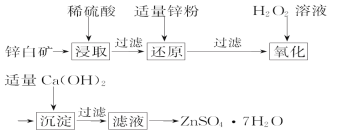
��Ϊ��������Ч�ʣ����Բ�ȡ�Ĵ�ʩ��_____________�� (д����������)��
������������H2O2������Ӧ�����ӷ���ʽΪ___________________________��
������Һ�õ�ZnSO4��7H2O�IJ�������Ϊ__________��___________�����ˡ�ϴ�ӡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʯ�ͻ�������Ҫԭ��CxHy���Ժϳɺܶ��л������������CxHy�ϳ�����E��J ������ͼ��
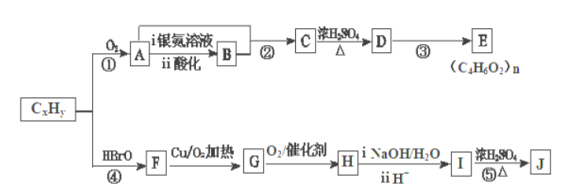
��֪���������з�Ӧ��R��R����������

����J�ķ���ʽΪC4H4O4 ����һ�ֻ�״�����
��1����CxHyͬϵ����������̼ԭ��һ����ƽ����̼ԭ�������ķ��ӵ�������
��2��д��G�еĹ����� ���� ��H������ʽ�� ��
��3������˵����ȷ����
a��CxHy�ͱ�����ʹ��ˮ��ɫ��ԭ����ͬ
b����Ӧ�ںͷ�Ӧ�ܵķ�Ӧ���;�Ϊ�ӳɷ�Ӧ
c��C����Na��NaOH��NaHCO3��Ӧ
d�� E��һ��ˮ���Ժܺõĸ߷��ӻ�����
e��J�����Ի���Ի����о���ˮ��
��4��K��J��ͬ���칹������1 mol K��������NaHCO3��Һ��Ӧ�ɷų�2mol CO2��������д��һ�ַ�������K�Ľṹ��ʽ
��5��д����Ӧ�ݵĻ�ѧ����ʽ
��6��D�ж���ͬ���칹�壬��D������ͬ�����ŵĻ��� ����������˳���칹�������к˴Ź���������3�����շ壬���ܷ���������Ӧ�Ľṹ��ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��ijЩ�����ת����ϵ�����ַ�Ӧ���������δ�г�������֪F��һ�ֺ��ɫ������M��K�dz����Ľ������ʣ�B��һ���д̼�����ζ�����壻��C��Һ�м���BaCl2��Һ�����ɲ�����ϡ����İ�ɫ������
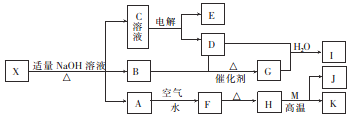
��1����֪��X�����ᾧˮ����X�Ļ�ѧʽΪ_________��
��2������������ʧ��G��D��H2O��ǡ����ȫ��Ӧ����I����ӦʱG��D�����ʵ���֮��Ϊ__________��
��3������K��I��ϡ��Һ��Ӧ�����ӷ���ʽΪ____________________��
��4��J��NaOH��Һǡ����ȫ��Ӧ������һ���Ρ������ε�ˮ��Һ�������տɵõ�_________���ѧʽ����
��5����0.02 mol��L-1��X��Һ�У��������ӵ�Ũ���ɴ�С��˳��Ϊ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Ԫ�������ɵ�������ȷ���ǣ� ��
A. ͬ����Ԫ�����϶��£������Լ���
B. ͬ����Ԫ�����϶��£��õ���������ǿ
C. ͬ����Ԫ��������A��Ԫ�ص�ԭ�Ӱ뾶��С
D. ͬ����Ԫ��������A��Ԫ����̬�⻯�����ȶ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com