
(10分)某白色粉末可能含有K2SO4、NH4Cl、NaCl。请设计合理实验探究该白色粉末的组成。
限选实验仪器与试剂:烧杯、试管、玻璃棒、量筒、胶头滴管、药匙、酒精灯、火柴、试管夹、镊子;红色石蕊试纸、1mol?L-1硫酸、1mol?L-1硝酸、1mol?L-1盐酸、2mol?L-1NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、AgNO3溶液、蒸馏水。
完成以下实验探究过程:
(1)提出假设:根据题意,该白色粉末的组成有______种可能的情况。
(2)设计实验方案
基于该粉末中上述三种盐均存在这一假设,设计出实验方案(不要在答题卡上作答)。
(3)根据(2)的实验方案,叙述实验操作、预期现象和结论。
实验操作 | 预期现象和结论 |
步骤1: |
|
步骤2: |
|
步骤3: |
|
步骤4: |
|
…… |
|
![]() (1) 7 (2分)
(1) 7 (2分)
![]() (3)
(3)
实验操作 | 预期现象和结论 |
步骤1:用药匙取少量白色粉末于试管A底部,点燃酒精灯,充分加热试管。(1分) | 白色粉末减少,有白烟生成,试管上部有白色固体凝结,说明原白色粉末含有NH4Cl。(1分) |
步骤2:用药匙取少量试管A中的残留固体于试管B中,滴加适量蒸馏水,振荡。(1分) | 固体溶解得无色溶液。(1分) |
步骤3:向试管B中滴加过量的 Ba(NO3)2溶液和1mol?L-1硝酸,充分振荡后静置。(1分) | 有白色沉淀生成,证明原白色粉末含有 K2SO4。(1分) |
步骤4:取试管B中上层清液少量于试管C中,滴加 AgNO3溶液和1mol?L-1硝酸。(1分) | 有白色沉淀生成,证明原白色粉末含有NaCl。(1分) |
注:NH4Cl的检验用NaOH溶液和红色石蕊试纸同样得1分;另取样品溶于水进行K2SO4的检验同样得1分;NaCl的检验必须包含有上述4个步骤的操作,共4分(着重号为关键点);步骤设计不合理,次序混乱酌情扣分。


科目:高中化学 来源: 题型:阅读理解
| 实验 编号 |
实验目的 | T/K | 催化剂用量/g | C/mol?l-1 | |
| KMnO4 | H2C2O4 | ||||
| ① | 为以下实验作参考 | 298 | 0.5 | 0.01 | 0.1 |
| ② | 探究KMnO4酸性溶液的浓度对该反应速率的影响 | 298 | 0.5 | 0.001 | 0.1 |
| ③ | 323 | 0.5 | 0.01 | 0.1 | |
| ④ | 探究催化剂对反应速率的影响 | 0.1 | |||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
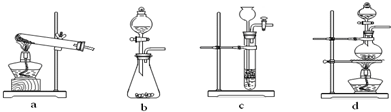
(17分)具有还原性的无水草酸是无色无臭的透明结晶或白色粉末。草酸在浓硫酸并加热条件下容易脱去水分,分解为二氧化碳和一氧化碳。
(1) 草酸(H2C2O4)分解的化学方程式 为: ,
下列装置中,可用于草酸分解制取气体的是 。(填字母)
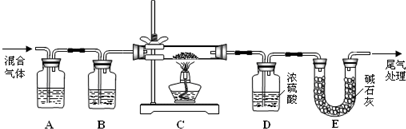
(2) 某探究小组利用草酸分解产生的混合气体和铁锈反应来测定铁锈样品组成(假定铁锈中只有Fe2O3·nH2O和Fe两种成份),实验装置如下图所示,请回答:
① 为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的试剂分别是 、 。
② 在点燃酒精灯之前应进行的操作是:(a) ;(b)通入混合气体一段时间。
③ 准确称量样品的质量10.00 g置于硬质玻璃管中,充分反应后冷却、称量,硬质玻璃 管中剩余固体质量为8.32 g,D中浓硫酸增重0.72 g,则n= (假定Fe和H2O 不发生反应,实验过程中每步均完全吸收或反应)。
④ 在本实验中,下列情况会使测定结果n偏大的是 (填字母)。
a.缺少洗气瓶B b.缺少装置E
c.反应后固体是铁和少量Fe2O3 d.反应后固体是铁和少量Fe2O3·nH2O
(3) 该探究小组还利用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素。
① 请完成以下实验设计表(表中不要留空格):
(每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液的用量均为2mL,催化剂 的用量可选择0.5g、0g)
| 实验 编号 | 实验目的 | T/K | 催化剂用量/g | C/mol·l-1:] | |
| KMnO4 | H2C2O4 | ||||
| ① | 为以下实验作参考 | 298 | 0.5 | 0.01 | 0.1 |
| ② | 探究KMnO4酸性溶液的浓度对该反应速率的影响 | 298 | 0.5 | 0.001 | 0.1 |
| ③ |
| 323 | 0.5 | 0.01 | 0.1 |
| ④ | 探究催化剂对反应速率的影响 |
|
|
| 0.1 |
② 若要准确计算反应速率,该实验中还需测定溶液紫色消失所需要的时间。请你设计出
通过测定褪色时间长短来判断浓度大小与反应速率关系的实验方案 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河南省郑州市高三第一次模拟考试化学试卷(解析版) 题型:实验题
无水AlCl3是一种重要的有机合成催化剂,该物质在183℃时升华,遇潮湿空气即产生大量白雾。某中学化学兴趣小组拟利用中学常见仪器设计实验制备无水AlCl3,实验装置如下图所示。

请回答下列问题:
(1)制备实验开始时,先检查装置的气密性,接下来的操作依次是 。
a.加入MnO2粉末 b.点燃A中酒精灯 c.加入浓盐酸 d.点燃D处酒精灯
(2)写出A装置中发生反应的化学方程式: 。
(3)装置B和C中的试剂分别是 。
(4)甲同学认为F和G可以用一种仪器替代,且加入一种药品即可达到相同效果。这种药品可以是 。
(5)E中得到少量白色粉末,打开软木塞后可明显观察到锥形瓶中有白雾生成,用化学方程式表示其原因 。
(6)制备过程中随着盐酸的浓度下降,氯气的制取反应会停止。为测定残余液中盐酸的浓度,某同学量取残余液10.00mL,加水稀释到250.00mL。然后从中取出20.00mL,用0.1000mol·L-1的NaOH标准溶液进行滴定,终点时消耗NaOH溶液24.00mL。则该残余液体中盐酸的浓度为 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省高三5月模拟考试理科综合化学试卷(解析版) 题型:填空题
(15分)氨基磺酸(H2NSO3H)是一元固体强酸,溶于水和液氨,不溶于乙醇,在工业上用作酸性清洗剂、阻燃剂、磺化剂等。市售商品为白色粉末,在常温下,只要保持干燥不与水接触,固体的氨基磺酸不吸湿,比较稳定。它具有不挥发、无臭味和对人体毒性极小的特点。某实验组用尿素和发烟硫酸(溶有SO3的硫酸)为原料合成氨基磺酸的路线如下 “磺化”步骤中所发生的反应为:
①CO(NH2)2(s) + SO3(g)  H2NCONHSO3H(s)
△H<0
H2NCONHSO3H(s)
△H<0
②H2NCONHSO3H + H2SO4  2H2NSO3H + CO2↑
2H2NSO3H + CO2↑

(1)下图是“磺化”过程的实验装置,恒压滴液漏斗的作用是 ____________

(2)抽滤时,所得晶体要用溶剂乙醇洗涤,则洗涤的具体操作是
(3)实验过程的讨论分析:
①重结晶时用溶剂甲(10%~12%的硫酸)作重结晶的溶剂用而不用水作溶剂的原因是
② “磺化”过程温度与产率的关系如图(1),控制反应温度为75~80℃为宜,若温度高于80℃,氨基磺酸的产率会降低,原因是 。

(4)测定产品中氨基磺酸纯度的方法如下:称取7.920g 产品配成l000mL待测液,量取25.00mL待测液于锥形瓶中,加入2mL 0.2000mol·L-1稀盐酸,用淀粉碘化钾试剂作指示剂,逐滴加入0.08000mol·L-1NaNO2溶液,当溶液恰好变蓝时,消耗NaNO2溶液25.00mL,此时氨基磺酸恰好被完全氧化成N2,NaNO2的还原产物也为N2。
①以酚酞为指示剂,用NaOH进行酸碱中和滴定也能测定产品中氨基磺酸的纯度,测定结果通常比NaNO2法偏高,原因是氨基磺酸中混有 _____ 杂质。
②写出NaNO2滴定法中的化学方程式为: 。
③试求产品中氨基磺酸的质量分数__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com