
下列变化过程不能直接实现的是
①HCl ②Cl2 ③Ca(ClO)2 ④HClO ⑤CO2
A.①→② B.②→③
C.③→④ D.④→⑤
科目:高中化学 来源: 题型:
化合物A经李比希法和质谱法分析得知其相对分子质量为136,分子式为C8H8O2。A的核磁共振氢谱有4个峰且面积之比为1∶2∶2∶3,A分子中只含一个苯环且苯环上只有一个取代基,其核磁共振氢谱与红外光谱如下图。关于A的下列说法中,正确的是( )

A.A分子属于酯类化合物,在一定条件下不能发生水解反应
B.A在一定条件下可与4 mol H2发生加成反应
C.符合题中A分子结构特征的有机物只有1种
D.与A属于同类化合物的同分异构体只有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
部分氧化的FeCu合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理:

下列说法正确的是
A.滤液A中的阳离子为Fe2+、Fe3+、H+ B.样品中CuO的质量为4.0 g
C.V=448 D.原样品中Fe元素的质量分数为41%
查看答案和解析>>
科目:高中化学 来源: 题型:
现有A、B、C、D四种短周期元素,它们之间的关系如下:
Ⅰ.原子半径:A < C < B < D Ⅱ.原子的最外层电子数:A + C = B + D = 8
Ⅲ.原子的核外电子层数:B = C = 2A Ⅳ.B元素的主要化合价:最高正价 + 最低负价 = 2
请回答:
(1)由A、B两种元素组成的常见气体,其电子式为 ▲ ;只有A和B两种元素组成的属于离子晶体的化合物可能为 ▲ (用化学式表示)。
(2)由D元素形成的氢氧化物,与强碱溶液反应的离子方程式为 ▲ 。
(3)由B、C元素组成的化合物BC3,该化合物具有强氧化性,与水反应生成两种酸和一种无色气体,该气体常温下遇空气变红棕色,写出该化合物与水反应的化学方程式 ▲ 。
(4)由A、B和C三种元素组成的盐,常温下其水溶液显酸性,则0.1 mol·L-1 该盐溶液中浓度最大的离子为 ▲ (写离子符号)。
(5)由A、B、C和D四种元素组成的配位化合物己,写出己的化学式 ▲ ;写出检验化合物己中所含阳离子的实验方法 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于漂白粉的叙述正确的是
A.漂白粉的有效成分是Ca(ClO)2和CaCl2
B.漂白粉在空气中久置后会变质
C.漂白粉是由Cl2与烧碱制得的
D.在使用漂白粉时应用浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
用经Cl2消毒的自来水配制下列溶液:①Na2SO3;②KI;③AlCl3;④FeCl2;⑤AgNO3;⑥稀 盐酸,发现部分药品变质,它们是
盐酸,发现部分药品变质,它们是
A.①②④⑤ B.①②③④
C.①②④ D.③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
一氧化二氯(Cl2O)是黄棕色具有强烈刺激性气味的气体。它的熔点为-116 ℃,沸点是3.8 ℃。一氧化二氯不稳定,接触一般有机物易发生爆炸;它易溶于水且易与水反应形成次氯酸溶液。制备出一氧化二氯之后,要冷却为固态才便于操作和贮存,制取少量一氧化二氯,是用干燥的氧化汞与氯气反应(同时还生成HgO·HgCl2)。制备装置如下图所示,加热装置和夹持仪器已略去。
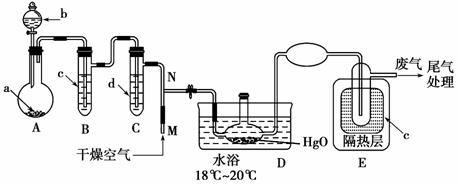
部分物质的有关资料如下:
| 化学式 | N2 | O2 | CO2 | NH3 | Cl2 |
| 熔点(℃) | -209.86 | -218.4 | -78.5(升华) | -77.3 | -101 |
| 沸点(℃) | -195.8 | -183 | -33.35 | -34.6 |
试回答:
(1)试说明加入试剂前检验A、B、C处仪器气密性的操作方法___________________
____________________________________________________________________。
(2)A中盛有的深色固体试剂a应是________,分液漏斗中的b试剂是________。
(3)B中盛有的液体c应是________________,C中的液体d是____________。
(4)D中发生反应的化学方程式是_______________________________________。
(5)E中的保温瓶中盛有液态致冷剂c,它应是________(在“干冰”“冰水”“液态空气”“液氨”“液氯”中选择一种)。在E的内管得到的Cl2O中可能含有的杂质主要是________。
(6)装置D、E间的连接方式与A、B、C间的连接方式有明显的差别,这区别是_____ ___________________________________________________________________,
___________________________________________________________________,
用这种不同的连接方式的主要理由是______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有0.1 mol由等物质的量组成的Fe、Cu合金,研成粉末后,全部投入稀硝酸中,微热使其充分反应,已知硝酸的还原产物只有NO。由于HNO3用量的不同,溶液中的金属离子和残留固体的成分会有多种情况。下列说法不正确的是
A.根据溶液中的金属离子和残留固体的成分最多会有6种情况
 B.若金属有剩余,在溶液中再滴入稀硫酸后,金属又开始溶解
B.若金属有剩余,在溶液中再滴入稀硫酸后,金属又开始溶解
C.当合金刚好溶解时,在标准状况下产生2.24 L NO
D.若合金全部溶解,在溶液中加入过量的氨水,经过滤、洗涤、干燥、充分灼烧、称量、得固体4 g

查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应aA(g)+bB(g)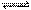 cC(g)+dD(g)ΔH同时符合下列两图中各曲线的规律的( )
cC(g)+dD(g)ΔH同时符合下列两图中各曲线的规律的( )

A.a+b>c+d T1<T2 ΔH<0
B.a+b>c+d T1<T2 ΔH>0
C.a+b<c+d T1>T2 ΔH<0
D.a+b>c+d T1>T2 ΔH>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com