
����A��B��C��D���ֶ�����Ԫ�أ�����֮��Ĺ�ϵ���£�
��ԭ�Ӱ뾶��A < C < B < D ��ԭ�ӵ�������������A + C = B + D = 8
��ԭ�ӵĺ�����Ӳ�����B = C = 2A ����BԪ�ص���Ҫ���ϼۣ�������� + ����� = 2
��ش�
��1����A��B����Ԫ����ɵij������壬�����ʽΪ �� ��ֻ��A��B����Ԫ����ɵ��������Ӿ���Ļ��������Ϊ �� ���û�ѧʽ��ʾ����
��2����DԪ���γɵ����������ǿ����Һ��Ӧ�����ӷ���ʽΪ �� ��
��3����B��CԪ����ɵĻ�����BC3���û��������ǿ�����ԣ���ˮ��Ӧ�����������һ����ɫ���壬�����峣���������������ɫ��д���û�������ˮ��Ӧ�Ļ�ѧ����ʽ �� ��
��4����A��B��C����Ԫ����ɵ��Σ���������ˮ��Һ�����ԣ���0.1 mol��L-1 ������Һ��Ũ����������Ϊ �� ��д���ӷ��ţ���
��5����A��B��C��D����Ԫ����ɵ���λ�����Z��д�����Ļ�ѧʽ �� ��д�����黯���Z�����������ӵ�ʵ�鷽�� �� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������ҹ��IJ����о�Ѹ�ͷ�չ�������������������ܵ����Ͳ��ϡ�
(1)���ǽ�̫����ת��Ϊ���ܵij��ò��ϣ��ӹ����������ȡ�ֹ�Ļ�ѧ����ʽΪ________________________________________________________________________��
(2)������G�ǿ�����һ���������������²��ϡ�G����Է�������Ϊ140�����й�Ԫ�أ�����������Ϊ60%��������Ԫ��Y��E(������Ԫ��)��NH3��Ӧ�Ƶ�G��HCl��G��E��ѧʽ�ֱ�Ϊ________________________________________________________________________��
��ѹ��������G���������������������ս��Ƴ�һ�ָ�ǿ�ȡ���Ӳ�ȡ���ĥ�𡢿���ʴ���մɲ��ϣ���ѧͨʽ�ɱ�ʾΪSi6��xOxY8��x���ڽӽ�1 700 ��ʱx�ļ���ֵԼΪ4.0��������YԪ�صĻ��ϼ�Ϊ________��
(3)�������ײ�����ȱλ������(MFe2Ox��3��x��4��M��Mn��Zn��Ni�Ҿ��ԣ�2�ۣ���ͬ)��������(MFe2O4)�����±�H2��ԭ���ã���֪������(MFe2O4)���»�ԭʱ��������Ӧ��MFe2O4��H2�����ʵ���֮��Ϊ2��1����ԭ����MFe2Ox��x��____________��MFe2Ox�У���2�����룫3���������ʵ���֮��Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������+4�۵���������������л�ԭ�ԡ������Լ�����ˮ��������Һ������������Һ��ϡ���ᡢ����������Һ����ˮ��
��1��Ҫ֤������������Һ���л�ԭ�ԣ�Ӧѡ�õ��Լ��� ���۲쵽�������� ��
��Ӧ�����ӷ���ʽ��
��2��Ҫ֤������������Һ���������ԣ�Ӧѡ�õ��Լ��� ���۲쵽�������� ��
��Ӧ�����ӷ���ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ��ֱ��Ǽס�������ͬѧ����Ӧ��AsO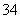 ��2I����2H��
��2I����2H�� AsO
AsO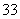 ��I2��H2O����Ƴɵ�ԭ���װ�ã�����C1��C2��Ϊ̼����������ͼ���ձ�����μ�������Ũ���������ͼ��B�ձ�����μ�������40% NaOH��Һ��������������ȷ����
��I2��H2O����Ƴɵ�ԭ���װ�ã�����C1��C2��Ϊ̼����������ͼ���ձ�����μ�������Ũ���������ͼ��B�ձ�����μ�������40% NaOH��Һ��������������ȷ����
A���������ʱ��������(G)ָ�뷢��ƫת
B���������ʱ����Һ��ɫ��dz
C���������ʱ��C2������
D���������ʱ��C1�Ϸ����ĵ缫��ӦΪI2��2e��===2I��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ڿ��淴Ӧ��aA(g)��bB(g)  cC(g)��dD(g) ��H���й�ͼ�����£�
cC(g)��dD(g) ��H���й�ͼ�����£�
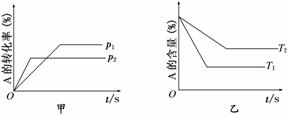
�����в���ȷ����
A��p1<p2��T1>T2 B����Сѹǿ�����淴Ӧ���ʶ���С��ƽ������
C����H>0����S>0 D�������¶ȣ���������ƽ��Ħ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ʢ��Cl2����������ƿ�ס��ҡ����и�ע������Һ���е�һ�֣���������������ͼ��ʾ����ס��ҡ�����ע���Һ��ֱ���
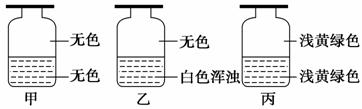
��AgNO3��Һ����NaOH��Һ����ˮ
A���٢ڢۡ������������� B���ڢ٢�
C���ۢ� �� D���٢ۢ�
�� D���٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���б仯���̲���ֱ��ʵ�ֵ���
��HCl����Cl2����Ca(ClO)2����HClO����CO2
A���١��� B���ڡ���
C���ۡ��� D���ܡ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��ѧ��ȤС��Է���м������ͼ��ʾ�Ĵ�������ط�����ȷ����
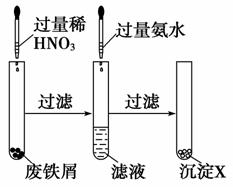
A����Һ��������Fe(NO3)2
B����ʵ���з����ķ�Ӧ��Ϊ������ԭ��Ӧ
C������XΪFe(OH)2
D������X���ȷֽ�õ�Fe2O3

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ����( )
A����100 �桢101 kPa�����£�Һ̬ˮ��������Ϊ40.69 kJ��mol-1����H2O(g)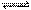 H2O(l) ��
H2O(l) ��
��H = ��40.69 kJ��mol-1
B����25�桢101kPa��2mol S��ȼ������1mol S��ȼ����2��
C��CH4(g) +2O2(g) === CO2(g) +2H2O(g) ��H����akJ��mol-1 �����捻H����ȼ����
| ���ۼ� | C��C | C=C | C��H | H��H |
| ����/ kJ��mol-1 | 348 | 610 | 413 | 436 |
D����֪��
����Լ������Ӧ�Ħ�HΪ��384 kJ��mol-1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com