
下列说法正确的是( )
A.在100 ℃、101 kPa条件下,液态水的气化热为40.69 kJ·mol-1,则H2O(g)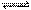 H2O(l) 的
H2O(l) 的
ΔH = —40.69 kJ·mol-1
B.在25℃、101kPa,2mol S的燃烧热是1mol S的燃烧热2倍
C.CH4(g) +2O2(g) === CO2(g) +2H2O(g) ΔH=-akJ·mol-1 ,这里ΔH代表燃烧热
| 共价键 | C-C | C=C | C-H | H-H |
| 键能/ kJ·mol-1 | 348 | 610 | 413 | 436 |
D.已知:
则可以计算出反应的ΔH为-384 kJ·mol-1
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
现有A、B、C、D四种短周期元素,它们之间的关系如下:
Ⅰ.原子半径:A < C < B < D Ⅱ.原子的最外层电子数:A + C = B + D = 8
Ⅲ.原子的核外电子层数:B = C = 2A Ⅳ.B元素的主要化合价:最高正价 + 最低负价 = 2
请回答:
(1)由A、B两种元素组成的常见气体,其电子式为 ▲ ;只有A和B两种元素组成的属于离子晶体的化合物可能为 ▲ (用化学式表示)。
(2)由D元素形成的氢氧化物,与强碱溶液反应的离子方程式为 ▲ 。
(3)由B、C元素组成的化合物BC3,该化合物具有强氧化性,与水反应生成两种酸和一种无色气体,该气体常温下遇空气变红棕色,写出该化合物与水反应的化学方程式 ▲ 。
(4)由A、B和C三种元素组成的盐,常温下其水溶液显酸性,则0.1 mol·L-1 该盐溶液中浓度最大的离子为 ▲ (写离子符号)。
(5)由A、B、C和D四种元素组成的配位化合物己,写出己的化学式 ▲ ;写出检验化合物己中所含阳离子的实验方法 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有0.1 mol由等物质的量组成的Fe、Cu合金,研成粉末后,全部投入稀硝酸中,微热使其充分反应,已知硝酸的还原产物只有NO。由于HNO3用量的不同,溶液中的金属离子和残留固体的成分会有多种情况。下列说法不正确的是
A.根据溶液中的金属离子和残留固体的成分最多会有6种情况
 B.若金属有剩余,在溶液中再滴入稀硫酸后,金属又开始溶解
B.若金属有剩余,在溶液中再滴入稀硫酸后,金属又开始溶解
C.当合金刚好溶解时,在标准状况下产生2.24 L NO
D.若合金全部溶解,在溶液中加入过量的氨水,经过滤、洗涤、干燥、充分灼烧、称量、得固体4 g

查看答案和解析>>
科目:高中化学 来源: 题型:
化合物X的分子式为C5H11Cl,用NaOH的醇溶液处理X,可得分子式为C5H10的两种产物Y、Z,Y、Z经催化加氢后都可得到2甲基丁烷。若将化合物X用NaOH的水溶液处理,则所得有机产物的结构简式可能是( )
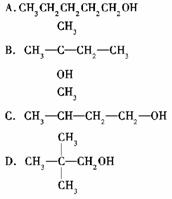
查看答案和解析>>
科目:高中化学 来源: 题型:
金刚烷是一种重要的化工原料,工业上可通过下列途径制备:
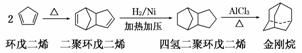
请回答下列问题:
(1)环戊二烯分子中最多有________个原子共平面;
(2)金刚烷的分子式为________,其分子中的CH2基团有________个;
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:
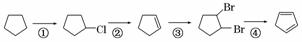
其中,反应 ①的产物名称是________,反应②的反应试剂和反应条件是________,反应③的反应类型是________;
①的产物名称是________,反应②的反应试剂和反应条件是________,反应③的反应类型是________;
(4)已知烯烃能发生如下反应:

 RCHO+R′CHO
RCHO+R′CHO
请写出下列反应产物的结构简式:
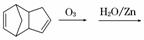 ___________________________________________;
___________________________________________;
(5)A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸[提示:苯环上的烷基(—CH3,—CH2R,—CHR2)或烯基侧链经高锰酸钾酸性溶液氧化得羧基],写出A所有可能的结构简式(不考虑立体异构):
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
T ℃时在2 L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的百分含量与时间的关系如图2所示。则下列结论正确的是( )
A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·L-1·min-1
B.容器中发生的反应可表示为:3X(g)+Y(g) === 2Z(g)
C.保持其他条件不变,升高温度,反应的化学平衡常数K增大
D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应aA(g)+bB(g)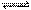 cC(g)+dD(g)ΔH同时符合下列两图中各曲线的规律的( )
cC(g)+dD(g)ΔH同时符合下列两图中各曲线的规律的( )

A.a+b>c+d T1<T2 ΔH<0
B.a+b>c+d T1<T2 ΔH>0
C.a+b<c+d T1>T2 ΔH<0
D.a+b>c+d T1>T2 ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.反应CaCO3(s)=CaO(s)+CO2(g)在常温下不能发生,则该反应的△H>0
B.0.1 mol·L-1CH3COOH溶液加水稀释后,溶液中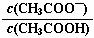 的值减小
的值减小
C.铅蓄电池在放电过程中,负极质量增加,正极质量减少
D.锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去
查看答案和解析>>
科目:高中化学 来源: 题型:
有n种微粒的电子层结构如图所示: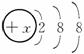 。其中:
。其中:
(1)某电中性的微粒一般不和其他元素的原子反应,这种微粒的符号为________。
(2)某微粒的可溶性盐溶液,加入AgNO3溶液会出现白色沉淀,且该沉淀不溶于酸,这种微粒的符号是________________________________________________________________________。
(3)某微粒带一个单位正电荷,且氧化性很弱,但得到电子后还原性很强,这种微粒的符号为________。
(4)某微粒是一种常见的还原剂,且这种微粒失去2个电子后即变为原子,这种微粒的符号是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com