
����Ŀ������Ҫ�����
(1)CaCO3(s)���ȷֽ�����CaO(s)��CO2(g)����S____________��������>0������<0������=0����
(2)��֪��1 mol H��H���� 1 mol N��H����1 mol N��N���ֱ���Ҫ��������436 kJ��391 kJ��946 kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ___________________________________________________________��
(3)��֪��![]() ��H��-393.5kJ/mol
��H��-393.5kJ/mol
![]() ��H��-571.6kJ/mol
��H��-571.6kJ/mol
![]() ��H��-2599 kJ/mol
��H��-2599 kJ/mol
����298Kʱ��C(s��ʯī)��H2(g)���� 1 mol C2H2(g)��Ӧ���ʱ䣺![]() ___________________��
___________________��
(4)ij�о�����������ͼ��ʾװ���õ绯ѧԭ���������ᡣ

ͨ��SO2��һ���缫��Ӧʽ��__________________________________
(5)��25 �桢101 kPa�£�1 g�״�ȼ������CO2��Һ̬ˮʱ����22.68 kJ�����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ______________________________��
���𰸡�>0 ![]() 226.7 kJ��mol��1
226.7 kJ��mol��1 ![]()
![]()
��������
��1���������ֵ�������壬���̼��ƷֽⷴӦ����������Ӧ������S>0��
��2��N2��H2��Ӧ����NH3�Ļ�ѧ����ʽΪN2��3H2![]() 2NH3���䷴Ӧ������ܺ�=��946+436��3��kJ/mol=2254kJ/mol�����������=391��3��2 kJ/mol=2346kJ/mol���䷴Ӧ�ʱ�
2NH3���䷴Ӧ������ܺ�=��946+436��3��kJ/mol=2254kJ/mol�����������=391��3��2 kJ/mol=2346kJ/mol���䷴Ӧ�ʱ�![]() H=2254kJ/mol-2346kJ/mol=-92 kJ/mol����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ��
H=2254kJ/mol-2346kJ/mol=-92 kJ/mol����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ��![]() ��
��
��3���Ӧ��![]() ��H��-393.5kJ/mol
��H��-393.5kJ/mol
��![]() ��H��-571.6kJ/mol
��H��-571.6kJ/mol
��![]() ��H��-2599 kJ/mol
��H��-2599 kJ/mol
���ݸ�˹���ɣ�������2+����![]() -����
-����![]() �ɵã�2C(s��ʯī)��H2(g)=C2H2(g) ��H��[��-393.5����2+��-571.6����
�ɵã�2C(s��ʯī)��H2(g)=C2H2(g) ��H��[��-393.5����2+��-571.6����![]() -��-2599����
-��-2599����![]() ] kJ/mol=+226.7 kJ/mol��
] kJ/mol=+226.7 kJ/mol��
��4����ͼ��֪��ͨ���SO2����������Ӧ������SO42-����ͨ��SO2��һ���缫��ӦʽΪ��![]() ��
��
��5����25 �桢101 kPa�£�1 g�״�ȼ������CO2��Һ̬ˮʱ����22.68 kJ����1mol�״���ȫȼ�����ų�������Ϊ32��22.68 kJ=725.76kJ�����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Y���п������������ã�����X�Ƶá������йػ�����X��Y��˵����ȷ����

A.X��Y����������KMnO4��Һ��Ӧ
B.1 mol X�������2 mol NaOH��Ӧ
C.Y���Ҵ�����������Ӧ�ɵõ�X
D.1 mol Y��NaHCO3��Ӧ��������1 mol CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����(����)
A.��ʯī���缫���CuSO4��Һ��![]()
B.����ͭƬ���缫���AgNO3��Һ��![]()
C.��ʯī���缫���MgCl2��Һ��![]()
D.��ʯī���缫���NaCl��Һ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڻ�ѧ��Ӧ���ʵ�˵����ȷ���� ( )
A. �����¶ȿɽ��ͻ�ѧ��Ӧ�Ļ�ܣ�ʹ��ѧ��Ӧ�������
B. ���¶ȡ��������ͬ���������У��ֱ������ͬ���ʵ�����Br2��Cl2�������������������������Ӧ����Ӧ������ͬ
C. 0.1 mol��L-1�����0.1 mol��L-1��������ͬ��״�ʹ�С�Ĵ���ʯ��Ӧ��������ͬ
D. ������μӵĻ�ѧ��Ӧ��������ѹǿ������С��Ӧ�������ݻ����������ӻ���ӵİٷ������Ӷ�ʹ��Ӧ���ʼӿ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ж���![]() ˵������ȷ���ǣ� ��
˵������ȷ���ǣ� ��
A.��֪��![]() ��
��![]() ��Ҫʹ
��Ҫʹ![]() ��NO���������ȫ��NaOH���գ��������������ʵ�����
��NO���������ȫ��NaOH���գ��������������ʵ�����![]()
B.����β����ת��װ�ÿɽ�β���е�NO��CO���к�����ת��Ϊ![]() ��
��![]() ����װ���еĴ����ɽ���NO��CO��Ӧ�Ļ�ܣ���������߸÷�Ӧ��ƽ��ת����
����װ���еĴ����ɽ���NO��CO��Ӧ�Ļ�ܣ���������߸÷�Ӧ��ƽ��ת����
C.��![]() ��ԭ
��ԭ![]() ����N2��H2O�������ı����
����N2��H2O�������ı����![]()
![]() ʱת��
ʱת��![]() ����
����
D.װ��4L![]() ��NO��������������������ʢ��ˮ��ˮ���У���ͨ����ͬ������
��NO��������������������ʢ��ˮ��ˮ���У���ͨ����ͬ������![]() ��ǡ�ó�������
��ǡ�ó�������![]() ��NO�����Ϊ1��1
��NO�����Ϊ1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϩ��Ϊԭ�ϣ��ϳ�ijЩ�߾����·�����£�
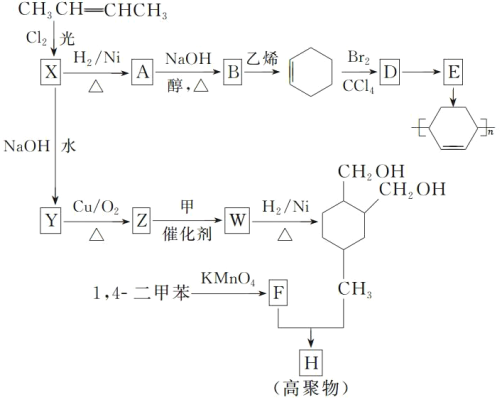
��֪��

��1��CH3CH=CHCH3 ��������_____��
��2��X �к��еĹ�������_____��
��3��A��B �Ļ�ѧ����ʽ��_____��
��4��D��E �ķ�Ӧ������_____��
��5����Ϊ����F ���� NaHCO3 ��Ӧ���� CO2��
�������й�˵����ȷ����_____��
a���л���Z �ܷ���������Ӧ
b���л���Y ��HOCH2CH2OH ��Ϊͬϵ��
c���л���Y �ķе�� B ��
d���л���F ���뼺�������۳ɾۺ���
��Y ��ͬ���칹���ж��֣�д�����ӽṹ�к�������������ͬ���칹��Ľṹ��ʽ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȥ���°�����ʡ��������ʮ�����ء�PM2.5ϸ�����ﺬ�еĶ���������Դ֮һ������β���ŷš�ͨ�������ܼ�װ��װ�ã�����Ч����CO��NO���ŷţ���װ���ڷ����ķ�ӦΪ��NOx+CO��N2+CO2�����й��ڴ˷�Ӧ��˵���У�����ȷ����
A.���漰Ԫ�صĵ�һ�����ܣ�N��O��C
B.��x=2ʱ��ÿ����1molN2��ת�Ƶ�����Ϊ4mol
C.�����ʵ���N2��CO2�У�![]() ���ĸ�����Ϊ1:1
���ĸ�����Ϊ1:1
D.�������뻹ԭ�������ʵ���֮��Ϊ1:1ʱ��NOx�е�Ԫ�صĻ��ϼ�Ϊ+2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 ��ʱ�������й���Һ���������ʵ���Ũ�ȹ�ϵ��ȷ���ǣ�������
A.0.1 mol��L��1(NH4)2Fe(SO4)2��Һ�У�c(![]() )>c(
)>c(![]() )>c(Fe2��)>c(H��)
)>c(Fe2��)>c(H��)
B.pH��11�İ�ˮ��pH��3��������Һ�������ϣ�������Һ�У�c(Cl��)>c(![]() )>c(OH��)>c(H��)
)>c(OH��)>c(H��)
C.��0.1 mol��L��1 Na2CO3��Һ�У�2c(Na��)��c(![]() )��c(
)��c(![]() )��c(H2CO3)
)��c(H2CO3)
D.0.1 mol��L��1�Ĵ�������Һ20 mL��0.1 mol��L��1����10 mL��Ϻ���Һ�����ԣ�c(CH3COO��)> c(Cl��)> c(CH3COOH)> c(H��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��25 �桢101 kPa�������£�

��ش������й����⣺
����H��H��H2��������1 mol H2ʱ��Ҫ________(���������������ų�������ͬ)436 kJ����������Cl2��Cl��Cl��������1 mol Cl2�еĹ��ۼ�ʱ��Ҫ________243 kJ��������
�ڶ��ڷ�ӦH2(g)��Cl2(g)=2HCl(g)���������2 molHCl(g)ʱ����Ӧ�����зų�183 kJ����������Ͽ� 1 mol H��Cl �������������________kJ��
����������Ӧ��a.H2(g)��Cl2(g)![]() 2HCl(g)��b.H2(g)��Cl2(g)
2HCl(g)��b.H2(g)��Cl2(g)![]() 2HCl(g)����������Ӧ�У���ͬ���ʵ�����H2(g)��Cl2(g)��Ӧ������ͬ������HCl(g)ʱ���ų�������________(��������������������)��
2HCl(g)����������Ӧ�У���ͬ���ʵ�����H2(g)��Cl2(g)��Ӧ������ͬ������HCl(g)ʱ���ų�������________(��������������������)��
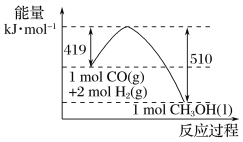
(2)����ͼʾ������ת����ϵ�жϣ�����16 g CH3OH(l)________(���������������ų���)________kJ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com