
【题目】下列离子方程式正确的是
A.足量铁屑溶于稀硝酸: Fe+2H+= 2Fe2++ H2↑
B.氯化铝溶液中加入过量的氨水:Al3+ + 4NH3·H2O =AlO2- + 4NH4++ 2H2O
C.NO2通入水中:3NO2 + H2O = 2H+ + 2NO3- + NO
D.实验室用加热铵盐和碱的固体混合物的方法制取氨:OH- + NH4+ ![]() NH3↑+ H2O
NH3↑+ H2O
【答案】C
【解析】
A.因为硝酸有强氧化性,Fe与稀硝酸反应不产生H2,足量铁屑溶于稀硝酸反应生成硝酸亚铁、NO和水,则离子方程式为3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故A错误;
B.氯化铝溶液中加入过量的氨水,生成氢氧化铝沉淀,而氢氧化铝不溶于氨水,正确的离子方程式为:Al3++3NH3H2O═3NH4++Al(OH)3↓,故B错误;
C.NO2通入水中,反应生成硝酸和一氧化氮,该反应的离子方程式为:3NO2+H2O═2H++2NO3-+NO,故C正确;
D.实验室用加热铵盐和碱的固体混合物的方法制取氨,此反应是固固反应,不是在溶液中进行,不能用OH- + NH4+ ![]() NH3↑+ H2O来表示,故D错误;
NH3↑+ H2O来表示,故D错误;
答案为C。


科目:高中化学 来源: 题型:
【题目】如图装置,放电时可将 Li、CO2 转化为 Li2CO3 和 C,充电时选用合适催化剂仅使Li2CO3 转化为Li、CO2 和O2。下列有关表述正确的是( )
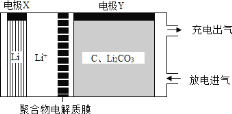
A.放电时,Li+向电极X 方向移动
B.放电时,每转移 4mol 电子,生成 1mol C
C.充电时,电极Y 应与外接直流电源的负极相连
D.充电时阳极的电极反应式为 C+2Li2CO3+4e- = 3CO2+4Li+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 烷烃的通式为CnH2n+2,随n值增大,碳元素的质量百分含量逐渐减小
B. 乙烯与溴加成反应的产物为溴乙烷
C. 1 mol苯恰好与3 mol氢气完全加成,说明苯分子中有三个碳碳双键
D. n=7,主链上有5个碳原子的烷烃共有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA
B.1L0.1molL-1NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA
C.235g核素![]() U发生裂变反应:
U发生裂变反应:![]() U+
U+![]() n
n![]()
![]() Sr+
Sr+![]() Xe+10
Xe+10![]() n,净产生的中子(
n,净产生的中子(![]() n)数为10NA
n)数为10NA
D.标准状况下,11.2L甲烷和乙烯混合物中含氢原子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是__________。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的 pH 均增大
②在相同时间内, 两烧杯中产生气泡的速度: 甲__________乙(填“>”、 “<”或“=”)。
③请写出图中构成原电池的负极电极反应式: ____________。
④当甲中溶液质量增重 31.5 克时,电极上转移电子数目为______。
(2)图丙为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是 KOH。通甲烷一极的电极反应方程式为 ______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是( )
A.加入少量水,水的电离平衡向电离方向移动
B.再通入少量氯气,Cl2+H2O![]() HCl+HCIO,平衡向正方向移动,c(Cl2)减少
HCl+HCIO,平衡向正方向移动,c(Cl2)减少
C.通入少量SO2,溶液漂白性增强
D.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜单质及其化合物在很多领域有重要用途,如金属铜用来制造电线电缆,五水合硫酸铜可用作杀菌剂等。
(1)基态Cu2+的核外电子排布式为____________。
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下:
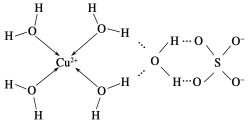
①胆矾的化学式用配合物的形式表示为____________。
②胆矾中SO42-的立体构型名称为________,H2O的VSEPR模型名称为____。
(3)向硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是______________________。
(4)Cu3N形成的晶体结构如下图所示,N3-的配位数是______。设晶胞边长为a cm,密度为b g/cm3,则阿伏加德罗常数可表示为______________(用含a、b的式子表示)。
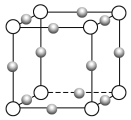
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用橄榄石尾矿(主要成分为MgO及少量FeO、Fe2O3、Al2O3等)制备纯净氯化镁晶体(MgCl2·6H2O),实验流程如下:

已知几种金属阳离子形成氢氧化物沉淀时的pH如下表

回答下列问题:
(1)“浸取”步骤中,能加快浸取速率的方法有______________________(任写两种)。
(2)气体X的电子式为___________,滤渣1经过处理可以制得一种高效的无机高分子混凝剂、净水剂,其化学式为[Fe2(OH)n(SO4)(3-0.5n)]m,则该物质中铁元素的化合价为___________。
(3)加入H2O2的目的是___________;若将上述过程中的“H2O2”用“ NaClO”代替也能达到同样目的,则发生反应的离子方程式为_________________________________。
(4)“一系列操作”主要包括加入足量盐酸,然后经过______________________、过滤、洗涤,即得到氯化镁晶体。
(5)准确称取2.000g氯化镁晶体产品于250mL锥形瓶中,加水50mL使其完全溶解,加入100mL氨性缓冲液和少量铬黑T指示剂,溶液显酒红色,在不断震荡下,用0.5000mol·L-1的EDTA标准溶液进行滴定,其反应原理为Mg2++Y4-=MgY2-,滴定终点时消耗EDTA标准溶液的体积19.00mL。
①则产品中MgCl2·6H2O的质量分数为___________(结果保留3位有效数字)。
②下列滴定操作会导致测量结果偏高的是___________(填宇母)。
a.锥形瓶洗涤后没有干燥 b.滴定时锥形瓶中有液体溅出
c滴定终点时俯视读数 d滴定管滴定前有气泡,滴定后气泡消失
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com