
| A.阳离子只能得到电子被还原,只能作氧化剂 |
| B.海轮外壳上镶入锌块,可减缓船体的腐蚀 |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.为减少中和滴定实验的误差,锥形瓶必须洗净并烘干后使用 |
科目:高中化学 来源:不详 题型:单选题

| A.放电时储氢合金作正极 |
| B.充电时储氢合金作阳极 |
| C.充电时阳极周围c(OH―)增大 |
| D.放电时负极反应:LaNi5H6 + 6OH―→ LaNi5 + 6H2O + 6e― |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.粗铜精炼时,把粗铜接在电源的负极 |
| B.充电时,把铅蓄电池的负极接在外电源的正极 |
| C.镀锡铁破损后铁更易被腐蚀 |
D.碱性氢氧燃料电池工作时,负极反应为: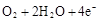 = =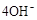 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
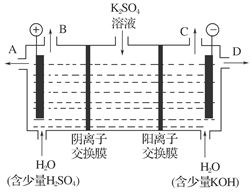
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向1mol/L氯化铁溶液中加入1mol/L氢氧化钠溶液可制得氢氧化铁胶体 |
| B.0.1mol/L的氨水和氢氧化钠溶液分别稀释100倍后,氢氧化钠溶液的pH较氨水的大 |
| C.用标准盐酸滴定未知浓度的氢氧化钠溶液,选用石蕊试液作指示剂 |
| D.在铜、锌、稀硫酸构成的原电池中,阳离子向负极移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.放电时,钠极发生还原反应 |
| B.放电时,钠作正极,硫作负极 |
| C.充电时,阳极发生的反应是:Sx2--2e- = xS |
| D.充电时,钠极与外电源的正极相连,硫极与外电源的负极相连 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
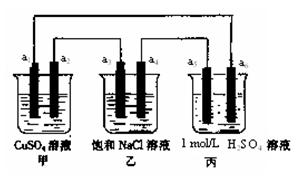
| A.a2电极上有亮红色固体 |
| B.a1、a3电极上产生的物质,物质的量比是1:2 |
| C.丙中的SO42-向a6电极移动 |
| D.当装置电路中有6.02×1021个电子通过时,乙中溶液的pH是13 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com