
| 实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
| 1 | 25.00 | 24.41 |
| 2 | 25.00 | 24.39 |
| 3 | 25.00 | 22.60 |


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.pH=3的硝酸和pH=11的氢氧化钠溶液 |
| B.pH=3的盐酸和pH=11的氨水 |
| C.pH=3的硫酸和pH=11的氢氧化钠溶液 |
| D.pH=3的醋酸和pH=11的氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2H2(g)+O2(g)=2H2O(l)△H=—285.8kJ·mol—1 |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=+890.3kJ·mol—1 |
| C.H2(g)+1/2O2(g)=H2O(g)△H<—285.8kJ·mol—1 |
| D.C(s)+2H2(g)=CH4(g)△H=—74.8 kJ·mol—1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层) | pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径 |
| B.钢铁是用量最大、用途最广泛的合金 |
| C.硅主要以单质、氧化物、硅酸盐的形式存在于自然界中 |
| D.利用催化设施,可以将汽车尾气中CO和NO转化为无害气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
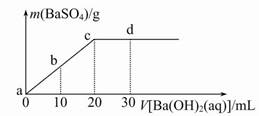
| A.a~d溶液的pH:a<b<c<d |
| B.a~d溶液的导电能力:a<b<c<d |
| C.b处溶液的c(H+)与d处溶液的c (OH-)相等 |
| D.c处溶液和d处溶液均呈碱性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.01mol/L CH3COOH | B.0.01mol/L HNO3 |
| C.pH=2的H2SO4溶液 | D.pH=2的CH3COOH溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.11∶1 | B.9∶1 | C.1∶11 | D.1∶9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com