
| A. | M、X、A、E | B. | A、M、X、E | C. | M、X、E、A | D. | E、A、M |
分析 依据氧化还原反应的强弱规律,结合题干中反应分析判断,标注化合价判断氧化剂、还原剂、氧化产物、还原产物,依据氧化还原反应中还原剂的还原性大于还原产物,氧化剂的氧化性大于氧化产物,进行判断.
解答 解:①水溶液中,M+X2+═M2++X,还原剂M的还原性大于还原产物X,即M>X;
②A+2H2O(冷)═A(OH)2+H2↑,还原剂A的还原性大于还原产物H2,即A>H2;
③X、E相连浸入稀H2SO4中,电极反应:X-2e-═X2+,2H++2e-═H2↑,说明X易失去电子,还原性X>E;
由于A能和冷水反应,而M在溶液中不与水反应,所以A的还原性最大;
所以还原性由强到弱的顺序是A>M>X>E;故选B.
点评 本题考查了氧化还原反应的概念应用和氧化还原反应的强弱规律应用,主要是还原性强弱的比较判断.


科目:高中化学 来源:2016-2017学年辽宁省高一上10月月考化学卷(解析版) 题型:选择题
下列说法正确的是
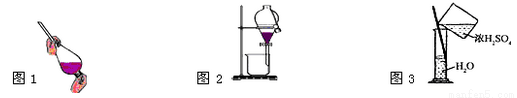
A. 萃取操作时,振荡过程中需要放气,放气是通过打开分液漏斗上口的玻璃塞进行的
B. 可以采用蒸发浓缩、冷却结晶的方法从硝酸钾溶液中获得硝酸钾晶体
C. 将乙醇与水分离,如图1、图2操作
D. 稀释浓H2SO4,如图3操作
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
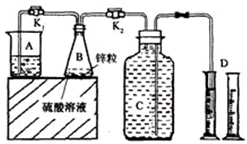
| 实验序号 | 硫酸浓度 | 饱和硫酸铜溶液体积/mL | B反应达到平稳时间/min | 第1分钟收集氢气体积/mL | 第2分钟收集氢气体积/mL | 第3分钟收集氢气体积/mL | … |
| 1 | 20% | 0 | 5.4 | 6.1 | 11.9 | 13.7 | … |
| 2 | 20% | 0.5 | 2.5 | 23.9 | 32.1 | 33.5 | … |
| 3 | 30% | 0.5 | 1.1 | 60.7 | 89.9 | 90.1 | … |
| 4 | a% | 3.0 | 0.8 | 55.7 | 66.0 | 61.4 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | a为电池的负极 | |
| B. | 电池充电时a极反应为:Li1-xMn2O4+xe-+xLi+═LiMn2O4 | |
| C. | 充电时,a极锂的化合价发生变化 | |
| D. | 放电时,溶液中SO42-从a向b迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在蒸馏水中滴加浓硫酸,KW不变 | |
| B. | 在硫化钠稀溶液中,c(H+)═c(OH-)-2c(H2S)-c(HS-) | |
| C. | 氯化钠溶液和醋酸铵溶液均显中性,但两溶液中水的电离程度不相同 | |
| D. | pH=1的强酸溶液加水稀释后,溶液中各离子浓度均减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1 mol任何物质的体积都约为22.4 L | |
| B. | 标准状况下,18g H2O所占的体积约为22.4 L | |
| C. | 标准状况下,1mol O2和N2的混合气体的体积约为是22.4L | |
| D. | 在同温同压下,相同体积的任何气体单质所含原子数目相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 蕴藏在海底的“可燃冰”是高压下形成的外观像冰的甲烷水合物固体.根据你所学的知识回答下列问题:
蕴藏在海底的“可燃冰”是高压下形成的外观像冰的甲烷水合物固体.根据你所学的知识回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
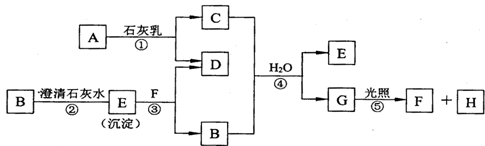
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com