
【题目】乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中正确的是( )

①分子式为C12H19O2;②不能发生银镜反应;③mol该有机物最多能与3mol氢气发生加成反应;④它的同分异构体中不可能有酚类;⑤1mol该有机物与NaOH溶液反应最多消耗1molNaOH;⑥属于芳香族化合物。
A.②④⑤B.①④⑤C.②③⑥D.②③④
【答案】A
【解析】
本题主要考查有机物的结构与性质。不存在醛基,不能发生银镜反应,不饱和度仅有三个酚类至少有四个不饱和度,能与氢氧化钠反应的官能团只有酯基。据此回答。
①由结构简式可知分子中含有12个C原子,20个H原子,2个O原子,则分子式为C12H20O2,故错误;
②分子中不含醛基,则不能发生银镜反应,故正确;
③只有碳碳双键能与氢气发生加成反应,1mol该有机物在一定条件下和H2反应,共消耗H2为2mol,故错误;
④分子中含有3个双键,则不饱和度为3,而酚类物质的不饱和度至少为4,则它的同分异构体中不可能有酚类,故正确;
⑤能与氢氧化钠反应的官能团只有酯基,水解生成羧基和羟基,只有羧基能与氢氧化钠反应,则1mol该有机物水解时只能消耗1mol NaOH,故正确;
⑥分子中不含苯环或稠环,则不属于芳香族化合物,故错误。
故选A。


科目:高中化学 来源: 题型:
【题目】根据题意,完成下列问题。
(1)常温下,将1 mL pH=1的H2SO4溶液加水稀释到100 mL,稀释后的溶液pH=_____。
(2)某温度时,测得0.01 mol·L-1的NaOH溶液的pH为11,则该温度下水的离子积常数Kw=______。该温度__________25℃(填“高于”、“低于”或“等于”)。
(3)常温下,设pH=5的H2SO4的溶液中由水电离出的H+浓度为c1;pH=9的Ba(OH)2溶液中由水电离出的H+浓度为c2,则c1/ c2=__________。
(4)常温下,pH=13的Ba(OH)2溶液aL与pH=3的H2SO4溶液bL混合(混合后溶液体积变化忽略不计)。
若所得混合溶液呈中性,则a∶b=__________。若所得混合溶液pH=12,则a∶b=__________。
(5)向明矾溶液中逐渐加入Ba(OH)2溶液至硫酸根离子刚好沉淀完全时,溶液的pH______7(填>,<,=),离子反应总方程式为______________________。
(6)用实验确定某酸HA是弱电解质。两同学的方案是:
甲:a.称取一定质量的HA配制成0.1molL-1的溶液100mL;
b.用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:a.用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各 100mL;
b.分别取这两种溶液各10mL,加水稀释为100mL;
c.各取相同体积的两种稀释液装入两个试管中,同时加入纯度相同的锌粒,观察反应现象,即可证明HA是弱电解质。
①在两个方案的第①步中,都要用到的定量仪器是_______。
②甲方案中,说明HA是弱电解质的理由是测得溶液的pH____1(选填“>”、“<”或“=”)。
乙方案中,说明HA是弱电解质的现象是_______(多选扣分)。
A.装HCl溶液的试管中放出H2的速率快
B.装HA溶液的试管中放出H2的速率快
C.两个试管中生成气体的速率一样快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池构造如图所示,下列叙述正确的是( )

A. 在外电路中,电子由银电极流向铜电极
B. 取出盐桥后,电流表的指针仍发生偏转
C. 外电路中每通过0.1 mol电子,铜的质量理论上减小6.4 g
D. 原电池的总反应式为Cu+2AgNO3===2Ag+Cu(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石墨烯具有原子级的厚度、优异的电学性能、出色的化学稳定性和热力学稳定性。制备石墨烯方法有石墨剥离法、化学气相沉积法等。石墨烯的球棍模型及分子结构示意图如下:

(1)下列有关石墨烯说法正确的是________。
A.石墨烯的结构与金刚石相似
B.石墨烯分子中所有原子可以处于同一平面
C.12 g石墨烯含σ键数为NA
D.从石墨剥离得石墨烯需克服石墨层与层之间的分子间作用力
(2)化学气相沉积法是获得大量石墨烯的有效方法之一,催化剂为金、铜、钴等金属或合金,含碳源可以是甲烷、乙炔、苯、乙醇或酞菁等中的一种或任意组合。
①钴原子在基态时,核外电子排布式为________。
②乙醇沸点比氯乙烷高,主要原因是_______________________。
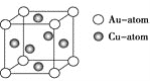
③下图是金与铜形成的金属互化物合金,它的化学式可表示为:________。
④含碳原子且属于非极性分子的是________;
a.甲烷 b.乙炔 c.苯 d.乙醇
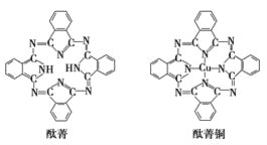
⑤酞菁与酞菁铜染料分子结构如下图,酞菁分子中氮原子采用的杂化方式有:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中横坐标表示完全燃烧时耗用可燃气体X(X=A、B、C)的物质的量n(x)。纵坐标表示消耗O2的物质的量n(O2),A、B是两种可燃气体,C是A和B的混合气体,则C中n(A)∶n(B)为 ( )

A. 2∶1 B. 1∶2 C. 1∶1 D. 任意比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知前四周期六种元素A、B、C、D、E、F的原子序数之和为107,且它们的核电荷数依次增大。B原子的p轨道半充满,其氢化物沸点是同族元素中最低的,D原子得到一个电子后3p轨道全充满,A与C能形成A2C型离子化和物,其中的阴、阳离子相差一个电子层,E4+离子和氩原子的核外电子排布相同。请回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序是____________(填元素符号)
(2)化合物BD3的分子空间构型可描述为_________,B的原子轨道杂化类型为________。
(3)已知F元素在人体内含量偏低时,会影响O2在体内的正常运输。已知F2+与KCN溶液反应得F(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物。则F的基态原子价电子排布式为______。CN-与___________(一种分子)互为等电子体,则1个CN-中π键数目为___________。
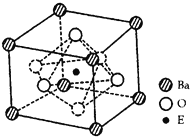
(4)EO2与碳酸钡在熔融状态下反应,所得晶体的晶胞结构如图所示,则该反应的化学方程式为________
在该晶体中,E4+的氧配为数为____________。若该晶胞边长为a nm可 计算该晶体的密度为__________g/cm3(阿伏加德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A.pH=l的溶液中:Ba2+、Fe3+、Cl-、SCN-
B.能使酚酞变红的溶液:Ca2+、K+、HCO3-、CO32-
C.![]() =10-12的溶液中:NH4+、Cu2+、NO3-、SO42-
=10-12的溶液中:NH4+、Cu2+、NO3-、SO42-
D.由水电离的c(H+)=10-12mol·L-1的溶液中:Na+、Al3+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量。请填写下列空白:
(1)移取10.00mL密度为ρg/mL的过氧化氢溶液至250mL容量瓶中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下。2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑
(3)滴定时,将高锰酸钾标准溶液注入___(填“酸式”或“碱式”)滴定管中,滴定到终点。
(4)重复滴定三次,平均耗用cmol/LKMnO4标准溶液VmL,则原过氧化氢溶液中过氧化氢的质量分数为___。
(5)若滴定前仰视滴定管读数,滴定后平视,则测定结果___(填“偏高”、“偏低”或“不影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是
A. CaCO3+2HCl=CaCl2+CO2↑+ H2O
B. CaO+H2O=Ca(OH)2
C. 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
D. CaCO3![]() CaO+CO2↑
CaO+CO2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com