
����Ŀ��������ѧ֪ʶ��ա�
��1������������������Թ��ɣ������������������ᰴ��������������һ�飬������������ �� ������ű�ʾ��
��H3PO4 ��HClO ��H3BO3 ��HNO2
��2�����龧��ľ����ṹ��ɱ����ƣ�����һ��������ӽ������ڵļ������������
��3�����������Ӻ�δ�ɶԵ���Խ�࣬�����Խ�ż�¼����Խ�ã�������������V2O5��CrO2�У��ʺ���¼�����ŷ�ԭ�ϵ��� ��
��4��SiC��������ʯ�Ľṹ���ƣ�����Cԭ�Ӻ�Siԭ�ӵ�λ���ǽ���ģ���SiC����С�Ļ�������ԭ�ӣ�SiC����ʯ��ȣ��۵�ϸߣ�
ԭ���� ��
��5��������ľ����ṹ��ͼ����ԭ�ӵĿռ�������Ϊ �� ��֪�������ܶ���dg/cm3 �� �����ӵ�����ΪNA �� ����ԭ�ӵİ뾶��cm�� 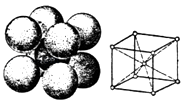
���𰸡�
��1���٣��ܣ��ڣ���
��2��12
��3��CrO2
��4��6�����ʯ�����߶���ԭ�Ӿ��壬C��C�����̣����ܴ����Խ��ʯ�۵����̼����
��5��68%��![]()
![]()
���������⣺��1.����H3PO4��д�ɣ�HO��3PO��n=1����HClO��д�ɣ�HO��1Cl��n=0����H3BO3��д�ɣ�HO��1B��n=0����HNO2��д�ɣ�HO��NO��n=1������H3PO4��HNO2���������HClO��H3BO3������������Դ��ǣ��٣��ܣ��ڣ��ۣ�
��2.�����龧���ṹ�����������ṹ����һ��������ӽ������ڵļ�����Ӹ���=3��8��2=12�����Դ��ǣ�12��
��3.��V2O5��V����������ȫ��ʧȥ��ɼ���CrO2��Crʧȥ4�����ӣ����ӵ���������Ϊ2��Ϊ�ɶԣ����Ӻ�δ�ɶԵ���Խ�࣬�����Խ�����ʺ���¼�����ŷ�ԭ�ϵ���CrO2 �� ���Դ��ǣ�CrO2��
��4.�����������С��Ϊ��Ԫ��������6��ԭ�ӣ�SiC��辧�����ƣ����Ҳ����6��ԭ�ӣ����߶���ԭ�Ӿ��壬�ṹ��������ƣ�Si��C��������C��C������C��Si����С�����Խ��ʯ������۷е����̼���裬���Դ��ǣ�6�����ʯ�����߶���ԭ�Ӿ��壬C��C�����̣����ܴ����Խ��ʯ�۵����̼���裻
��5.����������λ�ھ����Ķ�������ģ�����ƽ������8�� ![]() +1=2����ԭ�ӣ��辧���߳�Ϊx������ԭ�Ӱ뾶Ϊ
+1=2����ԭ�ӣ��辧���߳�Ϊx������ԭ�Ӱ뾶Ϊ ![]() x����ռ�������Ϊ
x����ռ�������Ϊ ![]() ��100%=
��100%= ![]() ��100%=68%�����������ܶ�Ϊdgcm��3 �� �������ԭ��������56������d=
��100%=68%�����������ܶ�Ϊdgcm��3 �� �������ԭ��������56������d= ![]() ��x=
��x= ![]() cm��������ԭ��Ϊ
cm��������ԭ��Ϊ ![]()
![]() cm�����Դ��ǣ�68%��
cm�����Դ��ǣ�68%�� ![]()
![]() ��
��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ����֤��̼�ķǽ����Աȹ�ǿ���ǣ� ��
����Na2SiO3��Һ��ͨ��CO2������ɫ����
��ʯī�ǵ��壬������ǰ뵼��
���Ʋ��������з�����ӦNa2CO3+SiO2 ![]() Na2SiO3+CO2��
Na2SiO3+CO2��
��CH4��SiH4�ȶ���
A.�٢�
B.�ڢ�
C.�ۢ�
D.�٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�Al��NO3��3��Һ��������ȷ���ǣ� ��
A.����Һ��H+��Fe2+��SO ![]() ��Cl�����Դ�������
��Cl�����Դ�������
B.�����Һ��ͨ��SO2���岻�ᷢ����Ӧ
C.�����Һ�м��������ˮ������Ӧ�����ӷ���ʽAl3++4NH3?H2O�TAlO2��+4NH4++2H2O��
D.�����Һ�е���Na2CO3��Һ������Ӧ�����ӷ���ʽ��2Al3++3CO ![]() +3 H2O�T2Al��OH��3��+3CO2��
+3 H2O�T2Al��OH��3��+3CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС��ģ�ҵ��Ư�ۣ����������ͼ��ʵ��װ�á���֪���������ͼӦ�ų���������6Cl2+6Ca(OH)2![]() 5CaCl2+Ca(ClO3)2+6H2O��
5CaCl2+Ca(ClO3)2+6H2O��
�ش��������⣺
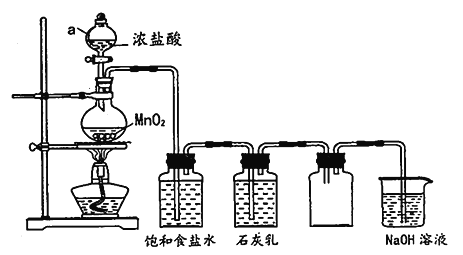
��1����װ��������a��������_____________________��
��2��װ�����б���ʳ��ˮ��������_____________________��
��3������ȡƯ�۵Ļ�ѧ����ʽ��______________________________��
�ڸ�С���Ƶõ�Ư����n(CaCl2)Զ����n[Ca(ClO)2]��������л����������ʵĻ�ѧʽ��______��
��Ϊ���Ca(ClO)2�ĺ���,���ɲ�ȡ�Ĵ�ʩ��__________________����дһ�ּ��ɣ���
��4��Ư��Ӧ�ܷⱣ�棬ԭ����______________���û�ѧ����ʽ��ʾ����
��5����ͥ�г���84 ����Һ����Ҫ�ɷ�NaClO��������飨��Ҫ�ɷ����ᣩ�������������ͬʱ���ʹ�û�����ж���������д���÷�Ӧ�����ӷ���ʽ________________________________��
��6��ʵ������MnO2��Ũ���ᷴӦʱ��������Ũ�ȵ���8mol/Lʱ�Ͳ�������������ij��ȤС����Բ����ƿ��ʵ�ʼ�����MnO28.7g��20mL36.5%��Ũ����(�ܶ�1.18g/mL)����ַ�Ӧ������ܹ��ռ���_______L��״���µ�����������3λ��Ч���֣������Ƿ�Ӧ��������Һ����仯����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¹���ѧ�ҹ�����1902 �꿪ʼ�о��ɵ���������ֱ�Ӻϳɰ�����Ӧԭ��Ϊ��N2(g)+3H2(g)![]() 2NH3(g) ��H=-92.4kJmol-1
2NH3(g) ��H=-92.4kJmol-1
��1���ں��º��������£���Ӧƽ����ϵ�г��뵪�����ﵽ��ƽ��ʱ��c(H2)��_________(����������������С�������������������ж�������ͬ)��c(N2)��c3(H2)��___________��
��2����ҵ�Ͽ���CH4��ˮ������������CH4(g)+H2O(g)![]() CO(g)+3H2(g)����200��ʱ2L���ܱ������У���1molCH4��1mol H2O(g)��ϣ���ƽ��ʱCH4 ��ת����Ϊ80%����200��ʱ�÷�Ӧ��ƽ�ⳣ��K=______________������һλС������
CO(g)+3H2(g)����200��ʱ2L���ܱ������У���1molCH4��1mol H2O(g)��ϣ���ƽ��ʱCH4 ��ת����Ϊ80%����200��ʱ�÷�Ӧ��ƽ�ⳣ��K=______________������һλС������
��3����ͼΪ�ϳɰ���Ӧ�ڲ�ͬ�¶Ⱥ�ѹǿ��ʹ����ͬ���������£���ʼʱ�����������������Ϊ1:3 ʱ��ƽ�������а���������������ֱ���vA(NH3)��vB(NH3)��ʾ�ӷ�Ӧ��ʼ����ƽ��״̬A��B ʱ�Ļ�ѧ��Ӧ���ʣ���vA(NH3)____ ( ����>����<������=��)vB(NH3)��

��4����ҵ�������ݳ��İ�����ϡ�������ա���ǡ������NH4HSO4������Һ�и����ӵ����ʵ���Ũ���ɴ�С��˳����______________________��
��5��H2NCOONH4�ǹ�ҵ�ϳ����ص��м����÷�Ӧ�������仯��ͼ��ʾ����CO2�Ͱ��ϳ����ص��Ȼ�ѧ����ʽΪ_________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����FeCl3��Һʴ��ͭ�������·��Ĺ����У���Һ������Fe2+��Fe3+��Cu2+����������Դ���պ������壮�������洦���������ش��������⣺

��1���Լ�2��_____������B��_____��ͨ��������C��_________�����ѧʽ��
��2��д�������Լ�1������Ӧ�����ӷ���ʽ��__________��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͬ�����Ķ������������������˵�����й�ϵ��ȷ���ǣ� ��
A. ����ԭ�ӵĸ�����Ϊ2��3 B. ����Ԫ�ص���������5��4
C. ����Ԫ�ص�������Ϊ5��4 D. ����ԭ�ӵĸ�����Ϊ1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣��������е���ĸ�ֱ����ijһ��ѧԪ�ء�
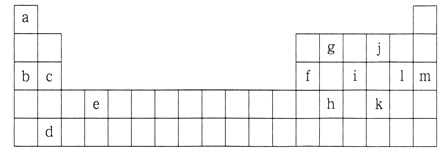
��1����������Ԫ����:
���ڶ�����Ԫ�ص���__________����������Ԫ�ص���_________��eԪ����Ԫ�����ڱ��е�λ����________���ڣ�_______�塣
��2������___________��Ԫ�صĵ��ʿ��ܶ��ǵ�������塣
A.b,c,i B.a,g,k C.c,g,l D.d,e,f
��3����Ԫ��a,b,c,f,1��ԭ�Ӱ뾶����С�����˳������:________
��4�� iԪ������_________(���������������ǽ�����)Ԫ��,��������ϼ���________����ͻ��ϼ���________��������������Ӧ������һ����ˮ�Ժ�ǿ�����ʣ�����������ʵ�����ﳣ�����������д��i�ĵ�����������Ӧ�Ļ�ѧ����ʽ:_____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A���ܵ����H+ �Ļ����������
B��ʵ����1molij�������Ϊ22.4 L���ⶨ����һ���DZ�״��
C��Ħ�����߸�����������֮һ
D���������Ϊ�ᡢ��κ�������������״���෨�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com