
| A、生铁是铁碳混合物,钢是纯铁、纯净物 |
| B、钢的性能不如生铁优越,使用范围不如生铁广 |
| C、生铁和钢是含碳量不同的两种铁碳的合金 |
| D、生铁和钢的主要成分都是铁,性能相近 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用加热法可除去Na2CO3中的NaHCO3 |
| B、Na2CO3的热稳定性大于NaHCO3 |
| C、可用石灰水区分Na2CO3与NaHCO3溶液 |
| D、小苏打可中和胃酸、热纯碱可除去油污 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、放电时正极附近溶液的碱性增强 |
| B、放电时每转移3 mol电子,正极有1mol K2FeO4被还原 |
| C、充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O |
| D、充电时锌极与外电源正极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验示意图 | 实验现象 | 解释 |
甲: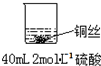 | 无明显现象 | |
乙: | 稀硝酸是氧化性的酸,能与铜发生反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O |
| 22 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、云、烟、雾等均能产生丁达尔现象 |
| B、开发氢能、太阳能、风能、生物质能等新型能源是践行低碳生活的有效途径 |
| C、“光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关 |
| D、用脱硫处理的煤代替原煤做燃料可以有效减少空气中CO2气体的含量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碱 纯碱 NaOH |
| B、酸性氧化物 干冰 CO |
| C、酸 硫酸 H2S |
| D、盐 纯碱 Na2CO32 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com