
�������л������NaCl����NaOH����HCl����NH4Cl����CH3COONa����CH3COOH����NH3��H2O����H2O���ش����⣺
��1��NH4Cl��Һ��________�ԣ������ӷ���ʽ��ʾ___________ _____________��
��2����֪ˮ�д�������ƽ�⣺H2O��H2O H
H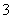 O��OH������H>0������ʹƽ�������ƶ�����������Һ�����ԣ�ѡ��ķ�����________��
O��OH������H>0������ʹƽ�������ƶ�����������Һ�����ԣ�ѡ��ķ�����________��
A����ˮ�м���NaHSO4���� B����ˮ�м���Na2CO3����
C��������100 �� D����ˮ�м���(NH4)2SO4����
��3������pH��������Ģ�(NaOH)�͢�(��ˮ)�ֱ��ˮϡ��m����n����ϡ�ͺ�pH��ȣ���m________n(�>����<������)��
��4��pH��12��NaOH��Һ100mL��Ҫʹ����pHΪ11��������仯���Բ��ƣ�
�����������ˮ��Ӧ��_________mL���������pH��10��NaOH��Һ��Ӧ��_________mL��
�����0.01mol/L HCl��Ӧ��_________mL��
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����йص�������ȷ���ǣ� ��
A��HClO�����ᣬ����NaClO���������
B�����ˮ����μ�����������FeCl3��Һ�����Ƶ�Fe(OH)3����
C�����ݷ�ɢ�����ӵ�ֱ����С����ɢϵ�ɷ�Ϊ��Һ����Һ�ͽ��壬��Һ�ķ�ɢ�����Ӵ�С������Һ�뽺��֮��
D����ѪҺ����ԭ���뽺���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NAΪ�����ӵ���������ֵ������˵����ȷ����
A.18gH2O����10 NA������ B.1mol���麬��18NA����ѧ��
C. 22.4L��ˮ����NA��NH3���� D.56g��ƬͶ������ŨH2SO4������NA��SO2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�Թ�ҵ��ˮ��������ˮ���д����Ƿ�ֹˮ����Ⱦ������ˮ�ʵ���Ҫ��ʩ��
��1�������ˮ�е�CN���о綾��
��CN����CԪ����+2�ۣ� NԪ����-3�ۣ���ԭ�ӽṹ����NԪ���Ը��۵�ԭ����
�����õ��Ӷ�ƫ��Nԭ�ӣ�NԪ���Ը��ۡ�
��������������£�CN���ܹ�������������HCO3-��ͬʱ����NH3���÷�Ӧ�����ӷ���ʽΪ ��
��2���������ƺͶ��ȷӣ�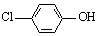 ���ķ�ˮ�������������س�ȥ����ԭ������ͼ��ʾ��
���ķ�ˮ�������������س�ȥ����ԭ������ͼ��ʾ��
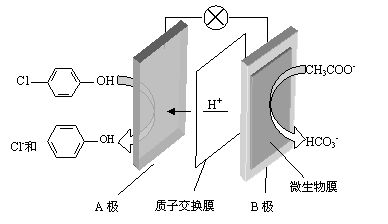
��B�ǵ�ص� �����������������
��A���ĵ缫��ӦʽΪ ��
|
 |  | ||||
 |
 |
�� �����ĵ缫��ӦʽΪ ��
�� ����Ũ�����еõ�Ũ�����ԭ���� ��
�� �������У���ȡһ���Ĵ�ʩ�ɿ��������ҵ�pHԼΪ6-8����ʱ����Ũ���ҵ�OH-�ɺ��Բ��ơ�400mL 10 g?L-1������Һͨ��һ��ʱ���Ũ������Ϊ145 g?L-1����Һ����仯���Բ��ƣ��������ϲ�����H2�ڱ�״���µ����ԼΪ L���������Ħ������Ϊ90 g? mol-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ijѧ���ü�ʽ�ζ�����ȡ0.1mol/L��NaOH��Һ����ʼʱ����Һ�棬����Ϊ11.00mL��ȡ��������Һ����Һ�棬����Ϊ19. 00mL��ʵ��ȡ��Һ��������
A������8.00mL B��С��8.00mL C������8. 00mL D����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з�Ӧ����������ԭ��Ӧ����( )
A.CaO��H2O==Ca(OH)2 B.Fe2O3��3CO 2Fe��3CO2
2Fe��3CO2
C.CaCO3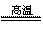 CaO��CO2�� D.CO2��2NaOH==Na2CO3��H2O
CaO��CO2�� D.CO2��2NaOH==Na2CO3��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������CCl4��ȡ��ˮ��˵��������ȷ����( )
A.����CCl4�е��ܽ�ȴ�����ˮ�е��ܽ�� B.��ȡ���ϲ���ɫ��dz
C.��ȡ��CCl4��Һ��Ϊ�Ϻ�ɫ D.�þƾ�Ҳ����ȡ��ˮ�еĵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й�˵����ȷ���� (����)
A����ӦNH3(g)+HCl(g)= NH4Cl(s)�������¿��Է����У���÷�Ӧ�ġ�H<0
B�����������Ͷ�п���Ʋ�����ʱ�����߸��ױ���ʴ
C��CH3COOH��Һ��ˮϡ�ͺ���ƽ�������ƶ�����Һ�е�c(CH3COO-)����
D��Na2CO3��Һ�м�������Ca(OH)2���壬CO32��ˮ��̶ȼ�С����Һ��pH��С
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com