
�Թ�ҵ��ˮ��������ˮ���д����Ƿ�ֹˮ����Ⱦ������ˮ�ʵ���Ҫ��ʩ��
��1�������ˮ�е�CN���о綾��
��CN����CԪ����+2�ۣ� NԪ����-3�ۣ���ԭ�ӽṹ����NԪ���Ը��۵�ԭ����
�����õ��Ӷ�ƫ��Nԭ�ӣ�NԪ���Ը��ۡ�
��������������£�CN���ܹ�������������HCO3-��ͬʱ����NH3���÷�Ӧ�����ӷ���ʽΪ ��
��2���������ƺͶ��ȷӣ�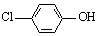 ���ķ�ˮ�������������س�ȥ����ԭ������ͼ��ʾ��
���ķ�ˮ�������������س�ȥ����ԭ������ͼ��ʾ��
��B�ǵ�ص� �����������������
��A���ĵ缫��ӦʽΪ ��
|
 |  | ||||
 |
 |
�� �����ĵ缫��ӦʽΪ ��
�� ����Ũ�����еõ�Ũ�����ԭ���� ��
�� �������У���ȡһ���Ĵ�ʩ�ɿ��������ҵ�pHԼΪ6-8����ʱ����Ũ���ҵ�OH-�ɺ��Բ��ơ�400mL 10 g?L-1������Һͨ��һ��ʱ���Ũ������Ϊ145 g?L-1����Һ����仯���Բ��ƣ��������ϲ�����H2�ڱ�״���µ����ԼΪ L���������Ħ������Ϊ90 g? mol-1��
��1����C��N��ԭ�ӵ��Ӳ�����ͬ���˵����CС��N������������CС��N��ԭ�Ӱ뾶C����N���õ�������C����N
�� 2CN��+ 4H2O + O2  2HCO3�� + 2NH3
2HCO3�� + 2NH3
��2���ٸ����� Cl�� ��OH + e�� + H+ ===
��OH + e�� + H+ ===  ��OH + Cl��
��OH + Cl��
��3����4OH����4e��=== 2H2O+O2��
�� ����OH-�ŵ磬c(H+)����H+������ͨ�������ӽ���Ĥ����Ũ���ң�
A��ͨ�������ӽ���Ĥ����������Ũ���ң�H+ +A�� === HA������Ũ������
�� 6.72



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
300mLijŨ�ȵ�NaOH��Һ�к���60g���ʣ���������1mol/L NaOH��Һ��Ӧȡԭ��Һ������ˮ�������ԼΪ( )
A��1��4���������£�1��5���������ã�2��1 �����������ģ�2��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1���£�N2H4���Ƿ��亽��ɴ����õĸ���ȼ�ϣ���NH3��NaClO��һ�����ʵ����Ȼ�Ϸ�Ӧ�������¡�NaCl��ˮ���÷�Ӧ�Ļ�ѧ����ʽ�ǡ�2NH3+NaClO=N2H4+NaCl+H2O����
��2���ڻ���ƽ�����װ��ǿ��ԭ���£�N2H4����ǿ�������������⣬�����ǻ��ʱ���������������壬���ų������ȣ���֪��H2O��l�� H2O��g����H=+44kJ/mol��12.8gҺ̬���������������ⷴӦ���ɵ�����ˮ�������ų�256.65kJ��������
����д��Һ̬����������ⷴӦ����Һ̬ˮ���Ȼ�ѧ����ʽ������
����16g Һ̬���������������ⷴӦ����Һ̬ˮʱ�ų��������ǡ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
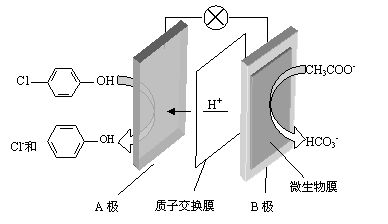
������CO2ͨ��KOH��Ca(OH)2�Ļ��ϡ��Һ�У����ɳ��������ʵ���(n)��ͨ��
CO2���(y)�Ĺ�ϵ��ȷ����
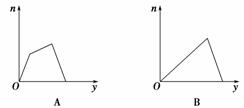 | |||
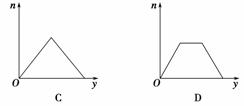 | |||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪����Cl2ͨ������KOH��Һ�������п�����KC1��KClO��KClO3���� ��ֵ���¶ȸߵ��йء���n(KOH) = a molʱ�������й�˵���������
A.�μӷ�Ӧ�����������ʵ�������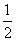 a mol
a mol
 B.��ij�¶��£���Ӧ�� =11������Һ�� =
B.��ij�¶��£���Ӧ�� =11������Һ�� = 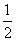
C. �ı��¶ȣ�������KC1O3��������۲���Ϊ 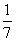 a mol
a mol
D.�ı��¶ȣ���Ӧ��ת�Ƶ��ӵ����ʵ���ne�ķ�Χ��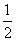 a mol �� ne ��
a mol �� ne �� 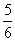 a mol
a mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���Խ���ӦZn+Br2 = ZnBr2��Ƴ����أ�����4���缫��Ӧ
��Br2 + 2e�� = 2Br- ����2Br- - 2e�� = Br2 ����Zn �C 2e�� = Zn2+�� ��Zn2+ + 2e�� = Zn
�� ���б�ʾ���ʱ��������Ӧ�ͷŵ�ʱ�ĸ�����Ӧ�ķֱ���
�� A���ںۡ͢��� �� B���ں͢� ����C���ۺ͢١������� D���ܺ͢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������л������NaCl����NaOH����HCl����NH4Cl����CH3COONa����CH3COOH����NH3��H2O����H2O���ش����⣺
��1��NH4Cl��Һ��________�ԣ������ӷ���ʽ��ʾ___________ _____________��
��2����֪ˮ�д�������ƽ�⣺H2O��H2O H
H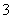 O��OH������H>0������ʹƽ�������ƶ�����������Һ�����ԣ�ѡ��ķ�����________��
O��OH������H>0������ʹƽ�������ƶ�����������Һ�����ԣ�ѡ��ķ�����________��
A����ˮ�м���NaHSO4���� B����ˮ�м���Na2CO3����
C��������100 �� D����ˮ�м���(NH4)2SO4����
��3������pH��������Ģ�(NaOH)�͢�(��ˮ)�ֱ��ˮϡ��m����n����ϡ�ͺ�pH��ȣ���m________n(�>����<������)��
��4��pH��12��NaOH��Һ100mL��Ҫʹ����pHΪ11��������仯���Բ��ƣ�
�����������ˮ��Ӧ��_________mL���������pH��10��NaOH��Һ��Ӧ��_________mL��
�����0.01mol/L HCl��Ӧ��_________mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������£���������������ԭ����һ����ȵ���( )
A.ͬ��������ͬ�ܶȵ�N2��CO B.ͬ�¶ȡ�ͬ�����H2��N2
C.ͬ�����ͬ�ܶȵ�C2H6��NO D.ͬѹǿ��ͬ�����N2O��CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ�鷽���У����ܲⶨNa2CO3��NaHCO3������� Na2CO3������������
Na2CO3������������
A��ȡa�˻�����ּ��ȣ�����b��
B��ȡa�˻����������ϡ�����ַ�Ӧ�����ȡ����ɡ����գ���b�˹���
C��ȡa�˻����������ϡ�����ַ�Ӧ���ݳ������ü�ʯ�����գ�����b��
D��ȡa�˻����������Ba(OH)2��Һ��ַ�Ӧ�����ˡ�ϴ�ӡ���ɣ���b�˹���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com