
| A.碱金属元素中,金属活泼性最强的是Li |
| B.第三周期元素中,原子半径最大的是Cl |
| C.短周期元素最高价氧化物对应的水化物中,酸性最强的是H2SO4 |
| D.原子序数为11与9的元素能够形成离子化合物,该化合物中存在离子键 |
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.X>Y>Z>W | B.Y>X>W>Z | C.Z>Y>X>W | D.Y>X>Z>W |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.第IA族元素铯的两种同位素137Cs比133Cs多4个质子 |
| B.元素周期表有十八个纵行,共十六个族 |
| C.第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强 |
| D.同主族元素从上到下,单质的熔点逐渐降低 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.最高正化合价数值逐渐增大 | B.原子半径逐渐减小 |
| C.电子层数逐渐增多 | D.从硅到氯,最低负化合价从-4到-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.b=a-n+m | B.b=a-n-m |
| C.离子半径Xm+<Yn+ | D.原子半径X<Y |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | | | E | | | F | | |
| 三 | A | C | D | | | | G | R |
| 四 | B | | | | | | H | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
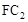 气体有毒,排放到大气中易形成酸雨,写出
气体有毒,排放到大气中易形成酸雨,写出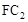 与氧气和水蒸气反应的化学方程式 。
与氧气和水蒸气反应的化学方程式 。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com