
四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
| 元素 | A | B | C | D |
| 性质结构信息 | 原子中最外层电子数为电子层数的2倍。常温下为淡黄色固体,其燃烧热为Q KJ/mol | 单质常温、常压下是气体,能溶于水。原子的M层p轨道有1个未成对的电子 | 单质质软、银白色固体、导电性强。单质在空气中燃烧发出黄色的火焰。 | 原子最外层电子层上s电子数等于p电子数。单质是一种重要的半导体材料。 |
(1)S(s) + O2(g) = SO2(g) △H="-Q" KJ/mol
(2)Cl2 + H2O ="HCl" + HClO
(3)2Cl- + 2H2O Cl2 ↑+H2 ↑+2OH-
Cl2 ↑+H2 ↑+2OH-
(4)离子键
(5)Si S Cl
(6)Si, 取高氯酸溶液少量加入硅酸钠溶液中,若有白色沉淀生成,证明高氯酸酸性强于硅酸,(合理即可)
解析试题分析:(1)A原子中最外层电子数为电子层数的2倍,则该原子的最外层有4个或6个电子,且常温下为淡黄色固体,所以A为硫元素,则A燃烧的热化学方程式为S(s)+O2(g)=SO2(g) △H="-Q" KJ/mol
(2)B原子的M层p轨道有1个未成对的电子且常温下是气体,则B为氯元素,氯气与水反应的化学方程式为Cl2 + H2O ="HCl" + HclO
(3)C单质在空气中燃烧发出黄色的火焰。则C为钠,电解氯化钠溶液的离子方程式为2Cl- + 2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
(4)A与C形成的化合物即硫化钠,该化合物中只存在离子键
(5)原子最外层电子层上s电子数等于p电子数。单质是一种重要的半导体材料。则D为硅元素,根据同周期元素的电负性随核电荷数增加而增强,所以S、Cl、Si三种元素的电负性由小到大的顺序为Si、S、Cl
(6)Cl、Si中非金属性较弱的是Si,只要证明HClO4酸性大于H2SiO3酸性即可。取高氯酸溶液少量加入硅酸钠溶液中,若有白色沉淀生成,证明高氯酸酸性强于硅酸,
考点:考查元素推断、方程式的书写、化学键的判断、非金属性、电负性强弱的比较


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:填空题
短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5,X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和,Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X元素形成氢化物和最高价氧化物的水化物能发生反应。请回答:
(1)X元素在周期表中的位置 ,X元素形成氢化物和最高价氧化物的水化物能发生反应的化学方程式 。
(2)Y的最高价氧化物的结构式是 。
(3)XZ3实验室制法的化学方程式为 。
(4)Z的简单氧化物属于 晶体。(填“分子”或“原子”)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D、E、F六种短周期元素的原子序数依次增大。A、D同族,B、C同周期;B原子最外层电子数是次外层的两倍;在周期表中A的原子半径最小;C是地壳中含量最多的元素,C是F不同周期的邻族元素;E和F的原子序数之和为30。由上述六种元素中的几种元素组成的甲、乙、丙、丁、戊、己六种化合物如下表所示:
元素形成的化合物
| 化合物 | 甲 | 乙 | 丙 |
| 各元素原子 个数比 | N(A):N(C) =2:1 | N(A):N(C) =1:1 | N(B):N(A) =1:4 |
| 化合物 | 丁 | 戊 | 己 |
| 各元素原子 个数比 | N(D):N(B):N(C) =2:1:3 | N(E):N(F) =1:3 | N(B):N(F) =1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物。
(1)①H、C、N、0四种元素的电负性由小到大的顺序为_____________________。
②下列叙述不正确的是_____________。(填字母)
A.因为HCHO与水分子间能形成氢键,所以HCHO易溶于水
B.HCHO和CO2分子中的中心原子均采用 杂化
杂化
C.C6H6分子中含有6个 键和1个大
键和1个大 键,C2H2是非极性分子
键,C2H2是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是__________。
②六氰合亚铁离子[Fe(CN)6] 中不存在______________________________________。
中不存在______________________________________。
A.共价键 B.非极性键 C.配位键 D. 键 E.
键 E. 键
键
写出一种与CN-互为等电子体粒子的分子式_____________________。
(3) SO3分子的立体构型为_____________,SeO32-的立体构型为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
按照下列元素基态原子的电子排布特征判断元素,并回答问题:A原子中只有一个电子层且只含有一个电子;B原子的3p轨道上得到一个电子后不能再容纳外来电子;C原子的2p轨道上有一个电子的自旋方向与2p轨道上其他电子的自旋方向相反;D原子的第三电子层上有8个电子,第四层上只有1个电子;E原子的价电子排布式为3s23p6。
(1)A~E分别是哪种元素(用元素符号填空):
A:__________;B:________;C:__________;D:________;E:________。
(2)E的原子结构示意图________________。
(3)C的轨道表示式____________________。
(4)B原子的核外电子排布式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X、Y、Z、W、T是元素周期表中前四周期的五种元素。有关这五种元素的信息如下表:
| 元素代号 | 相关信息 |
| X | 它的一种核素的原子核内没有中子 |
| Y | 能组成很多种性质不同的单质,也是形成化合物种类最多的一种元素 |
| Z | 基态原子的最外层电子排布式为nsnnpn+1 |
| W | 与钠元素能组成两种化合物,这些化合物与水反应均生成碱;大气平流层中W3被誉为地球生物“保护伞” |
| T | 主要化合价有+1和+2价,其二价离子在水溶液中呈蓝色 |
 YZ- (aq)+X3W+(aq) ΔH="+45.6" KJ/mol
YZ- (aq)+X3W+(aq) ΔH="+45.6" KJ/mol查看答案和解析>>
科目:高中化学 来源: 题型:填空题
制冷剂是一种易被压缩、液化的气体,液化后在管内循环,蒸发时吸收热量,使环境温度降低,达到制冷的目的。人们曾采用乙醚、NH3、CH3Cl等作制冷制,但它们不是有毒就是易燃,于是科学家根据元素性质的递变规律来开发新的制冷剂。根据已有知识,某些元素化合物的易燃性、毒性变化趋势如下:
(1)氢化物的易燃性:
SiH4>PH3>H2S>HCl,则________>________>H2O>HF(填物质的化学式)。
(2)化合物的毒性:
PH3>NH3,CCl4>CF4,则H2S________H2O,CS2________CO2(填“>”“=”或“<”)。
于是科学家们开始把注意力集中在含F、Cl的化合物上。
(3)已知CCl4的沸点为76.8 ℃,CF4的沸点为-128 ℃,新的制冷剂的沸点范围应介于二者之间,经过较长时间的反复实验,发现了制冷剂CF2Cl2(氟利昂),其他类似的制冷剂可以是________。
(4)然而这种制冷剂造成的当今某一环境问题是_____________________________。
但求助于周期表中元素及其化合物的______(填写下列选项的编号)变化趋势开发制冷剂的科学思维方法是值得借鉴的。
①毒性;②沸点;③易燃性;④水溶性;⑤颜色
| A.①②③ | B.②④⑤ | C.②③④ | D.①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
碳及其化合物应用广泛。
I.工业上利用CO和水蒸汽反应制氢气,存在以下平衡:CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
(1)沸石分子筛中含有硅元素,请写出硅原子结构示意图__________。
(2)向1L恒容密闭容器中注人CO和H2o(g),830℃时测得部分数据如下表。则该温度下反应的平衡常
数K=______________。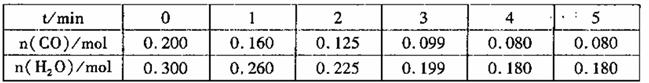
(3)相同条件下,向1L恒容密闭容器中,同时注人1mol CO、1mol H2O(g),2molCO2和2mo1 H2,此时v(正 ) __________v(逆)(填“>”“=”或“<”)
II.已知CO(g)+1/2 O2 (g)=CO2 (g) △H=一141 kJ·mol-1
2H2(g)+ O2(g)=2H2O(g) △H=一484 kJ·mol-1
CH3OH(1)+3/2O2 (g)=CO2(g)+2H2O(g) △Hl=一726 kJ·mol-1
(4)利用CO、H2化合制得液态甲醇的热化学方程式为___________。
III.一种新型氢氧燃料电池工作原理如下图所示
(5)写出电极A的电极反应式_____________。
(6)以上述电池电解饱和食盐水,若生成0.2mo1 Cl2,则至少需通人O2的体积为_____L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
短周期元素A、B、C、D在周期表中的位置如图,E2+与D的简单阴离子有相同的电子层结构,回答下列问题: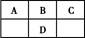
(1)设A、B、C、D四种元素的原子序数之和为m,则m 。
A.一定为奇数
B.一定为偶数
C.可能为奇数,也可能为偶数
(2)D元素原子的次外层电子数等于其他层电子数之和,则:
①写出A形成的简单离子的结构示意图 ,元素D位于元素周期表的第 族。
②A元素的一种氢化物分子中有6个原子,其结构简式为 。常压298 K时0.2 mol该气态氢化物在O2中完全燃烧,生成气态A单质和水,放出热量106.8 kJ,该气态氢化物燃烧的热化学方程式为 。
③写出C单质与B的最简单氢化物反应的化学方程式:
④实验证实AC3与水会发生反应生成HNO2和HF,则AC3和NaOH溶液反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com