
【题目】下列物质中,化学式能准确表示该物质分子组成的是( )
A. NH4ClB. SiO2C. P4D. Na2SO4
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某工厂废水中含游离态氯,通过下列实验测定其浓度。
①取水样10.00mL于锥形瓶中,加入10.00mL的KI溶液(足量),发生的反应为:Cl2+2KI=2KCl+I2,滴入指示剂2~3滴。
②取一滴定管依次用自来水、蒸馏水洗净后,马上注入0.01mol/L溶液,调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3=2NaI+2Na2S4O6。
试回答下列问题:
(1)步骤①加入的指示剂是_____________。
(2)步骤②应使用______式滴定管。
(3)判断达到滴定终点的实验现象是_____________。
(4)用0.1032mol/LHCl溶液滴定未知浓度的NaOH溶液,下列情况对实验结果无影响的是___(填标号)。
A.酸式滴定管未用标准盐酸溶液润洗
B.锥形瓶未用待测液润洗
C.滴定滴定管尖嘴中有气泡,滴定后气泡消失了
D.滴定时将标准液溅出锥形瓶外
查看答案和解析>>
科目:高中化学 来源: 题型:
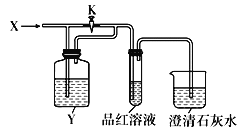
【题目】向如图所示装置中缓慢通入气体X,若打开活塞K,则品红溶液褪色;若关闭活塞K,则品红溶液无变化而澄清石灰水变浑浊。X和Y可能是
选项 | A | B | C | D |
X | SO2 | Cl2 | HCl | Cl2 |
Y | NaOH溶液 | 饱和NaHCO3溶液 | 饱和NaCl溶液 | Na2SO3溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、R、M、N为六种短周期元素,其原子半径和最外层电子数之间的关系如下图所示。
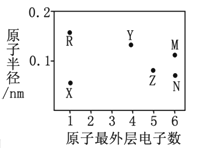
(1)M元素的原子核外有__________种能量不同的电子,有__________个未成对电子;Z元素在元素周期表中的位置是第______周期________族。
(2)N、R、X三种元素的原子可构成一种强碱性物质,该物质的电子式是_____________;Y元素的氧化物是制造光纤的主要材料,该氧化物是________晶体(填晶体类型)。
某化工生产的核心环节的反应为:2MN2(g) + N2(g) 2 MN3(g) + Q(Q>0)
(3)该反应的平衡常数表达式K=__________________________;欲使K值变大,可采取的措施是__________________________。
(4)该反应达到平衡后,在其他条件不变的情况下,若使容器的体积扩大为原来的两倍,则平衡____________________。(选填“正向移动”、“逆向移动”或“不移动”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同温度下,向2L密闭容器中加入1molNO和1mol活性炭,发生反应: ![]() H=-213.5kJ/mol,达到平衡时的数据如下:
H=-213.5kJ/mol,达到平衡时的数据如下:
温度/℃ | n(活性炭)/mol | n(CO2)/mol |
T1 | 0.70 | —— |
T2 | —— | 0.25 |
下列说法不正确的是
A. 上述信息可推知:T12
B. T1℃时,该反应的平衡常数K=9/16
C. T2℃时,若反应达平衡后再缩小容器的体积,c(N2):c(NO)不变
D. T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知淀粉酶的成分为蛋白质,可将淀粉分解为葡萄糖。分析表格,可推测( )
溶液 | 双缩脲试剂 | 碘液 | 斐林试剂 |
甲 | + | - | - |
乙 | - | ++ | - |
甲、乙混合 | + | + | + |
注:“+”显色,“++”显色更深;“-”不显色。
A. 甲溶液含有淀粉 B. 乙溶液含有还原性糖
C. 混合溶液不含淀粉 D. 混合溶液含有淀粉酶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】支撑海港码头基础的钢管柱,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是

A. 通入保护电流使钢管桩表面腐蚀电流接近于零
B. 通电后外电路电子被强制从高硅铸铁流向钢管桩
C. 高硅铸铁的作用是作为损耗阳极材料和传递电流
D. 通入的保护电流应该根据环境条件变化进行调整
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮的氧化物具有重要意义。回答下列问题:
(1)2016年10月19日“天宫二号”与“神舟十一号”顺利实现太空交会对接。运载火箭用的是一种叫肼(N2H4)的燃料和氧化剂NO2,两者反应生成氮气和气态水。
已知: N2 (g) + 2O2 (g) = 2NO2 (g) △H = +67.7 kJ·mol-1
N2 H4 (g) +O2 (g) = N2 (g) +2H2 O (g) △H =-543 kJ·mol-1
①写出肼和NO2反应的热化学方程式__________________________________。
②若已知: 2H2(g)+O2(g)=2H2O(g) ΔH1=-Q1 kJ·mol-1;
2H2(g)+O2(g)=2H2O(l) ΔH2=-Q2 kJ·mol-1,
则 Q1_________Q2(填“>”“<”或“=”)。
(2)汽车尾气净化器中发生的反应为2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。一定条件下,在三个体积均为1.0 L恒容密闭容器中发生上述反应,测得有关实验数据如下:
N2(g)+2CO2(g)。一定条件下,在三个体积均为1.0 L恒容密闭容器中发生上述反应,测得有关实验数据如下:
容器 | 温度/(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | ||||
NO | CO | N2 | CO2 | N2 | CO2 | ||
I | 400 | 0.2 | 0.2 | 0 | 0 |
| 0.12 |
II | 400 | 0.4 | 0.4 | 0 | 0 |
| x |
III | 300 | 0 | 0 | 0.1 | 0.2 | 0.075 |
|
①容器I中达到平衡所需时间2 s,则v(N2)=_______;
②x_____0.24(填“>”、“=”、“<”);△H_____0 (填“>”、“=”、“<”);
③若起始时向I中充入NO、CO各0.1 mol,N2、CO2各0.0 5 mol,开始时v(正)
___ v(逆) (填“>”、“=”、“<”)。
(3)SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
①SCR(选择性催化还原)工作原理:
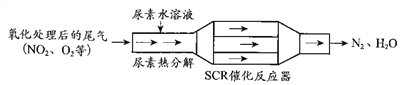
尿素溶液浓度影响NO2的转化,控制尿素的浓度非常关键。测定溶液中尿素(M=60 g·mol 1)含量的方法如下:取a g尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的V1 mL c1 mol·L1 H2SO4溶液吸收完全,剩余H2SO4用V2 mL c2 mol·L1 NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是________________________。
②NSR(NOx储存还原)工作原理:
NOx的储存和还原在不同时段交替进行,如图a所示。

通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。储存NOx的物质是_______;
用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H2与Ba(NO3)2的物质的量之比是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com