
����һ������ˮ��Һ��ֻ���ܺ������������е������֣�K����NH����Ca2����Ba2����Cl����CO32�D��SO42�D����ȡ����100 mL��Һ��������ʵ�飺
��1����һ�ݼ���AgNO3��Һ�г�������
��2���ڶ��ݼ�������NaOH��Һ���Ⱥ��ռ�������0.04 mol��
��3�������ݼ�������BaCl2��Һ�ó���6.27 g������������ϴ�Ӻ�ʣ���������Ϊ2.33 g��
��������ʵ�飬�����Ʋ���ȷ����
A��K��һ�����ڣ���c(K��)��0.2mol��L�D1
B��100 mL��Һ�к�CO32�D 0.01mol
C��K����һ������
D��Cl�D һ������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�������������߶���ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��̬PCl5�ķֽⷴӦΪ2PCl5��g�� 2PCl3��g��+2Cl2��g������473K�ﵽƽ��ʱ��̬PCl5��48.5%�ֽ⣬��573K�ﵽƽ��ʱ��̬PCl5��97%�ֽ⣬��˷�Ӧ��
2PCl3��g��+2Cl2��g������473K�ﵽƽ��ʱ��̬PCl5��48.5%�ֽ⣬��573K�ﵽƽ��ʱ��̬PCl5��97%�ֽ⣬��˷�Ӧ��
A�����ȷ�Ӧ
B�����ȷ�Ӧ
C����Ӧ���ʱ�Ϊ��ķ�Ӧ
D�����ж������ȷ�Ӧ���Ƿ��ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�Ͳ��и߶���ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ������
��֪2A��g����B��g�� 2C��g�������ݻ�Ϊ1L���ܱ������м���0.050 mol A��0.025mol B����500��ʱ��ַ�Ӧ����ƽ�����c��C��=0.010 mol��L-1���ų�����Q1kJ��
2C��g�������ݻ�Ϊ1L���ܱ������м���0.050 mol A��0.025mol B����500��ʱ��ַ�Ӧ����ƽ�����c��C��=0.010 mol��L-1���ų�����Q1kJ��
��1����˵��������Ӧ�Ѿ��ﵽ��ѧƽ��״̬���� ����д��ţ���
A��v��(A)=2v��(B) B��������ѹǿ���ֲ���
C��v(C)=2v(B) D��������������ܶȱ��ֲ���
��2��������ͬ�������м���0.100 mol A��0.050molB��500��ʱ��ַ�Ӧ��ƽ��ų�����Q2kJ����2Q1 Q2�����������������=������
��3��500��ʱ��������Ӧ�Ļ�ѧƽ�ⳣ��K= ��
��4����֪��K��300�棩��K��350�棩���÷�Ӧ�� ������ȡ������ȡ����ȷ�Ӧ������Ӧ�¶����ߣ�A��ת���� �����������С�����䡱����
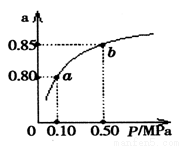
��5��ij�¶��£�A��ƽ��ת���ʣ�a������ϵ��ѹǿ��P���Ĺ�ϵ��ͼ��ʾ��ƽ��״̬��a�䵽bʱ����ѧƽ�ⳣ��K��A�� K��B�������������������=������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ������������ɳ�����չ������ء�����˵������ȷ����
A����������TiO2�ⴥý��������װ�������ͷŵ�HCHOת��Ϊ������
B��CO2��ˮ��Һ�����ԣ�CO2�Ĵ����ŷŻᵼ��������γ�
C����������Դ�����ٶԻ�ʯȼ�ϵ����������Դٽ���̼����
D����CO2�ϳɿɽ���ľ�̼�������ϣ�����ʵ�֡�̼����ѭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�ò����ϡ��Һ������Ƶ�������Һ����ϴ��ճ��Ƥ���ϵĸ�����أ������ӷ���ʽΪ(δ��ƽ)��MnO4����C2O42����H�� CO2����Mn2����___�����ڴ˷�Ӧ��������ȷ����
CO2����Mn2����___�����ڴ˷�Ӧ��������ȷ����
A���÷�Ӧ�ұ߷����ڵIJ�����OH��
B����ƽ�÷�Ӧ��H���Ļ�ѧ��������8
C���÷�Ӧ������������CO2
D���÷�Ӧ����ת��������5e��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ��ˮ�и�����ѧ�ڵ����β��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ڸ��������£����л����ߵ������ڻ�ѧ��Ӧ���ܱ���ȫ���ĵ���
A�������£���1 g��ƬͶ��20 mL 18��4 mol��L-1��������
B����100 mL 3 moI��L-1���������5��6 g��
C����50 mLŨ����������MnO2����
D����5��107 Pa��500 �������ý���������£���3 mol������2 mol�����ϳɰ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�����ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ҵ�ϳ��û�ԭ����������������ˮ(Cr2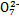 ��Cr
��Cr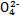 )������Ϊ:
)������Ϊ:
Cr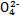
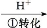 Cr2
Cr2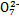
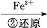 Cr3+
Cr3+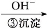 Cr(OH)3��
Cr(OH)3��
��֪:
(1)������д���ƽ��:2Cr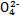 (��ɫ)+2H+
(��ɫ)+2H+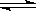 Cr2
Cr2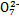 (��ɫ)+H2O
(��ɫ)+H2O
(2)��������ɵ�Cr(OH)3����Һ�д������³����ܽ�ƽ��:
Cr(OH)3(s) 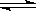 Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
(3)�����£�Cr(OH)3���ܶȻ�Ksp=10-32���ҵ���Һ������Ũ��С��10-5 mol��L-1ʱ�����������Ӳ�����
�����й�˵������ȷ����
A��������м��ᣬ����Һ��pH������2����Һ�Ի�ɫ��Cr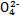 Ũ������
Ũ������
B��������е�2v(Cr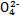 )=v(Cr2
)=v(Cr2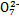 )ʱ��˵����Ӧ2Cr
)ʱ��˵����Ӧ2Cr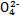 (��ɫ)+2H+
(��ɫ)+2H+  Cr2
Cr2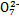 (��ɫ)+H2O�ﵽƽ��״̬
(��ɫ)+H2O�ﵽƽ��״̬
C��������У���Ҫ��ԭ1 mol Cr2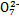 ����Ҫ12 mol (NH4)2Fe(SO4)2��6H2O
����Ҫ12 mol (NH4)2Fe(SO4)2��6H2O
D��������У�������Һ��pH������6ʱ�������Ϊ��ˮ�еĸ��ѳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ�γ��и�����ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���������ֵĿ�����Աȷ�ϻ��ǵر��������и������ε�Һ̬ˮ�������й�ˮ���������ε�˵���������
A��ˮ��һ���������
B��NH4ClO4��Һ������
C��NaClO4�к������Ӽ����ۼ�
D��NH4ClO4ֻ�������ԣ�û�л�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ������ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ���������������أ�����˵����ȷ����
A��̼�ᱵ��̼�����ơ���������������Ϊ����ҩ��ʹ��
B�������ڵĵ����ʲ��Ϸֽ⣬��������ˮ�Ͷ�����̼�ų�����
C����ҵ����������ˮ�࣬����Ҫ�ô���Ϊԭ��
D�����ع��͡�����Ҫ�ɷ�����֬������������͡�ú�Ͳ���ͬ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com