
【题目】常温下,用0.10 mol·L-1NaOH溶液分别滴定20.00 mL浓度均为 0.10mol L-1的CH3COOH(Ka=1.75×10-5)溶液和HCN (Ka=4.9×10-10)溶液所得滴定曲线如图。下列说法正确的是

A. 曲线I和曲线Ⅱ分别代表的是CH3COOH和HCN
B. 点③和点⑤所示溶液中:c(CN-)=c(CH3COO-)
C. 点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
D. 在点②和③之间(不包括端点)存在关系: c(Na+)>c(A-)>c(H+)>c(OH-) (A-代表溶液中的酸根离子)
【答案】C
【解析】A.CH3COOH酸性强,浓度相等时溶液的pH小,则曲线I和曲线Ⅱ分别代表的是HCN和CH3COOH,故A错误;B.点③中pH=7,则c(OH-)=c(H+),则点③中c(Na+)=c(CH3COO-),点⑤中pH=7,则c(OH-)=c(H+),则点⑤中c(Na+)=c(CN),但③中Na+浓度大于⑤中Na+浓度,即c(CN-)<c(CH3COO-),故B错误;C.点①的溶液中存在物料守恒为c(HCN)+c(CN-)=c(Na+),点②所示溶液中的物料守恒为c(CH3COOH)+c(CH3COO-)=c(Na+),二者中钠离子浓度相同,则c(HCN)+c(CN-)=c(CH3COOH)+c(CH3COO-),即c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH),故C正确;D.点②和点③所示溶液中存在电荷守恒c(OH-)+c(CH3COO-)=c(Na+)+c(H+),在点②所示溶液中,c(OH-)<c(H+),则c(CH3COO-)>c(Na+),在③中c(OH-)=c(H+),c(CH3COO-)=c(Na+),所以在点②和③之间(不包括端点)存在离子浓度大小关系:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故D错误;故选C。


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】在恒温2 L密闭容器中通入气体X并发生反应:2X(g)![]() Y(g) ΔH<0,X的物质的量n(x)随时间t变化的曲线如图所示(图中的两曲线分别代表有无催化剂的情形),下列叙述正确的是
Y(g) ΔH<0,X的物质的量n(x)随时间t变化的曲线如图所示(图中的两曲线分别代表有无催化剂的情形),下列叙述正确的是

A.虚线表示使用催化剂的情形
B.b、c两点表明反应在相应条件下达到了最大限度
C.反应进行到a点时放出的热量大于反应进行到b点时放出的热量
D.反应从开始到a点的平均反应速率可表示为v(Y)=0.01mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用微生物处理含KCN的废水。第一步是微生物在氧气充足的条件下,将KCN转化成KHCO3和NH3(最佳pH : 6.7~7.2);第二步是把氨转化为硝酸:NH3+202![]() HNO3+H2O
HNO3+H2O
请完成下列填空:
(1)写出第一步反应的化学反应方程式_____________,第二步反应的还原产物是_____________ (填写化学式)。
(2)在KCN中,属于短周期且原子半径最大的元素是_____,氮原子最外层电子的运动状态有_______种。水的电子式是________。
(3)比较碳和氮元素非金属性强弱,化学反应方程式为_____________。
(4)室握下,0.lmol/LK2CO3、KCN、KHCO3溶液均呈碱性且pH依次减小,在含等物质的量的KCN、KHCO3混合溶液中,阴离子(除OH-)浓度由大到小的顺序是_____________。
(5)工业上还常用氯氧化法处凡含KCN的废水:KCN+2KOH+Cl2=KOCN+2KCl+H2O,2KOCN+4KOH+3Cl2→N2+6KCl+2CO2+2H2O。两扮相比,微生物处理法的优点与缺点是(各写一条)。
优点:________;缺点:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含铜样品的主要成分为a CuCO3·bCu(OH)2(a、b均为最简正整数)。为测定其化学组成和Cu元素的质量分数。甲乙两个实验小组查阅资料,设计了不同的实验方案(假定杂质对实验无干扰)。
Ⅰ.甲组同学利用一下方法测定:
①在一定质量的样品中加入过量的稀硫酸,过滤,测量产生气体的体积
②在滤液中加过量的NaOH稀溶液,过滤
③灼烧②中所得滤渣、直至残留固体恒重
(1)为了除去滤渣中的可溶性杂质,需要对滤渣进行的操作是_____,滤渣应在_____(填仪器名称)中进行灼烧。
(2)利用右图装置测量气体体积,读数时应注意:
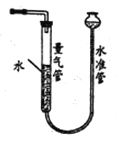
①恢复至室温;②__________;③平视且视线与凹液面最低点相切。
若操作无误,但气体体积测量结果仍然明显偏低,合理的改进措施是____________。
(3)甲组同学在处理实验数据时,将常温常压下测得的气体体积VL换算成V/22.4mol进行计算,则计算所得a值将_______(填“偏大”、“偏小”或“无影响”)。
Ⅱ.乙组同学利用下图装置进行测量(夹持及加热装置略去):
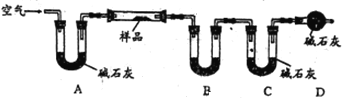
(4)U型管B中的药品是_________,D的作用是_________。
(5)若样品的质量为20g,充分反应后测得B中固体质量增加了0.9g,C中固体质量增加了4.4g,则样品中主要成分的化学式为___________,样品中铜元素的质量分数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu(NO3)2是重要的化工原料。回答下列工业生产和化学实验中的几个问题。
实验室欲制备0.3 mol Cu(NO3)2晶体,甲、乙两同学分别设计实验方案如下:
![]()
①绿色化学的角度分析,_________同学的方案更合理,此同学可节约2mol/L的稀硝酸_________mL;
②甲方案的离子方程式为___________;
③乙同学实验时通入O2的速率不宜过大,为便于观察和控制产生O2的速率,宜选择__________方案(填字母序号)。

④B装置如何检查气密性:_________________。
(2)某校化学兴趣小组的同学对硝酸铜的受热分解进行探究。他们设计了如下左图装置加热Cu(NO3)2固体(加热及夹持装置未画出)。加热过程发现:装置①中的固体逐渐变为黑色;装置②中有气泡产生,但在上升的过程中消失;石蕊试液逐渐变为红色,液体几乎不被压至装置③中。请写出Cu(NO3)2受热分解的化学方程式:______________;


(3)NO2、O2和熔融NaNO3可制作燃料电池,其原理见上右图。该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理利用或转化NO2、SO2、CO、NO等污染性气体是人们共同关注的课题。
Ⅰ.某化学课外小组查阅资料后得知:2NO(g)+O2(g)![]() 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
①2NO(g)![]() N2O2(g)(快) v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2) H1<0
N2O2(g)(快) v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2) H1<0
②N2O2(g)+O2(g)![]() 2NO2(g)(慢) v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2) H2<0
2NO2(g)(慢) v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2) H2<0
请回答下列问题:

(1)反应2NO(g)+O2(g)![]() 2NO2(g)的H=________________(用含H1和H2的式子表示)。一定温度下,反应2NO(g)+O2(g)
2NO2(g)的H=________________(用含H1和H2的式子表示)。一定温度下,反应2NO(g)+O2(g)![]() 2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=_____________________。
2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=_____________________。
(2)决定2NO(g)+O2(g)![]() 2NO2(g)反应速率是反应②,反应①的活化能E1与反应②的活化能E2的大小关系为E1________E2(填“>”、“<”或“=”)。
2NO2(g)反应速率是反应②,反应①的活化能E1与反应②的活化能E2的大小关系为E1________E2(填“>”、“<”或“=”)。
Ⅱ.(3)反应N2O4(g)![]() 2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强有如下关系:v(N2O4)=k1·p(N2O4),v(NO2)=k2·p2(NO2)。其中k1、k2是与温度有关的常数。一定温度下,相应的速率与压强关系如图所示,在图中标出的点中,能表示该反应达到平衡状态的两个点是_______________,理由是__________________________________________________________________________________________。
2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强有如下关系:v(N2O4)=k1·p(N2O4),v(NO2)=k2·p2(NO2)。其中k1、k2是与温度有关的常数。一定温度下,相应的速率与压强关系如图所示,在图中标出的点中,能表示该反应达到平衡状态的两个点是_______________,理由是__________________________________________________________________________________________。
(4)在25℃时,将a mol·L-1的氨水溶液与0.02 mol·L-1 HCl溶液等体积混合后溶液恰好呈中性(忽略溶液混合后体积的变化),用含a的表达式表示250C时NH3·H2O的电离常数Kb=_________________。用质量分数为17%,密度为0.93 g/cm3的氨水,配制200 mL a mol·L-1的氨水溶液,所需原氨水的体积V=___________mL。
(5)如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。物质A的化学式为_________,阴极的电极反应式是__________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列括号中的物质是除去杂质所需的药品,其中错误的是( )
A.NaCl溶液中有杂质Na2SO4(氯化钡)
B.FeSO4溶液中有杂质CuSO4(铁粉)
C.生石灰中混有少量石灰石(盐酸)
D.BaCl2溶液中有少量MgCl2(氢氧化钡)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com