
某离子反应中涉及H2O、ClO—、NH4+、H+、N2、Cl—六种微粒。其中N2的物质的量随时间变化的曲线如图所示。下列判断正确的是: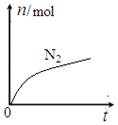
| A.该反应的还原剂是Cl— |
| B.消耗1 mol还原剂,转移6 mol电子 |
| C.氧化剂与还原剂的物质的量之比为2:3 |
| D.反应后溶液的酸性明显增强 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:单选题
按要求写出下列反应的化学方程式
(1)短周期元素组成的三种有色物质(单质或化合物)可以与水发生氧化还原反应,水既不是氧化剂也不是还原剂,按相对分子质量由小到大的顺序写出三种物质与水反应的方程式。
①
②
③
(2)由短周期元素构成的两种单质与水发生氧化还原反应
④水只作氧化剂
⑤水只作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在加热时,浓硫酸与铜发生反应的化学方程式为:2H2SO4(浓)+Cu  CuSO4+SO2↑+2H2O,对于该反应,下列说法中不正确的是
CuSO4+SO2↑+2H2O,对于该反应,下列说法中不正确的是
| A.是氧化还原反应 | B.浓硫酸是还原剂 |
| C.H2SO4表现了氧化性和酸性 | D.反应中Cu发生了氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
三氟化氮(NF3)在微电子工业中有重要用途,可由氨气和氟气反应得到,它在潮湿的空气中与水蒸气反应的产物有HF、NO和HNO3。下列说法错误的是
| A.原子半径:N>F |
| B.在与水蒸气反应中,NF3既是氧化剂又是还原剂 |
| C.若NF3泄漏,可用石灰水溶液喷淋的方法减少污染 |
| D.在潮湿空气中反应,被氧化与被还原的元素的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知常温下可用Co2O3制备Cl2,反应前后存在六种微粒:Co2O3、H2O、Cl2、H+、Cl-和Co2+。下列叙述不正确的是 ( )。
| A.氧化产物为Cl2 |
| B.参加反应的氧化剂与还原剂的物质的量之比为1∶2 |
| C.若有3 mol H2O生成,则反应中有2 mol电子转移 |
| D.当该反应生成2.24 L Cl2(标准状况)时,反应中有0.1 mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氯酸是一种强酸,浓度超过40%时会发生分解,该反应可表示为aHClO3―→bO2↑+cCl2↑+dHClO4+eH2O,下列有关说法不正确的是( )
| A.由反应可确定氧化性:HClO3>O2 |
| B.由非金属性:Cl>S,可推知酸性:HClO3>H2SO4 |
| C.若氯酸分解所得1 mol混合气体的质量为45 g,则反应方程式可表示为3HClO3=2O2↑+Cl2↑+HClO4+H2O |
| D.若化学计量数a=8,b=3,则生成3 mol O2时该反应转移20 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据下列事实:①A+B2+=A2++B;②D+2H2O=D(OH)2+H2↑;③以B、E为电极与E的盐溶液组成原电池,电极反应为E2++2e-=E,B-2e-=B2+。由此可知A2+、B2+、D2+、E2+的氧化性强弱关系是( )。
A.D2+>A2+>B2+>E2+
B.A2+>B2+>D2+>E2+
C.D2+>E2+>A2+>B2+
D.E2+>B2+>A2+>D2+
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
为实现中国消除碘缺乏病的目标,卫生部规定食盐必须加碘,其中碘以碘酸钾(KIO3)形式存在,已知在溶液中I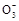 可和I-发生反应:I
可和I-发生反应:I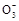 +5I-+6H+
+5I-+6H+ 3I2+3H2O,根据此反应,可用试纸和一些生活中常见物质进行实验,证明食盐中存在I
3I2+3H2O,根据此反应,可用试纸和一些生活中常见物质进行实验,证明食盐中存在I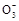 ,可供选用的物质有:①自来水②蓝色石蕊试纸,③碘化钾淀粉试纸④淀粉⑤食糖⑥食醋⑦白酒。进行上述实验时必须使用的物质是( )。
,可供选用的物质有:①自来水②蓝色石蕊试纸,③碘化钾淀粉试纸④淀粉⑤食糖⑥食醋⑦白酒。进行上述实验时必须使用的物质是( )。
| A.①③ | B.③⑥ | C.②④⑥ | D.①②④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
Na2FeO4是一种高效多功能水处理剂。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,下列说法中不正确的是( )
| A.Na2O2在上述反应中只作氧化剂 |
| B.Na2FeO4既是氧化产物又是还原产物 |
| C.Na2FeO4处理水时,既能杀菌,又能产生胶体净水 |
| D.2 mol FeSO4发生反应时,共有10 mol电子发生转移 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com