
【题目】在一定条件下,容积为2 L的密闭容器中,将2 mol L气体和3 mol M气体混合,发生如下反应:2L(g)+3M(g)![]() xQ(g)+3R(g),10s末,生成2.4 mol R,并测得Q的浓度为0.4 mol·L-1。计算:
xQ(g)+3R(g),10s末,生成2.4 mol R,并测得Q的浓度为0.4 mol·L-1。计算:
(1)10 s末L的物质的量浓度为_____________。
(2)前10 s内用M表示的化学反应速率为_____________。
(3)化学方程式中x值为_____________。
(4)在恒温恒容条件,往容器中加入1 mol氦气,反应速率________(增大、减小、不变)。
(5)在恒温恒压条件,往容器中加入1 mol氦气,反应速率________(增大、减小、不变)。
【答案】
(1)0.2mol/L;
(2)0.12mol/(Ls);
(3)1;(4)不变;(5)减小;
【解析】
试题分析:经2min达平衡,生成2.4molR,并测得Q的浓度为0.4mol/L,Q物质的量=0.4mol/L×2L=0.8mol,物质的量之比等于化学计量数之比,0.8:2.4=x:3,计算得到x=1;
2L(g)+3M(g)![]() Q(g)+3R(g)
Q(g)+3R(g)
起始量(mol) 2 3 0 0
变化量(mol) 1.6 2.4 0.8 2.4
10s末(mol) 0.4 0.6 0.8 2.4
(1)10s末L的物质的量浓度=![]() =0.2mol/L;
=0.2mol/L;
(2)前10s内用M表示的化学反应速率=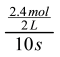 =0.12mol/(Ls);
=0.12mol/(Ls);
(3)经2min达平衡,生成2.4molR,并测得Q的浓度为0.4mol/L,Q物质的量=0.4mol/L×2L=0.8mol,物质的量之比等于化学计量数之比,0.8:2.4=x:3,计算得到x=1;
(4)在恒温恒容条件,往容器中加入1mol氦气,总压增大,分压不变平衡不动,反应速率不变;
(5)在恒温恒压条件,往容器中加入1mol氦气,为保持恒压条件增大,压强减小,反应速率减小。


科目:高中化学 来源: 题型:
【题目】25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
A.0.1 mol·L-1(NH4)2Fe(SO4)2溶液中:c(SO![]() )=c(NH
)=c(NH![]() )>c(Fe2+)>c(H+)>c(OH-)
)>c(Fe2+)>c(H+)>c(OH-)
B.pH=2的HNO3溶液与pH=12的NH3·H2O溶液等体积混合:
c(NH![]() )+c(H+)=c(OH-)+c(NO
)+c(H+)=c(OH-)+c(NO![]() )
)
C.浓度均为0.1 mol/L的Na2CO3与NaHCO3混合溶液:
c(Na+)>c(HCO![]() )>c(CO
)>c(CO![]() )>c(OH-)
)>c(OH-)
D.0.1 mol/L NaHS溶液:c(OH-)=c(H+)+2c(H2S)+c(HS-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取三份不同组成镁铝混合物分别加入1mol/L的盐酸,待混合完全溶解后,往溶液中加入1mol/L的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如下所示.下列说法中错误的是

A.图I中a的取值范围为0≤a<≤50
B.图I中![]() 的最大值为2.5
的最大值为2.5
C.图II中a的取值范围为80<a<96.7
D.图III中a的取值范围为75<a<80
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是由周期表中短周期元素组成的三种常见化合物,甲、乙、丙是三种单质,这些单质和化合物之间存在如图1所示的关系,完成下列空白:

(1)向酚酞试液中加入化合物A的粉末,现象为_____________。
(2)单质甲与化合物B反应的离子方程式为_______________。
(3)向20mL某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图2图示两种情况。

①由A确定滴加前60mL的盐酸时,发生反应的离子方程式为_________。
②由B表明,原溶液通入CO2气体后,所得溶液中的溶质的化学式为________。
③由A、B可知,两次实验通入的CO2的体积比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.Na2CO3水解:CO![]() +H2O == H2CO3+2OH-
+H2O == H2CO3+2OH-
B.NaHSO4溶液中滴加Ba(OH)2溶液至中性:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
C.Cu与稀HNO3反应:Cu+4H++2NO![]() =Cu2++2NO↑+2H2O
=Cu2++2NO↑+2H2O
D.醋酸除水垢:CO![]() +2CH3COOH===2CH3COO-+CO2↑+H2O
+2CH3COOH===2CH3COO-+CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
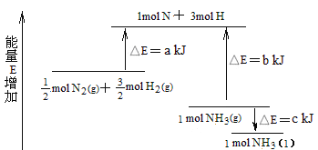
【题目】化学反应N2+3H2 ![]() 2NH3的能量变化下图所示,该反应的热化学方程式是
2NH3的能量变化下图所示,该反应的热化学方程式是
A.N2(g)+3H2(g) ![]() 2NH3(l) △H = 2(a-b+c) kJ/mol
2NH3(l) △H = 2(a-b+c) kJ/mol
B.N2(g)+3H2(g) ![]() 2NH3(l) △H = 2(a-b-c) kJ/mol
2NH3(l) △H = 2(a-b-c) kJ/mol
C.![]() N2(g)+
N2(g)+![]() H2(g)
H2(g) ![]() NH3(l) △H = (b+c-a) kJ/mol
NH3(l) △H = (b+c-a) kJ/mol
D.![]() N2(g)+
N2(g)+![]() H2(g)
H2(g) ![]() NH3(g) △H = (a+b) kJ/mol
NH3(g) △H = (a+b) kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】COCl2(g)![]() CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入稀有气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入稀有气体,能提高COCl2转化率的是( )
CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入稀有气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入稀有气体,能提高COCl2转化率的是( )
A. ①②④ B. ①④⑥ C. ②③⑤ D. ③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-25kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com