
(16分)A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示(部分产物略去):

(1)若A是能使湿润的红色石蕊试纸变蓝的气体,C、D均为空气的主要成分,E是一种有毒气体.
①C的电子式为_______________.
②写出反应Ⅱ的化学方程式______________________.
(2)若A是淡黄色化合物,常温下D是无色气体,C中含有的阴、阳离子均为10电子粒子.
①C中所含化学键的类型是____________.
②写出反应Ⅲ的离子方程式______________________.
(3)将(2)中一定量的气体D通入2 L C的溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl物质的量关系如图所示(忽略气体的溶解和HCl的挥发).

①O点溶液中所含溶质的化学式为_____________,a点溶液中各离子浓度由大到小的关系是_______________.
②标准状况下,通入气体D的体积为_____L,C溶液的物质的量浓度为_____mol·L-1.
(16分)(1)①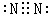 (2分) ② 2NO + 2CO
(2分) ② 2NO + 2CO 2CO2 + N2 (2分)
2CO2 + N2 (2分)
(2)①离子键、共价键 (2分) ② 2OH- + CO2 = CO32- + H2O (2分)
(3)① Na2CO3、NaOH (2分) c(Na+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-) (2分)
② 44.8 (2分) 2.5 (2分)
【解析】(1)若A是能使湿润的红色石蕊试纸变蓝的气体,则A是氨气。C、D均为空气的主要成分,E是一种有毒气体,所以C是氮气,D是氧气,E是CO。氨气发生催化氧化生成NO,NO能氧化CO生成氮气和CO2,方程式2NO + 2CO 2CO2 + N2 。
2CO2 + N2 。
(2)若A是淡黄色化合物,则A是过氧化钠。常温下D是无色气体,所以D是CO2,则B是碳酸钠,C是氢氧化钠。氢氧化钠吸收CO2即生成碳酸钠。
(3)氢氧化钠和CO2反应生成碳酸钠或者碳酸氢钠。由于碳酸钠和盐酸反应是分步进行的,首先生成碳酸氢钠,然后再生成CO2,且这两步反应中消耗的盐酸是相同的,所以根据图像可知,所得的溶液中氢氧化钠应该是过量的。所以O点溶液中所含溶质的化学式为Na2CO3、NaOH 。a点溶液是氯化钠和碳酸氢钠的混合液,且氯化钠的物质的量大于碳酸氢钠的。碳酸氢钠水解显碱性,因此a点溶液中各离子浓度由大到小的关系是c(Na+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-) 。由于最终生成的CO2是2mol,所以根据碳原子守恒可知,通入的CO2也是2mol。根据图像可知,最终生成氯化钠是5mol,所以根据钠抑制守恒可知,氢氧化钠也是5mol,起浓度是2.5mol/L。


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
(16分) A、B、C、D、E、F属于短周期主族元素。A的原子半径在短周期中最大,B的一种原子中,质量数与质子数之差为零, C与D、E与F均同主族,C元素的原子L层电子数是K层的2倍,E原子的核外电子总数等于C、D原子核外电子总数的差。
(1)离子B-的结构示意图为 ;化合物CE2的分子属于 分子(填“极性”或“非极性”);用电子式表示化合物A2F的形成过程 。
(2)A、E、F形成的简单离子的半径由大到小的顺序为 (用离子符号表示);元素C、D、E形成的常见单质中,熔沸点由高到低的顺序是(用名称表示)
(3)由B、C可以构成的最简单的化合物W,取16.0g分子式为W·8H2O的化合物,将其释放的W完全燃烧生成液态水,可放出89.03kJ的热量,则W燃烧的热化学方程式为
(4)使液化石油气氧化直接产生电流是新世纪最富有挑战性的课题之一。有人设计制造了一种燃料电池,一个电极通入富含E单质的气体和少量CE2,另一电极通入液化石油气(以C4H10表示),电池的电解质是熔融的K2CO3。该电池的负极反应式为 ,电池工作时,电解质里的CO32-向 极移动。
查看答案和解析>>
科目:高中化学 来源:2012届河北省石家庄市高三补充题、压轴题化学试卷(带解析) 题型:填空题
(16分)A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示(部分产物略去):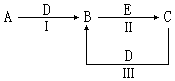
(1)若A是能使湿润的红色石蕊试纸变蓝的气体,C、D均为空气的主要成分,E是一种有毒气体.
①C的电子式为_______________.
②写出反应Ⅱ的化学方程式______________________.
(2)若A是淡黄色化合物,常温下D是无色气体,C中含有的阴、阳离子均为10电子粒子.
①C中所含化学键的类型是____________.
②写出反应Ⅲ的离子方程式______________________.
(3)将(2)中一定量的气体D通入2 L C的溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl物质的量关系如图所示(忽略气体的溶解和HCl的挥发).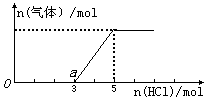
①O点溶液中所含溶质的化学式为_____________,a点溶液中各离子浓度由大到小的关系是_______________.
②标准状况下,通入气体D的体积为_____L,C溶液的物质的量浓度为_____mol·L-1.
查看答案和解析>>
科目:高中化学 来源:2013学年湖北省广水市高三第一次月考化学试卷(解析版) 题型:填空题
(16分)A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示(部分产物略去):
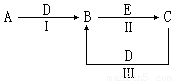
(1)若A是能使湿润的红色石蕊试纸变蓝的气体,C、D均为空气的主要成分,E是一种有毒气体.
①C的电子式为_______________.
②写出反应Ⅱ的化学方程式______________________.
(2)若A是淡黄色化合物,常温下D是无色气体,C中含有的阴、阳离子均为10电子粒子.
①C中所含化学键的类型是____________.
②写出反应Ⅲ的离子方程式______________________.
(3)将(2)中一定量的气体D通入2 L C的溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl物质的量关系如图所示(忽略气体的溶解和HCl的挥发).

①O点溶液中所含溶质的化学式为_____________,a点溶液中各离子浓度由大到小的关系是_______________.
②标准状况下,通入气体D的体积为_____L,C溶液的物质的量浓度为_____mol·L-1.
查看答案和解析>>
科目:高中化学 来源:2010年重庆市高三年级5月月考(理综)化学部分 题型:填空题
(16分) A、B、C、D、E、F属于短周期主族元素。A的原子半径在短周期中最大,B的一种原子中,质量数与质子数之差为零, C与D、E与F均同主族,C元素的原子L层电子数是K层的2倍,E原子的核外电子总数等于C、D原子核外电子总数的差。
(1)离子B-的结构示意图为 ;化合物CE2的分子属于 分子(填“极性”或“非极性”);用电子式表示化合物A2F的形成过程 。
(2)A、E、F形成的简单离子的半径由大到小的顺序为 (用离子符号表示);元素C、D、E形成的常见单质中,熔沸点由高到低的顺序是(用名称表示)
(3)由B、C可以构成的最简单的化合物W,取16.0g分子式为W·8H2O的化合物,将其释放的W完全燃烧生成液态水,可放出89.03kJ的热量,则W燃烧的热化学方程式为
(4)使液化石油气氧化直接产生电流是新世纪最富有挑战性的课题之一。有人设计制造了一种燃料电池,一个电极通入富含E单质的气体和少量CE2,另一电极通入液化石油气(以C4H10表示),电池的电解质是熔融的K2CO3。该电池的负极反应式为 ,电池工作时,电解质里的CO32-向 极移动。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com