
【题目】陶瓷的发明是人类早期科学技术发展史上的一个重要里程碑。陶瓷不具有的性质是
A.导电B.耐酸碱C.抗氧化D.耐高温
科目:高中化学 来源: 题型:
【题目】在温度不变的条件下,在恒容的容器中进行下列反应:N2O4(g)═2NO2(g),若N2O4的浓度由0.1molL﹣1降到0.07molL﹣1需要15s,那么N2O4的浓度由0.07molL﹣1降到0.05molL﹣1所需的反应时间( )
A.等于5s
B.等于10s
C.小于10s
D.大于10s
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50ml0.50molL﹣1盐酸与50mL0.55molL﹣1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程 中放出的热量可计算中和热.回答下列问题: 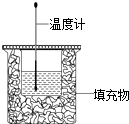
(1)从实验装置上看,图中缺少的仪器是 .
(2)实验中若用70mL0.50molL﹣1盐酸跟70mL0.55molL﹣1NaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等”或“不相等”),所求中和热(填“相等”或“不相等”).
(3)用50ml0.25molL﹣1H2SO4代替盐酸,用50mL0.275molL﹣1Ba(OH)2代替 NaOH溶液进行上述实验,测得的中和热的绝对值会(填“偏大”“偏小”或“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1 mol/L 的某二元酸H2A的溶液中可能存在的含A粒子(H2A、HA-、A2-)的物质的量分数随pH的变化如图所示,下列说法中不正确的是
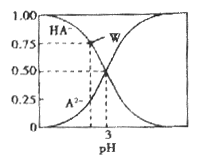
A. H2A的电离方程式为H2A![]() HA-+H+, HA-
HA-+H+, HA-![]() H++A2-
H++A2-
B. Na2A溶液一定呈碱性,NaHA溶液一定呈酸性
C. 常温下,电离常数K(HA-)=10-3
D. W点的溶液中pH=3-lg3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10 mL 0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是( )
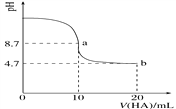
A. a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B. a、b两点所示溶液中水的电离程度相同
C. pH=7时,c(Na+)=c(A-)+c(HA)
D. b点所示溶液中c(A-)>c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 1H、2H、3H、H+、H2是氢元素形成的五种不同粒子
B. O2、O3互为同位素
C. 正丁烷和异丁烷互为同系物
D. 乙烷、乙烯互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氮及其化合物说法,不正确的是( )
A.氮气性质稳定,可用于工业制镁的冷却剂
B.N2H4和N2O4可用作航天飞机的燃料
C.碳酸氢铵常用作氮肥,不可与碱性肥料混用
D.硝酸可用于制造染料、塑料、炸药和硝酸盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X,Y,Z,W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( ) ![]()
A.原子半径:Z>W>X>Y
B.元素X、Y、Z、W的最高化合价分别与其主族序数相等
C.最简单气态氢化物的热稳定性:H2Y>XH3>WH3>ZH4
D.最高价氧化物对应水化物的酸性:HXO3>H3WO4>H2ZO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列氯化物中,既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的是()
A. CuCl2 B. FeCl2 C. FeCl3 D. MgCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com