
| A. | 氧气的摩尔质量是32 g | |
| B. | 6.02×1023个N2分子的质量是28 g/mol | |
| C. | 1 mol H2O的质量是18g | |
| D. | 1 mol CO2中所含氧原子数约是6.02×1023个 |
分析 A.摩尔质量的单位为g/mol;
B.根据n=$\frac{N}{{N}_{A}}$计算出氮气的物质的量,最高价m=nM计算出氮气的质量,质量的单位为g;
C.根据m=nM计算出1mol水的质量;
D.1mol二氧化碳分子中含有2molO原子,根据N=nNA计算出含有氧原子的数目.
解答 解:A.氧气的摩尔质量为32g/mol,故A错误;
B.6.02×1023个N2分子的物质的量为1mol,1mol氮气的质量是×1mol=28g,故B错误;
C.1 mol H2O的质量是:18g/mol×1mol=18g,故C正确;
D.1 mol CO2中所含氧原子数约是:6.02×1023×mol-1×1mol×2=6.02×2×1023个,故D错误;
故选C.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、阿伏伽德罗常数等物理量之间的关系为解答关键,试题侧重基础知识的考查,培养了学生的化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 铝是地壳中含量最多的元素 | |
| B. | 常温下,铝能与NaCl溶液发生置换反应 | |
| C. | 铝能溶解于冷浓硝酸中,生成硝酸铝 | |
| D. | 在化学反应中,铝容易失去电子,是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水洗涤2~3次后再使用 | |
| B. | 用滤纸擦干后才可使用 | |
| C. | 用盐酸洗涤后,经蒸馏水冲洗,方可使用 | |
| D. | 用盐酸洗涤后,再在酒精灯火焰上灼烧到没有颜色,才可使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
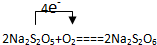 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | 氨水浓度/(mol•L-1) | 盐酸浓度/(mol•L-1) | 混合溶液pH |
| ① | 0.1 | 0.1 | pH=5 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH>7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
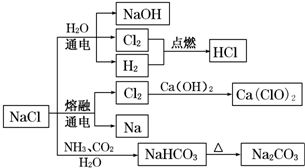
| A. | 25℃,NaHCO3在水中的溶解度比Na2CO3的大 | |
| B. | NaHCO3 受热分解的方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ | |
| C. | 电解饱和氯化钠溶液的方程式为:2NaCl$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑ | |
| D. | 图中所示转化反应都是氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com