
(14分)某学生利用下面实验装置探究盐桥式原电池的工作原理(Cu元素的相对原子 质量为64)。按照实验步骤依次回答下列问题:
质量为64)。按照实验步骤依次回答下列问题:
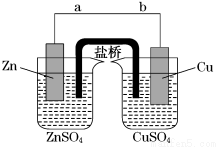
(1)导线中电子流向为____________(用a、b表示)。
(2)若装置中铜电极的质量增加0.64 g,则导线中转移的电子数目为________ (用“NA”表示) ;
(3)装置中盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,对盐桥中的K+、Cl-的移动方向的表述正确的是________。
A.盐桥中的K+向左侧烧杯移动、Cl-向右侧烧杯移动
B.盐桥中的K+向右侧烧杯移动、Cl-向左侧烧杯移动
C.盐桥中的K+、Cl-都向左侧烧杯移动
D.盐桥中的K+、Cl-几乎都不移动
(4)若将反应2Fe3++Cu===Cu2++2Fe2+设计成原电池,写出电极反应式。
正极反应_____________;
(5)下列是用化学方程式表示的化学变化,请在每小题后的横线上注明能量的转化形式。
①电池总反应:Zn+Ag2O+H2O===Zn(OH)2+2Ag:__________。
②2C2H2+5O2 4CO2+2H2O:_____________。
4CO2+2H2O:_____________。
③6H2O+6CO2 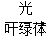 C6H12O6(葡萄糖)+6O
C6H12O6(葡萄糖)+6O 2:__________。
2:__________。
科目:高中化学 来源:2016届辽宁省高三10月月考化学试卷(解析版) 题型:选择题
从化学看生活,你认为下列说法不合理的是
A、塑料制品长期不使用也会老化
B、食醋和料酒混合即可产生大量有香味的乙酸乙酯
C、“84消毒液”可用于消毒、漂白,说明其具有强氧化性
D、纯碱是Na2C03,小苏打是NaHC03,其水溶液均呈碱性
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三上学期第二次月考理综化学试卷(解析版) 题型:选择题
下列各组离子能在指定溶液中大量共存的是
①遇到苯酚显紫色的溶液:SCN-、Na+、SO42-、Fe2+
②pH=13的溶液中:Na+、AlO2-、NO3-、S2-、SO32-
③加入Fe能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、NO3-
④使pH试纸呈红色的溶液中:Fe3+、MnO4-、Na+、SO42-
⑤酸性溶液中:Fe2+、Al3+、SO42-、I-
A.①②④ B.②③④ C.②④⑤ D.①③⑤
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列关于Na2CO3和NaHCO3性质的说法错误的是
A.热稳定性:NaHCO3<Na2CO3
B.与同浓度盐酸反应的剧烈程度:NaHCO3<Na2CO3
C.相同温度时,在水中的溶解性:NaHCO3<Na2CO3
D.等物质的量浓度溶液的pH:NaHCO3<Na2CO3
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省牡丹江市高三9月月考化学试卷(解析版) 题型:实验题
(14分)亚氯酸钠(NaClO2)是重要漂白剂,探究小组开展如下实验,回答下列问题:
实验Ⅰ:制取NaClO2晶体按如图装置进行制取。
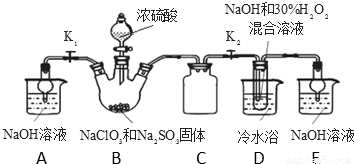
已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
(1)装置C的作用是 ;
(2)已知装置B中的产物有ClO2气体,则装置B中反应的化学方程式为 ;装置D中反应生成NaClO2的化学方程式为 ;反应后的溶液中阴离子除了ClO2-、ClO3-、Cl-、ClO-、OH-外还可能含有的一种阴离子是 ;检验该离子的方法是 ;
(3)请补充从装置D反应后的溶液中获得NaClO2晶体的操作步骤。
①减压,55℃蒸发结晶;② ;③ ;④ 得到成品。
(4)如果撤去D中的冷水浴,可能导致产品中混有的杂质是 ;
实验Ⅱ:样品杂质分析与纯度测定
(5)测定样品中NaClO2的纯度。测定时进行如下实验:
准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2-+4I-+4H+=2H2O+2I2+Cl-,将所得混合液稀释成100 mL待测溶液。取25.00 mL待测溶液,加入淀粉溶液做指示剂,用c mol•L-1 Na2S2O3标准液滴定至终点,测得消耗标准液体积的平均值为V mL(已知:I2+2S2O32-= 2I-+S4O62-)。请计算所称取的样品中NaClO2的物质的量为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省高一下期末化学试卷(解析版) 题型:选择题
由海水制备无水氯化镁,主要有以下步骤:
①在一定条件下脱水干燥;②加熟石灰;③加盐酸;
④过滤;⑤浓缩结晶。其先后顺序正确的是
A.②④⑤③① B.③②④①⑤ C.③④②⑤① D.②④③⑤①
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二9月月考化学试卷(解析版) 题型:填空题
按要求填空。
(1)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式是__ ______。
(2)已知拆开1 mol H—H键、1 mol I—I分别需要吸收的能量为436 kJ、151 kJ,而形成1 mol H—I键会释放299 kJ能量。则由氢气和碘反应生成1 mol HI需要________(填“放出”或“吸收”)_______ __kJ的热量。
(3)S(g)+O2(g)=SO2(g) ΔH 1<0;S(s)+O2(g)=SO2(g) ΔH 2<0,比较ΔH1 __ ___ΔH2大小。
查看答案和解析>>
科目:高中化学 来源:2016届江西省九江市七校高三第一次联考化学试卷(解析版) 题型:选择题
下列离子方程式表达正确的是
A.漂白粉溶液中通入过量的CO2:ClO-+CO2+H2O===HClO+HCO3﹣
B.用碳酸钠溶液吸收Br2:CO32-+Br2+2H2O===Br-+BrO3-+CO2↑+4H+
C.用铜电极电解硫酸铜溶液:2Cu2++2H2O △ 2Cu↓+O2↑+4H+
D.已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液中,形成无色溶液,当Pb(Ac)2溶液中通入H2S时有黑色沉淀生成:Pb2++2Ac﹣+H2S===PbS+2HAc
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期第一次月考化学试卷(解析版) 题型:填空题
(16分)(1)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是______
a.NH3 b.HI c.SO2 d.CO2
(2)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:__________
(3)工业生产甲醇的常用方法是:CO(g)+2H2(g) CH3OH(g) △H = —90.8kJ/mol。
CH3OH(g) △H = —90.8kJ/mol。
已知:2H2(g)+O2(g)=2H2O(l) △H = -571.6kJ/mol;
2CO(g)+O2(g)=2CO2(g) △H = -566.0kJ/mol
计算2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(l) △H = 。
(4)某实验小组设计了如图所示的甲醇燃料电池装置。
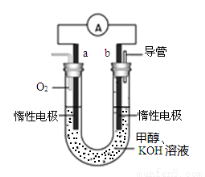
①该电池工作时,负极是 极(填“a”或 “b”);
②工作一段时间后,测得溶液的pH减小,该电池负极反应的离子方程式为 。
(5)电解法促进橄榄石(主要成分是Mg2SiO4)固定CO2的部分工艺流程如下:
已知:Mg2SiO4(s)+4HCl(aq) 2MgCl2(aq)+SiO2 (s)+ 2H2O(l) △H =-49.04 kJ·mol-1
2MgCl2(aq)+SiO2 (s)+ 2H2O(l) △H =-49.04 kJ·mol-1
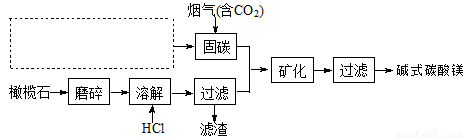
①某橄榄石的组成是Mg9FeSi5O20,用氧化物的形式可表示为 。
②在上图虚框内补充一步工业生产流程 。
③ 经分析,所得碱式碳酸镁产品中含有少量NaCl和Fe2O3。为提纯,可采取的措施依次为:对溶解后所得溶液进行除铁处理、对产品进行洗涤处理。判断产品洗净的操作是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com