
| A. | ρ400mol•L-1 | B. | 20ρmol•L-1 | C. | 2.5ρmol•L-1 | D. | 1.25ρmol•L-1 |
分析 溶液的体积=$\frac{20g}{ρg/ml}$=$\frac{20}{ρ}$mL=$\frac{0.02}{ρ}$L,n(Ca2+)=$\frac{1g}{40g/mol}$=$\frac{1}{40}$mol,c(Ca2+)=$\frac{\frac{1}{40}mol}{\frac{0.02}{ρ}L}$=$\frac{5ρ}{4}$mol/L,硝酸钙中钙离子和硝酸根离子的浓度之比等于其系数之比,据此计算硝酸根离子浓度.
解答 解:溶液的体积=$\frac{20g}{ρg/ml}$=$\frac{20}{ρ}$mL=$\frac{0.02}{ρ}$L,n(Ca2+)=$\frac{1g}{40g/mol}$=$\frac{1}{40}$mol,c(Ca2+)=$\frac{\frac{1}{40}mol}{\frac{0.02}{ρ}L}$=$\frac{5ρ}{4}$mol/L,硝酸钙中钙离子和硝酸根离子的浓度之比等于其系数之比,则c(NO3-)=2c(Ca2+)=2×$\frac{5ρ}{4}$mol/L=2.5ρmol/L,
故选C.
点评 本题考查物质的量浓度计算,为高频考点,侧重考查学生分析计算能力,明确钙离子、硝酸根离子浓度之比与其系数之比的关系是解本题关键,注意物质的量有关公式的灵活运用,注意单位换算,为易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题

| A. | 反应结束时溶液的pH=7 | |
| B. | 反应后溶液中存在的粒子只有Na+和Cl- | |
| C. | 该反应的实质是H+和OH-结合生成水 | |
| D. | 反应前后所有元素的化合价均无变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 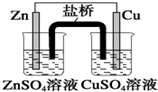 装置中,盐桥中的K+移向ZnSO4溶液 | |
| B. | 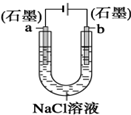 装置工作一段时间后,a极附近溶液的pH增大 | |
| C. | 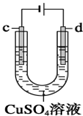 用装置精炼铜时,c极为精铜,电解过程中CuSO4溶液没有变化 | |
| D. | 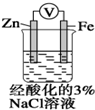 装置中电子由Zn流向Fe,装置中有Fe2+生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 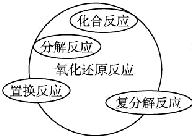 | B. | 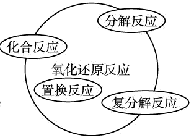 | ||
| C. |  | D. | 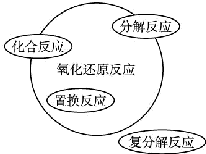 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8.5 g | B. | 10.8 g | C. | 6.2 g | D. | 4.6 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
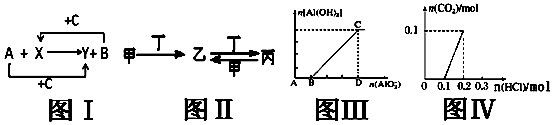
| A. | 关于图Ⅰ,已知C是氧气,X、Y是化合物,则A是钠,B是氢气 | |
| B. | 关于图Ⅱ,已知甲、乙、丙均含有相同的某种元素,若甲为NaOH溶液,则丁可能是CO2 | |
| C. | 关于图Ⅲ,表示NaAlO2溶液逐滴加入到NaOH溶液中,n(Al(OH)3)和n(AlO2-)之间的关系图象 | |
| D. | 关于图Ⅳ,表示各含0.1mol苏打和NaOH混合液中逐滴加入含溶质0.2mol的盐酸的关系图象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ•mol--1,则氢气的燃烧热为241.8 kJ•mol-1 | |
| B. | 已知2C(s)+2O2(g)=2CO2(g)△H=a,2C(s)+O2(g)=2CO(g)△H=b,则a>b | |
| C. | 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出的热量小于57.3 kJ | |
| D. | 已知P (白磷,s)=P (红磷,s)△H<0,则白磷比红磷稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com