
【题目】下列说法中错误的是( )
A.在Na2S溶液中滴入酚酞试液,呈红色
B.升高温度能使FeCl3溶液中的H+浓度增大
C.一切钾盐、钠盐、硝酸盐都不发生水解
D.醋酸盐溶于水能发生水解
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
【题目】现有NaHCO3和Na2CO3xH2O的混合物7.4g,加热到反应完全,并让产生的气体依次被无水氯化钙B和碱石灰C完全吸收,冷却至室温时,测得B管增重3.78g,C管增重0.44g,请求算下列问题:
(1)残留固体的成分是 , 质量是g.
(2)原混合物中NaHCO3的质量是g.
(3)求出x的值(要求有计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向体积为2L的固定密团容器中通入3molX气体,在一定温度下发生如下反应:2X(g) ![]() Y(g)+3Z(g)。
Y(g)+3Z(g)。
(1)经5min后反应达到平衡,容器内的压强为起始时的1.2倍,则Y的反应速率为________mol/(L·min)。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为甲:v(X)=3.5 mol/(L·min);乙:v(Y)=2 mol/(L·min);丙:v(Z)=4.5 mol/(L·min);丁:v(X)=3.5 mol/(L·s)。若其他条件相同,温度不同,则温度由高到低的顺序是(填序号)______。
(3)向达到(1)所述的平衡体系中充入氦气,则平衡_______(填“向左”、“向右”或“不”) 移动;从(1)所述的平衡体系中移走部分Y气体,则平衡_______(填“向左”、“向右”或“不”) 移动。
(4)在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,则平衡后X的转化率与(1)所述的平衡中X的转化率相比较_________。
A.无法确定 B.前者定大于后者 C.前者一定等于后者 D.前者一定小于后者
(5)保持温度和压强不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,a为任意值,达到平衡时仍与(1)的平衡等效。则:b、c该满足的关系为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列盐:①FeCl3 ②CH3COONa ③NaCl,其水溶液的pH由大到小排列正确的是( )
A.①>③>②
B.②>③>①
C.③>②>①
D.①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应能量变化的叙述中正确的是
A. 燃烧反应一定是放热反应
B. 只要是在点燃条件下进行的反应就一定是吸热反应
C. 只要是在常温常压下进行的反应就一定是放热反应
D. 如果反应物的总能量低于生成物的总能量,该反应一定是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 中和10 mL 0.1molL-1醋酸与中和100 mL 0.01molL-1的醋酸所需同种碱溶液的用量不同
B. 两种醋酸溶液的物质的量浓度分别c1和c2,pH分别为a和a+1,则c1=10c2
C. 常温下,pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D. 向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸俗名草酸,易溶于水,其水溶液与酸性KMnO4溶液反应的离子方程式为:2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
为了测定草酸晶体H2C2O4·xH2O中的x值,某实验小组进行实验,步骤如下:
①称取1.260g草酸晶体,配成100mL溶液。
②取25.00mL该H2C2O4溶液加入锥形瓶内,再加入适量稀硫酸。
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,至滴定达到终点。
④重复实验。记录整理数据如下:
实验序号 | V(KMnO4溶液) | |
滴定前刻度/mL | 滴定后刻度/mL | |
1 | 0.10 | 10.00 |
2 | 1.10 | 11.10 |
3 | 1.50 | 13.50 |
4 | 0.70 | 10.80 |
回答下列问题:
(1)步骤①需要使用烧杯、量筒、玻璃棒、胶头滴管,还缺少的玻璃仪器为_______(填名称);步骤③滴定过程中,盛装KMnO4溶液的仪器为__________________(填名称)。
(2)本实验滴定达到终点的标志是__________________________;
(3)根据数据,计算H2C2O4溶液的物质的量浓度为______mol/L,x=____________;
(4)若滴定终点时俯视滴定管刻度,则x值会______(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1 mol A(g)和1 mol B(g)投入一容积可变的密闭容器中,发生如下可逆反应:A(g)+B(g)![]() xC(g),经测定C在反应混合物中的物质的量分数(C%)与时间(t)符合图Ⅰ所示关系,由此推断下列说法中正确的是
xC(g),经测定C在反应混合物中的物质的量分数(C%)与时间(t)符合图Ⅰ所示关系,由此推断下列说法中正确的是
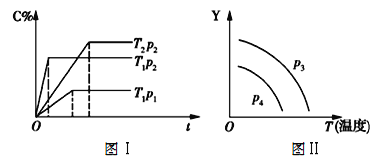
A. 在上述可逆反应中x=3
B. 在图Ⅱ中p3>p4,Y轴表示混合气体的平均摩尔质量
C. 一定温度下,向达到平衡后的容器中再加入2 mol C,重新达到平衡时,C的物质的量分数增大
D. 在图Ⅱ中p3<p4,Y轴表示A的转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com