
【题目】乙二酸俗名草酸,易溶于水,其水溶液与酸性KMnO4溶液反应的离子方程式为:2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
为了测定草酸晶体H2C2O4·xH2O中的x值,某实验小组进行实验,步骤如下:
①称取1.260g草酸晶体,配成100mL溶液。
②取25.00mL该H2C2O4溶液加入锥形瓶内,再加入适量稀硫酸。
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,至滴定达到终点。
④重复实验。记录整理数据如下:
实验序号 | V(KMnO4溶液) | |
滴定前刻度/mL | 滴定后刻度/mL | |
1 | 0.10 | 10.00 |
2 | 1.10 | 11.10 |
3 | 1.50 | 13.50 |
4 | 0.70 | 10.80 |
回答下列问题:
(1)步骤①需要使用烧杯、量筒、玻璃棒、胶头滴管,还缺少的玻璃仪器为_______(填名称);步骤③滴定过程中,盛装KMnO4溶液的仪器为__________________(填名称)。
(2)本实验滴定达到终点的标志是__________________________;
(3)根据数据,计算H2C2O4溶液的物质的量浓度为______mol/L,x=____________;
(4)若滴定终点时俯视滴定管刻度,则x值会______(填“偏大”、“偏小”或“不变”)。
【答案】 100mL容量瓶 酸式滴定管 当滴入最后一滴KMnO4溶液时,溶液由无色变为紫红色,且半分钟内不褪色,即达滴定终点 0.1000 2 )偏大
【解析】(1)配成100mL溶液使用的仪器有:量筒、玻璃棒、烧杯、100mL容量瓶、胶头滴管,所以还缺少的仪器为:100mL容量瓶;KMnO4具有强的氧化性,会氧化橡胶,不能装在碱式滴定管中,只能装在酸式滴定管中,故步骤③滴定过程中,盛装KMnO4溶液的仪器为酸式滴定管;(2)滴定终点时,略过量的KMnO4溶液显紫红色,本实验滴定达到终点的标志是:当滴入最后一滴KMnO4溶液时,溶液由无色变为紫红色,且半分钟内不褪色,即达滴定终点;
实验数据可知,四次滴定所消耗的KMnO4溶液的体积分别为:9.90mL、10.00mL、12.00mL、10.10mL,其中12.00mL相差太大,舍去,求平均值为:10.00mL,根据离子反应2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,有:
2MnO4﹣~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~5H2C2O4
2 5
0.1000mol/L×10.00mL×10-3L/mL c×25.00mL×10-3L/mL
c=![]() =0.1000mol/L;
=0.1000mol/L;
1.260g草酸晶体(H2C2O4·xH2O),配成100mL溶液,取25.00mL该H2C2O4溶液进行滴定,则草酸的物质的量为:0.1000mol/L×0.1L=0.0100mol,则有90+18x=![]() ,求得x=2;(4)若滴定终点时俯视滴定管刻度,则滴定消耗的标准液体积偏小,计算中草酸的物质的量偏小,相对分子质量偏大,则x值会偏大。
,求得x=2;(4)若滴定终点时俯视滴定管刻度,则滴定消耗的标准液体积偏小,计算中草酸的物质的量偏小,相对分子质量偏大,则x值会偏大。


科目:高中化学 来源: 题型:
【题目】实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( ) 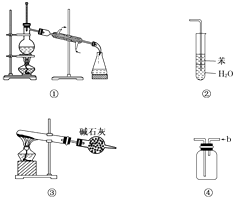
A.装置①常用于分离互不相溶的液体混合物
B.装置②可用于吸收氨气,能够防止倒吸
C.以NH4HCO3为原料,装置③可用于制备少量CO2
D.装置④a口进气可收集Cl2、NO2等气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.碳酸钙溶于醋酸溶液中:CaCO3+2H+═Ca2++CO2↑+H2O
B.氯化镁溶液和氨水混合:Mg2++2OH﹣═Mg(OH)2
C.铁与稀硝酸反应:Fe+2H+═Fe2++H2↑
D.铝片插入硝酸银溶液中 Al+3Ag+═Al3++3Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 中和10 mL 0.1molL-1醋酸与中和100 mL 0.01molL-1的醋酸所需同种碱溶液的用量不同
B. 两种醋酸溶液的物质的量浓度分别c1和c2,pH分别为a和a+1,则c1=10c2
C. 常温下,pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D. 向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚、75%乙醇、含氯消毒剂、过氧乙酸(CH3COOOH)、氯仿等均可有效灭活病毒。对于上述化学药品,下列说法错误的是
A.CH3CH2OH能与水互溶
B.NaClO通过氧化灭活病毒
C.过氧乙酸相对分子质量为76
D.氯仿的化学名称是四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种无色可溶性盐分别是由Na+、Mg2+、Ag+、Ba2+、Cl﹣、CO ![]() 、HCO
、HCO ![]() 、NO
、NO ![]() 中不同的阴阳离子所组成.A溶液与硫酸反应只有气体生成,B溶液与硫酸反应只有沉淀生成,C溶液与硫酸反应既有气体又有沉淀生成,D溶液与硫酸反应既无气体又无沉淀生成,则
中不同的阴阳离子所组成.A溶液与硫酸反应只有气体生成,B溶液与硫酸反应只有沉淀生成,C溶液与硫酸反应既有气体又有沉淀生成,D溶液与硫酸反应既无气体又无沉淀生成,则
(1)D为;(写化学式)
(2)分别写出下列反映的三个离子方程式①A与足量的硫酸溶液;
②C与足量的硫酸溶液;
③C与少量的氢氧化钠溶液 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类、油脂、蛋白质是人类基本营养物质,关于糖类、油脂、蛋白质的说法正确的是( )
A.单糖可以发生水解反应
B.油脂皂化是取代反应,硬化也是取代反应
C.蛋白质水解的最终产物均为氨基酸
D.饱和Na2SO4、CuSO4溶液均可用于蛋白质的盐析
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国本土科学家屠呦呦因为发现青蒿素而获得2015年的诺贝尔生理和医学奖.已知二羟甲戊酸是生物合成青蒿素的原料之一,下列关于二羟甲戊酸的说法正确的是( ) 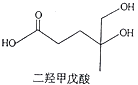
A.与乙醇发生酯化反应生成产物的分子式为C8H18O4
B.能发生加成反应,不能发生取代反应
C.在铜的催化下与氧气反应的产物可以发生银镜反应
D.标准状况下1mol该有机物可以与足量金属钠反应产生22.4L H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaC1O2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下: 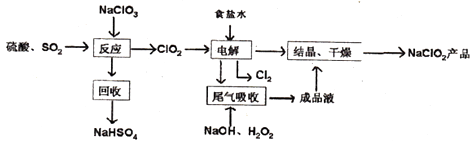
回答下列问题:
(1)“电解”所用食盐水由粗盐水精制而成,精制对,为除去Mg2+和Ca2+ , 要加入的试剂分别为、 .
(2)写出“反应”步骤中生成ClO2的化学方程式 .
(3)实验所用原料硫酸是由浓硫酸稀释而获得,写出实验过程 .
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2 . 此吸收反应中,氧化剂与还原剂的物质的量之比为 .
(5)将lmolSO2和lmolC12通入水中形成lL的溶液,所得溶液中氢离子浓度为mol/L.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com