
【题目】有A、B、C、D四种无色可溶性盐分别是由Na+、Mg2+、Ag+、Ba2+、Cl﹣、CO ![]() 、HCO
、HCO ![]() 、NO
、NO ![]() 中不同的阴阳离子所组成.A溶液与硫酸反应只有气体生成,B溶液与硫酸反应只有沉淀生成,C溶液与硫酸反应既有气体又有沉淀生成,D溶液与硫酸反应既无气体又无沉淀生成,则
中不同的阴阳离子所组成.A溶液与硫酸反应只有气体生成,B溶液与硫酸反应只有沉淀生成,C溶液与硫酸反应既有气体又有沉淀生成,D溶液与硫酸反应既无气体又无沉淀生成,则
(1)D为;(写化学式)
(2)分别写出下列反映的三个离子方程式①A与足量的硫酸溶液;
②C与足量的硫酸溶液;
③C与少量的氢氧化钠溶液 .
【答案】
(1)MgCl2
(2)2H++CO ![]() =H2O+CO2↑;2H++SO
=H2O+CO2↑;2H++SO ![]() +2HCO
+2HCO ![]() +Ba2+=BaSO4↓+2H2O+2CO2↑;OH﹣+HCO
+Ba2+=BaSO4↓+2H2O+2CO2↑;OH﹣+HCO ![]() +Ba2+=BaCO3↓+H2O
+Ba2+=BaCO3↓+H2O
【解析】解:(1)A溶液与稀硫酸混合产生无色无味的气体,说明A中含有CO ![]() 或HCO
或HCO ![]() ,B溶液与稀硫酸混合产生沉淀,则说明B中含有Ag+或Ba2+ , C溶液与硫酸反应有气体生成说明含CO
,B溶液与稀硫酸混合产生沉淀,则说明B中含有Ag+或Ba2+ , C溶液与硫酸反应有气体生成说明含CO ![]() 或HCO
或HCO ![]() 、又有沉淀生成,说明含Ag+或Ba2+ , 结合C可溶可知C为Ba(HCO3)2;Ag+和Cl﹣、CO
、又有沉淀生成,说明含Ag+或Ba2+ , 结合C可溶可知C为Ba(HCO3)2;Ag+和Cl﹣、CO ![]() 均生成沉淀,故B为和AgNO3;Mg2+和CO
均生成沉淀,故B为和AgNO3;Mg2+和CO ![]() 反应生成沉淀,故A为Na2CO3 , D为MgCl2 , 所以答案是:MgCl2;(2)①Na2CO3 与硫酸反应生成硫酸钠、二氧化碳和水,反应的离子方程式为:2H++CO
反应生成沉淀,故A为Na2CO3 , D为MgCl2 , 所以答案是:MgCl2;(2)①Na2CO3 与硫酸反应生成硫酸钠、二氧化碳和水,反应的离子方程式为:2H++CO ![]() =H2O+CO2↑,所以答案是:2H++CO
=H2O+CO2↑,所以答案是:2H++CO ![]() =H2O+CO2↑;②Ba(HCO3)2 和硫酸反应生成硫酸钡、二氧化碳和水,反应的离子方程式为:2H++SO
=H2O+CO2↑;②Ba(HCO3)2 和硫酸反应生成硫酸钡、二氧化碳和水,反应的离子方程式为:2H++SO ![]() +2HCO
+2HCO ![]() +Ba2+=BaSO4↓+2H2O+2CO2↑,所以答案是:2H++SO
+Ba2+=BaSO4↓+2H2O+2CO2↑,所以答案是:2H++SO ![]() +2HCO
+2HCO ![]() +Ba2+=BaSO4↓+2H2O+2CO2↑;②Ba(HCO3)2 和少量氢氧化钠反应,由于钡离子过量,故生成碳酸钡和水,反应的离子方程式为:OH﹣+HCO
+Ba2+=BaSO4↓+2H2O+2CO2↑;②Ba(HCO3)2 和少量氢氧化钠反应,由于钡离子过量,故生成碳酸钡和水,反应的离子方程式为:OH﹣+HCO ![]() +Ba2+=BaCO3↓+H2O;所以答案是:OH﹣+HCO
+Ba2+=BaCO3↓+H2O;所以答案是:OH﹣+HCO ![]() +Ba2+=BaCO3↓+H2O.
+Ba2+=BaCO3↓+H2O.


科目:高中化学 来源: 题型:
【题目】将足量CO2通入KOH和Ca(OH)2的混合溶液中,生成沉淀的质量(m)和通入CO2体积(V)的关系如图所示: 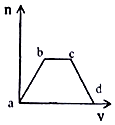
(1)ab段发生的离子反应方程式为 .
(2)bc段依次发生两个离子反应,首先是 , 其次是 .
(3)cd段发生的离子反应方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向某密闭容器中加入一定量的N2和H2发生可逆反应:N2(g)+3H2(g) ![]() 2NH3(g) ΔH = -92.2kJmol—1,测得0到10秒内,c(H2)减小了0.75molL—1,下列说法正确的是
2NH3(g) ΔH = -92.2kJmol—1,测得0到10秒内,c(H2)减小了0.75molL—1,下列说法正确的是
A.10到15秒内c(NH3) 增加量等于0.25mol L—1
B.化学反应速率关系是:3υ正(H2)= 2υ正(NH3)
C.达平衡后,分离出少量NH3,V正 增大
D.该反应的逆反应的活化能不小于92.2kJmol—1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸俗名草酸,易溶于水,其水溶液与酸性KMnO4溶液反应的离子方程式为:2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
为了测定草酸晶体H2C2O4·xH2O中的x值,某实验小组进行实验,步骤如下:
①称取1.260g草酸晶体,配成100mL溶液。
②取25.00mL该H2C2O4溶液加入锥形瓶内,再加入适量稀硫酸。
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,至滴定达到终点。
④重复实验。记录整理数据如下:
实验序号 | V(KMnO4溶液) | |
滴定前刻度/mL | 滴定后刻度/mL | |
1 | 0.10 | 10.00 |
2 | 1.10 | 11.10 |
3 | 1.50 | 13.50 |
4 | 0.70 | 10.80 |
回答下列问题:
(1)步骤①需要使用烧杯、量筒、玻璃棒、胶头滴管,还缺少的玻璃仪器为_______(填名称);步骤③滴定过程中,盛装KMnO4溶液的仪器为__________________(填名称)。
(2)本实验滴定达到终点的标志是__________________________;
(3)根据数据,计算H2C2O4溶液的物质的量浓度为______mol/L,x=____________;
(4)若滴定终点时俯视滴定管刻度,则x值会______(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用KMnO4氧化密度为1.19gcm﹣3 , 溶质质量分数为36.5%的HCl溶液.反应方程式如下:
KMnO4+HCl═ KCl+MnCl2+Cl2↑+H2O
(1)请配平方程,并用双线桥法表示该反应电子转移情况
(2)盐酸的物质的量浓度
(3)15.8gKMnO4能氧化 mol的HCl,转移电子数约为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组为探究ClO﹣、I2、SO ![]() 在酸性条件下的氧化性强弱,已知I2遇淀粉变蓝,设计实验如下: 实验①:在淀粉KI溶液中加入少量NaClO溶液,并加入少量的稀H2SO4 , 溶液立即变蓝;
在酸性条件下的氧化性强弱,已知I2遇淀粉变蓝,设计实验如下: 实验①:在淀粉KI溶液中加入少量NaClO溶液,并加入少量的稀H2SO4 , 溶液立即变蓝;
实验②:向实验①的溶液中加入4L 0.5mol/L的Na2SO3溶液,发生反应如下
SO ![]() +I2+H2O→SO
+I2+H2O→SO ![]() +I﹣+H+(未配平),恰好完全反应.
+I﹣+H+(未配平),恰好完全反应.
(1)以上实验说明,在酸性条件下ClO﹣、I2、SO42﹣的氧化性由弱到强的顺序是 .
(2)实验②中化学反应转移电子的物质的量是 .
(3)写出实验①中发生反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积均为1.0 L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应 CO2(g)+C(s)![]() 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是

A. 反应 CO2(g)+C(s)![]() 2CO(g)的 ΔS>0、ΔH<0
2CO(g)的 ΔS>0、ΔH<0
B. 体系的总压强p总:p总(状态Ⅱ)<2p总(状态Ⅰ)
C. 体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D. 逆反应速率v逆::v逆(状态Ⅰ)>v逆(状态Ⅲ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA表示阿伏加德罗常数,则下列说法不正确的是
A. 23g 钠在空气中充分燃烧,转移的电子数为NA
B. 50ml 12mol/L的盐酸与足量的MnO2共热,充分反应后,转移电子数为0.3NA
C. 0.6mol过氧化钠晶体中所含阴离子的数目为0.6NA
D. 常温常压下,8.8gN2O 和CO2混合气体所含的原子总数为0.6NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com